Clear Sky Science · fr
Le ciprofol atténue les lésions cérébrales d’ischémie‑reperfusion chez le rat en inhibant la ferroptose via l’activation d’AMPK
Pourquoi protéger le cerveau après un AVC est crucial
Lorsqu’une personne subit un AVC ischémique, les médecins s’efforcent de rouvrir le vaisseau obstrué et de rétablir l’apport sanguin au cerveau. Paradoxalement, cette intervention salvatrice peut elle‑même provoquer des dommages supplémentaires, un phénomène appelé lésion de reperfusion. Le cerveau, soudain inondé d’oxygène et de nutriments après une période de privation, déclenche une tempête de réactions chimiques susceptibles de tuer des neurones vulnérables. Cette étude examine si le ciprofol, un nouvel anesthésique déjà utilisé pour la sédation, peut aussi protéger le cerveau pendant cette fenêtre critique en atténuant certains des processus les plus nocifs activés au retour du flux sanguin.
Du flux sanguin bloqué aux lésions cérébrales
Pour reproduire ce qui se passe lors d’un AVC humain, les chercheurs ont bloqué temporairement une artère cérébrale majeure chez le rat puis ont rétabli la circulation, générant ce qu’on appelle une lésion cérébrale d’ischémie–reperfusion. Certains rats ont simplement subi la procédure, tandis que d’autres ont reçu du ciprofol peu après le rétablissement du flux sanguin. L’équipe a ensuite évalué la capacité des animaux à se déplacer et à répondre au toucher, et examiné leur cerveau pour localiser les zones de tissu nécrosé et les altérations structurelles des cellules nerveuses. Les rats traités au ciprofol présentaient des zones de lésion cérébrale plus petites, des neurones d’aspect plus sain, et de meilleurs scores moteurs et sensoriels que les animaux non traités, suggérant que le médicament a atténué les pires conséquences de l’insulte.
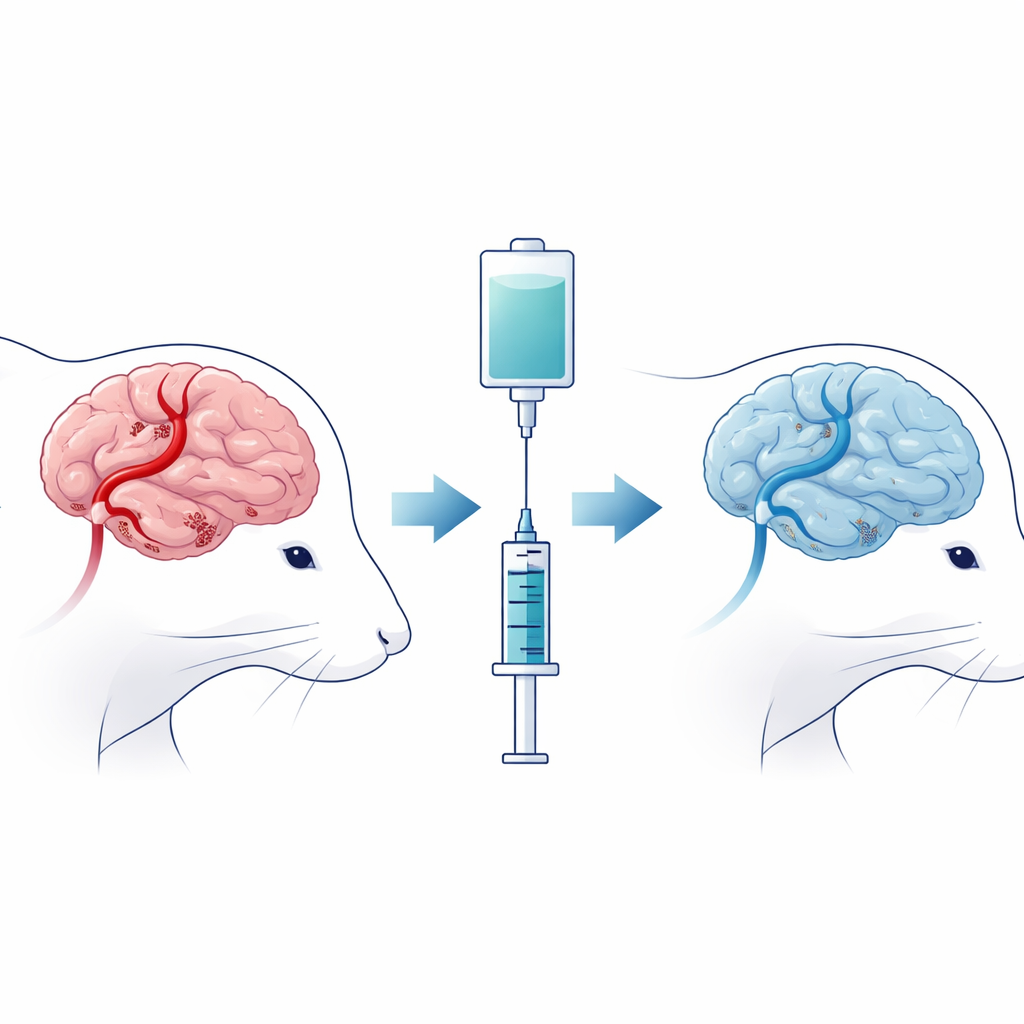
Une forme de mort cellulaire liée au fer
Au‑delà des lésions tissulaires visibles, les auteurs se sont intéressés à une forme de mort cellulaire récemment reconnue, la ferroptose, qui est alimentée par le fer et des réactions chimiques incontrôlées attaquant les composants lipidiques des membranes cellulaires. Chez les rats témoins du modèle d’AVC, le tissu cérébral de la zone vulnérable autour du noyau de la lésion contenait davantage de fer, des niveaux plus élevés d’un produit de dégradation lipidique, et des mitochondries neuronales gonflées et structurées de manière altérée à l’électronique. Les tests moléculaires ont montré que les protéines protectrices qui détoxifient normalement ces produits lipidiques nocifs étaient diminuées, tandis que les protéines favorisant ce processus destructeur étaient augmentées. Le ciprofol a largement inversé ces changements : le fer et les dommages lipidiques ont diminué, l’équilibre des protéines clés a basculé en faveur de la protection, et les mitochondries ont conservé des formes et une ultrastructure plus normales.
Un senseur d’énergie cellulaire comme interrupteur de contrôle
L’étude a ensuite investigué comment le ciprofol produit ces effets protecteurs. L’attention s’est portée sur AMPK, une protéine qui agit comme senseur d’énergie cellulaire et comme répondeur au stress. Dans les cerveaux lésés des rats non traités, l’activité d’AMPK était déprimée. Le ciprofol a augmenté la forme activée d’AMPK, en parallèle avec la réduction des dommages liés à la ferroptose. Pour tester si ce senseur d’énergie se situe véritablement en amont de la chaîne d’événements protecteurs, les chercheurs ont utilisé un autre composé, le Compound C, qui bloque AMPK. Lorsque les animaux ont reçu à la fois du ciprofol et cet inhibiteur d’AMPK, les bénéfices du ciprofol ont été partiellement perdus : les marqueurs associés à la ferroptose sont revenus vers des niveaux délétères, l’accumulation de fer est réapparue, et le signal d’activité d’AMPK a chuté encore plus bas que chez les animaux AVC non traités. Ce schéma soutient l’idée que l’activation d’AMPK est une étape clé par laquelle le ciprofol protège les cellules cérébrales.
Atténuer la tempête inflammatoire cérébrale
Les lésions liées à l’AVC ne se limitent pas à la mort neuronale intrinsèque ; la réponse immunitaire cérébrale joue également un rôle majeur. L’équipe a mesuré plusieurs molécules messagères inflammatoires qui augmentent typiquement après l’ischémie–reperfusion. Chez les animaux non traités, ces signaux étaient fortement élevés, reflétant une réaction inflammatoire intense. Le ciprofol a réduit les trois principaux marqueurs inflammatoires mesurés, suggérant qu’il supprime non seulement les dommages membranaires induits par le fer mais qu’il tempère aussi la tempête inflammatoire qui s’ensuit. Lorsque AMPK a été bloqué par le Compound C, ces effets anti‑inflammatoires ont été atténués, reliant encore une fois les bénéfices du ciprofol à cette voie centrale de détection énergétique.
Ce que cela pourrait signifier pour les soins futurs
Dans l’ensemble, ces résultats désignent le ciprofol comme plus qu’un simple sédatif : dans ce modèle rat, il semble limiter les lésions cérébrales liées à l’AVC en activant AMPK, ce qui à son tour freine la mort cellulaire pilotée par le fer et atténue l’inflammation. Comme le ciprofol est déjà utilisé en clinique pour l’anesthésie et la sédation procédurale, son potentiel additionnel comme agent neuroprotecteur est particulièrement prometteur. Néanmoins, le travail présente des limites importantes, notamment la dépendance à un seul modèle animal et la possibilité que l’inhibiteur d’AMPK ait des effets secondaires propres. D’autres études, y compris dans d’autres espèces et, en dernier ressort, chez des patients humains, seront nécessaires pour confirmer si le ciprofol peut aider en toute sécurité à protéger le cerveau pendant et après le traitement de l’AVC.
Citation: Zeng, H., Yu, X., Zheng, Z. et al. Ciprofol attenuates cerebral Ischemia‒reperfusion injury in rats by inhibiting ferroptosis through upregulating AMPK. Sci Rep 16, 9282 (2026). https://doi.org/10.1038/s41598-026-40104-6
Mots-clés: accident vasculaire ischémique, lésions de reperfusion, ciprofol, ferroptose, neuroprotection