Clear Sky Science · fr
Le mécanisme antitumoral de l’oclacitinib dans le lymphome canin
Pourquoi cela compte pour les chiens et leurs familles
Le lymphome est l’un des cancers les plus fréquents chez le chien de compagnie. Si la chimiothérapie aide de nombreux patients, elle n’est pas toujours efficace et peut entraîner des effets indésirables importants. L’oclacitinib, un comprimé déjà largement prescrit aux chiens qui souffrent de démangeaisons liées à des maladies allergiques de la peau, a récemment montré des bénéfices surprenants chez certains chiens atteints d’un lymphome cutané. Cette étude pose une question simple mais essentielle : comment, exactement, ce médicament anti-allergie courant peut-il agir contre des cellules cancéreuses, et peut-on prédire quels chiens sont les plus susceptibles d’en bénéficier ?
De médicament anti-allergique à agent anticancéreux
L’oclacitinib a été développé pour calmer des signaux immunitaires hyperactifs qui provoquent la dermatite atopique. Il agit en bloquant une famille d’interrupteurs moléculaires appelés JAK, en particulier JAK1, qui relaient des messages depuis les molécules inflammatoires à la surface des cellules jusqu’au noyau. Des vétérinaires ont commencé à remarquer que certains chiens atteints d’une forme de lymphome cutané s’amélioraient lorsqu’on leur donnait de l’oclacitinib, mais les raisons restaient floues et les réponses étaient variables. Les chercheurs ont donc entrepris d’étudier cela de façon contrôlée, en utilisant des cellules de lymphome cultivées en laboratoire issues de chiens, ainsi que des échantillons de patients canins réels, pour déterminer quand et comment l’oclacitinib peut effectivement tuer des cellules tumorales plutôt que simplement apaiser la peau. 
Tests sur des cellules de lymphome en laboratoire
L’équipe a examiné une lignée cellulaire de lymphome cutané canin et huit autres lignées de lymphome de haut grade représentant des cancers des cellules T et B. Lorsqu’ils ont exposé ces cellules à l’oclacitinib à des concentrations proches de celles atteintes chez les chiens traités, environ la moitié des lignées a présenté un ralentissement net de la croissance et plusieurs ont déclenché la mort cellulaire. Les cellules sensibles se sont accumulées en phase de repos du cycle cellulaire et ont présenté des signes caractéristiques de mort programmée, notamment l’activation d’une protéine exécutoire appelée caspase-3. En revanche, d’autres lignées de lymphome ont à peine réagi dans la même plage de concentration, soulignant que le lymphome chez le chien n’est pas une maladie unique mais un ensemble de cancers biologiquement distincts.
Localiser une voie de signalisation vulnérable
Pour comprendre ce qui séparait les tumeurs sensibles des résistantes, les scientifiques se sont concentrés sur la voie de signalisation JAK/STAT, un circuit de survie fréquent dans de nombreuses hémopathies. Ils ont trouvé que seules les lignées de lymphome répondant à l’oclacitinib présentaient une activation de base marquée de deux acteurs clés : JAK1 et STAT5. Lors du traitement de ces cellules sensibles par l’oclacitinib, l’activité de STAT5 chutait nettement, tandis que les niveaux globaux des protéines restaient inchangés. Un second médicament bloquant JAK1 utilisé en médecine humaine, le filgotinib, a produit un schéma similaire d’inhibition de la croissance et d’extinction de STAT5. Un profilage approfondi de l’activité génique a révélé que l’oclacitinib atténuait des ensembles de gènes liés à la signalisation JAK/STAT et réduisait l’expression de c-Myc, un régulateur majeur de la croissance souvent détourné dans les cancers, ce qui aide à expliquer l’arrêt du cycle cellulaire et la mort cellulaire observés. 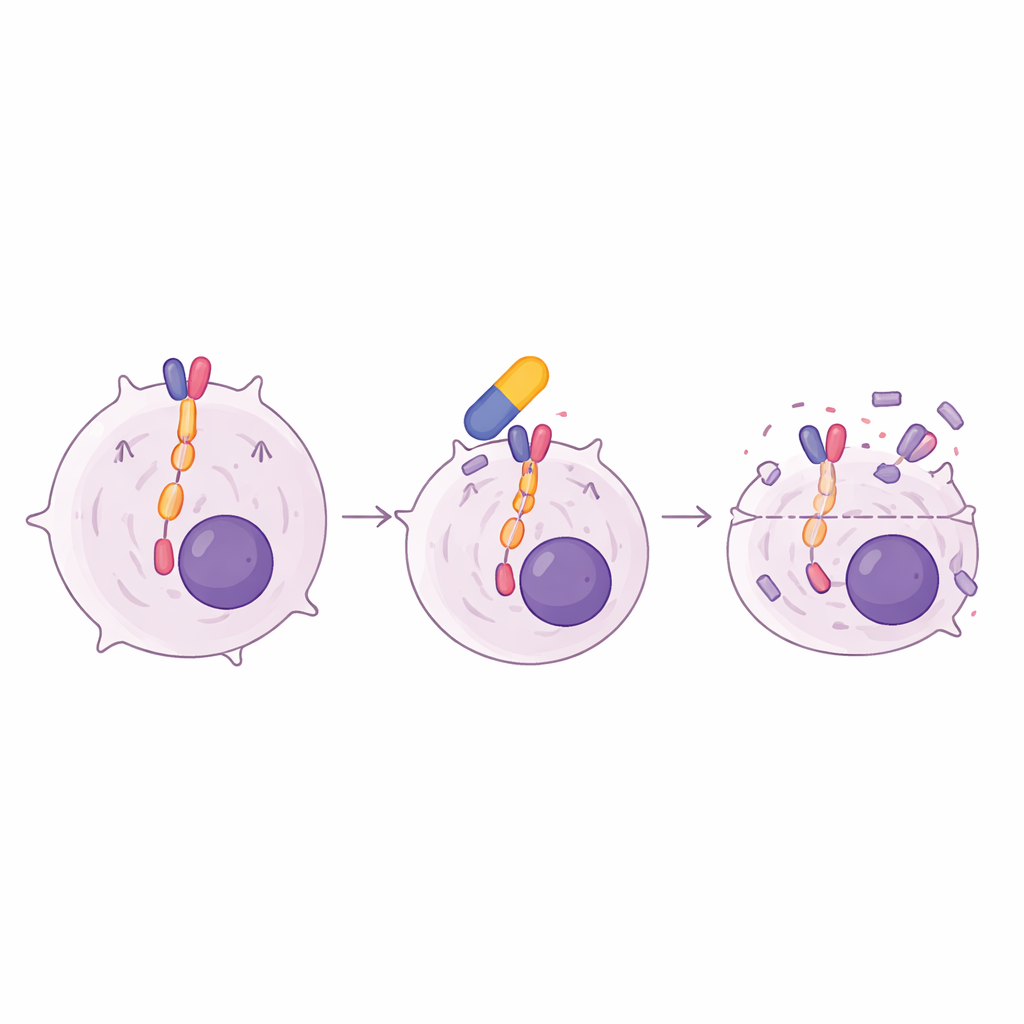
Relier les résultats de laboratoire aux patients canins
Les chercheurs se sont ensuite tournés vers des échantillons de biopsies de chiens atteints de lymphome cutané traités par oclacitinib en clinique. Grâce à des méthodes de coloration révélant les protéines activées, ils ont constaté que les chiens dont les tumeurs présentaient une activation de JAK1 et STAT5 étaient plus susceptibles d’avoir des réponses partielles ou complètes au médicament. Certains non-répondeurs présentaient néanmoins ces signaux activés, suggérant que des voies d’échappement supplémentaires peuvent soutenir certaines tumeurs, mais le schéma global montrait une association marquée. Fait important, de nombreux échantillons de lymphomes des ganglions lymphatiques et intestinaux provenant d’autres chiens présentaient également ce même profil d’activation JAK1/STAT5, soulevant la possibilité que les bénéfices de l’oclacitinib s’étendent au-delà du lymphome cutané à un plus large éventail de lymphomes canins agressifs.
Ce que cela pourrait signifier pour les traitements futurs
En somme, ce travail montre que l’oclacitinib peut directement freiner et parfois tuer certaines cellules de lymphome canin en désactivant une voie de survie clé centrée sur JAK1 et STAT5 et en diminuant l’activité de gènes favorisant la croissance tels que c-Myc. Les lymphocytes normaux de chiens sains étaient beaucoup moins affectés à des doses cliniquement pertinentes, bien que des concentrations élevées ralentissent l’expansion de cellules immunitaires activées, ce qui souligne la nécessité de concilier effets anticancéreux et suppression immunitaire potentielle. L’étude suggère que le dépistage tumoral pour JAK1 et STAT5 activés pourrait aider les vétérinaires à identifier les chiens les plus susceptibles de bénéficier de l’oclacitinib et de médicaments similaires. Bien que des essais cliniques supplémentaires soient nécessaires, ce médicament anti-allergie largement disponible pourrait entrer dans une boîte à outils de traitements ciblés pour le lymphome canin, guidé par des marqueurs moléculaires simples.
Citation: Harada, M., Inanaga, S., Sakurai, M. et al. The antitumor mechanism of oclacitinib in canine lymphoma. Sci Rep 16, 8427 (2026). https://doi.org/10.1038/s41598-026-40066-9
Mots-clés: lymphome canin, oclacitinib, voie JAK1 STAT5, thérapie ciblée contre le cancer, oncologie vétérinaire