Clear Sky Science · fr
MyoFuse est un flux de travail entièrement basé sur l’IA pour la quantification automatisée de la fusion des cellules musculaires squelettiques in vitro
Pourquoi compter les cellules musculaires importe
Lorsque nous faisons de l’exercice, que nous récupérons d’une blessure ou que nous développons des maladies comme le diabète, nos muscles squelettiques se remodelent en permanence. En laboratoire, les scientifiques reproduisent ce processus en cultivant des cellules musculaires dans une boîte de culture et en observant des cellules individuelles fusionner en longs fibres multi‑nucléées. Un simple nombre, l’indice de fusion, indique à quel point cette fusion se déroule bien. Mais aujourd’hui, ce chiffre est généralement obtenu par des personnes comptant manuellement des milliers de petits noyaux cellulaires à l’écran — un travail lent, sujet à incohérences et aux erreurs. Cette étude présente MyoFuse, un flux de travail entièrement fondé sur l’IA qui automatise cette tâche de comptage, visant à rendre la recherche sur le muscle plus rapide, plus fiable et moins biaisée.
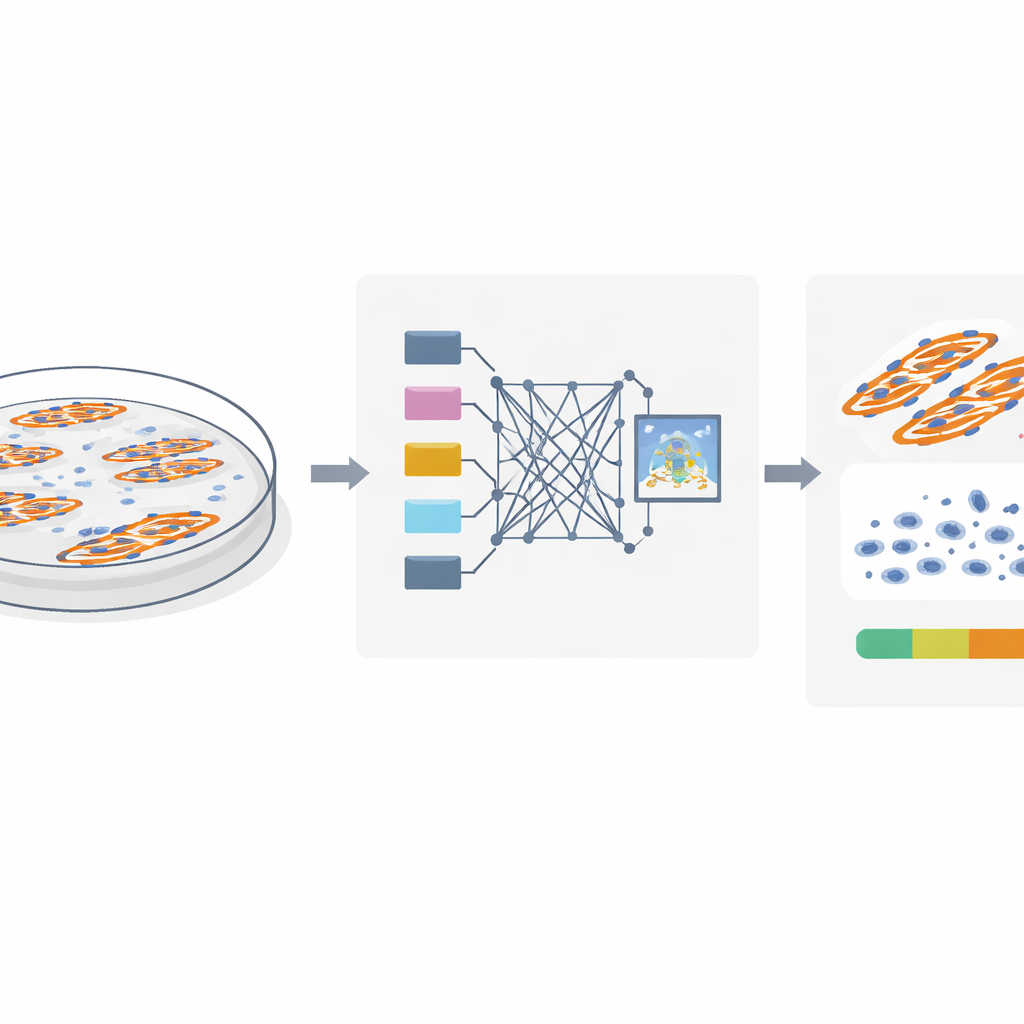
Le défi de voir ce qui est vraiment présent
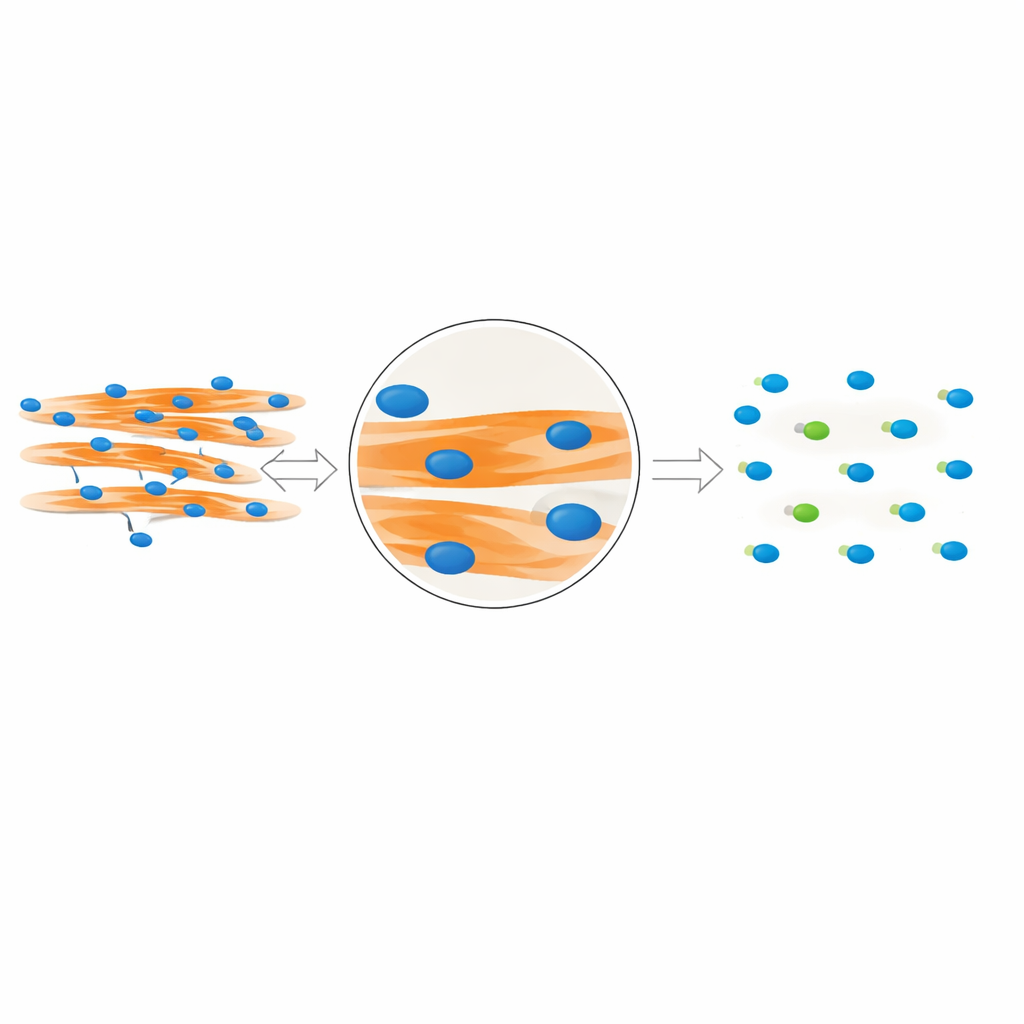
Pour étudier la fusion des cellules musculaires, les chercheurs colorent les noyaux et les fibres musculaires avec des colorants fluorescents et prennent des images au microscope. La question clé est de savoir quels noyaux sont réellement à l’intérieur des fibres fusionnées et lesquels appartiennent à des cellules non fusionnées situées à proximité. Les méthodes traditionnelles supposent que si un noyau chevauche une fibre musculaire dans une image plane en deux dimensions, il doit en faire partie. Cependant, les cellules se développent en trois dimensions : un noyau peut facilement se trouver au‑dessus ou au‑dessous d’une fibre et donner l’illusion d’un chevauchement dans l’image. Les auteurs utilisent des images confocales détaillées sur des cellules musculaires de souris et humaines pour montrer que cette astuce du chevauchement peut être trompeuse, amenant de nombreux noyaux voisins à être comptés à tort comme faisant partie de fibres fusionnées et gonflant ainsi l’indice de fusion.
Une manière plus intelligente d’interpréter les images fluorescentes
L’équipe a constaté que les vrais noyaux «dans la fibre» laissent une empreinte visuelle distincte. Parce que ces noyaux occupent physiquement de l’espace à l’intérieur de la fibre, ils créent de petits creux sombres dans le signal fluorescent qui marque la protéine musculaire MyHC. En revanche, les noyaux situés au‑dessus ou au‑dessous d’une fibre ne perturbent pas ce signal. En s’appuyant sur cette observation, les auteurs ont conçu MyoFuse, un flux de travail en deux étapes basé sur l’IA. D’abord, un modèle de segmentation spécialisé (adapté de l’outil open source Cellpose) délimite précisément les noyaux individuels, même lorsqu’ils sont fortement agrégés en amas. Ensuite, un classificateur neuronal léger examine le signal MyHC environnant pour chaque noyau et décide s’il se trouve à l’intérieur d’une fibre musculaire ou à l’extérieur, en se fondant uniquement sur ce motif local plutôt que sur un simple chevauchement.
Dans quelle mesure l’IA concorde avec des experts humains
Les chercheurs ont testé rigoureusement MyoFuse sur des images de cellules musculaires C2C12 de souris et de cellules musculaires humaines primaires provenant de différents muscles. Pour les deux espèces, le comptage total des noyaux par l’IA et l’indice de fusion calculé concordaient très bien avec des annotations manuelles soignées réalisées par des experts, avec des corrélations quasi parfaites. Au niveau des noyaux individuels, le classificateur a correctement distingué les noyaux à l’intérieur et à l’extérieur des fibres dans plus de 90 % des cas à travers les jeux de données, avec des métriques de performance rivalisant avec la discrimination de niveau humain. Fait important, MyoFuse a également bien fonctionné sur un jeu séparé de cellules humaines qui n’avait jamais été utilisé pour l’entraînement, ce qui suggère que l’approche peut se généraliser à de nouveaux échantillons plutôt que de se contenter de mémoriser les images d’entraînement.
Révéler un biais caché dans les méthodes courantes
Au‑delà de son exactitude, MyoFuse a mis en évidence des problèmes systémiques dans des méthodes à base de masques largement utilisées qui reposent sur le simple chevauchement des signaux de noyaux et de fibres. Lorsque les auteurs ont comparé les indices de fusion obtenus avec MyoFuse à ceux issus d’une approche à masque raffinée appliquée aux mêmes images, la méthode à masque surestimait systématiquement la fusion, en particulier dans les zones où les fibres musculaires couvraient une plus grande fraction de la surface de la culture. Ajuster les seuils de détection modifiait les chiffres mais n’éliminait pas ce biais de fond ; les améliorations apparentes provenaient souvent d’erreurs qui s’annulent plutôt que d’une meilleure capture de la biologie. L’équipe a également montré que les estimations de fusion peuvent varier largement entre différentes régions d’un même puits, soulignant que l’analyse de quelques champs choisis manuellement peut donner une vue déformée de la qualité de la fusion cellulaire.
Ce que cela signifie pour la recherche future sur le muscle
MyoFuse offre aux biologistes du muscle une manière de mesurer la fusion cellulaire à la fois plus rapide et plus fidèle à ce qui se passe réellement dans la boîte de culture. En combinant la microscopie automatisée avec une IA capable de segmenter et classifier des centaines de milliers de noyaux en quelques minutes, le flux de travail réduit la charge de travail humaine, minimise les choix subjectifs sur les zones à analyser et la définition des seuils d’image, et évite de compter comme fusionnées des cellules simplement proches. Les auteurs reconnaissent que des conditions d’imagerie extrêmes ou des protocoles de marquage très différents peuvent nécessiter un réentraînement, mais la méthode est disponible en accès ouvert et conçue pour être adaptable. Pour les laboratoires étudiant le développement musculaire, le vieillissement, la régénération ou les maladies métaboliques, MyoFuse promet des mesures de fusion plus robustes — et, par conséquent, des conclusions plus fiables sur la façon dont les muscles croissent et évoluent.
Citation: Lair, B., Cazorla, C., Lobeto, A. et al. MyoFuse is a fully AI-based workflow for automated quantification of skeletal muscle cell fusion in vitro. Sci Rep 16, 9387 (2026). https://doi.org/10.1038/s41598-026-40047-y
Mots-clés: muscle squelettique, fusion cellulaire, intelligence artificielle, analyse d’images, myogenèse