Clear Sky Science · fr
Embigin participe à la régulation du développement rénal précoce chez la souris
Pourquoi de petits reins comptent
Avant la naissance, les organes d’un bébé suivent un processus de construction complexe où les cellules doivent se diviser, se déplacer et se connecter de façon très précise. Les reins, qui filtrent le sang et maintiennent l’équilibre hydrique et sodé de l’organisme, sont constitués de tubes ramifiés qui poussent comme les branches d’un arbre. Cette étude examine une protéine de surface peu connue appelée embigin et montre qu’elle contribue discrètement à guider la morphogenèse précoce du rein chez la souris — en particulier la formation des premières ramifications — fournissant des éléments sur la coordination de la croissance des organes et sur ce qui peut mal tourner en cas de pathologie.
Un aide à la surface cellulaire
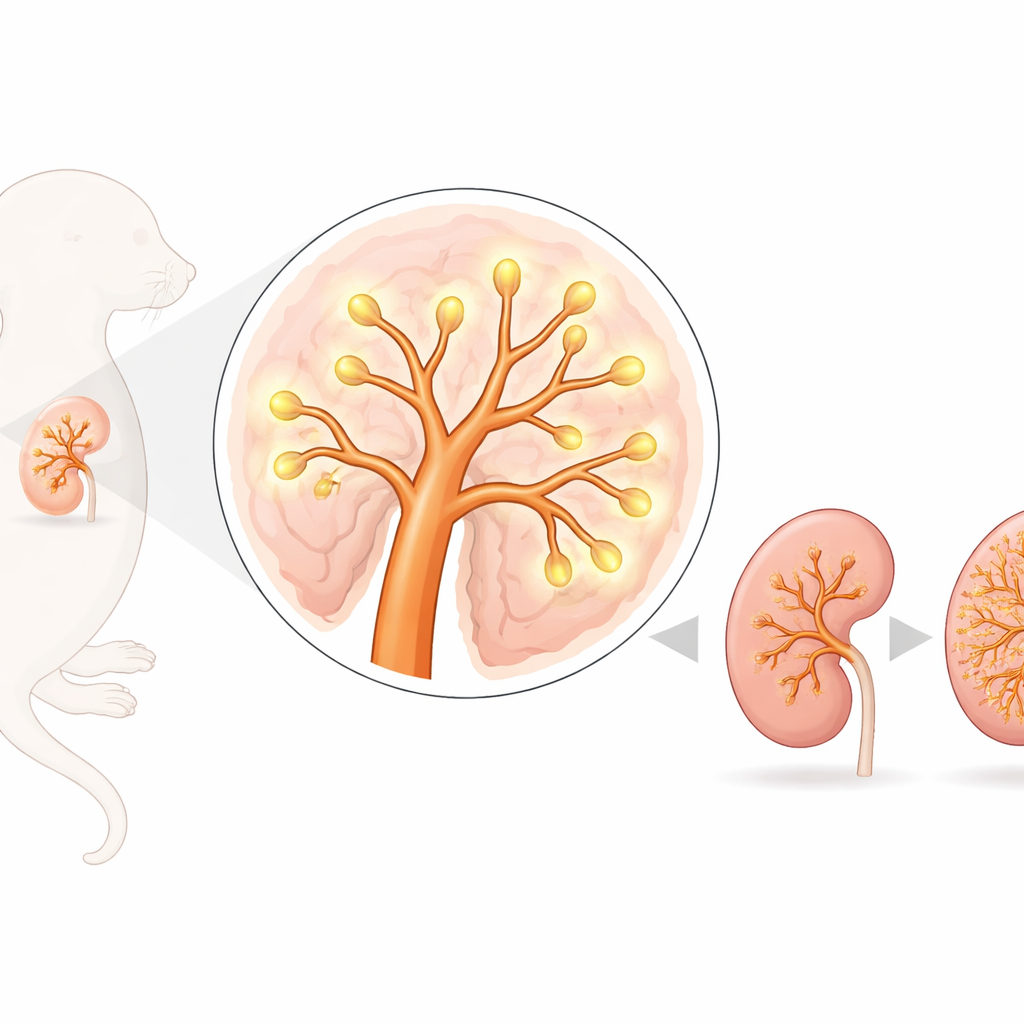
Embigin est située à la membrane externe des cellules et aide certains transporteurs qui acheminent de petites molécules métaboliques à l’intérieur et à l’extérieur des cellules. Elle peut aussi se lier à des éléments de l’échafaudage tissulaire qui entoure les cellules. Des travaux antérieurs ont montré que les souris privées d’embigin présentent des troubles du développement pulmonaire et meurent souvent peu après la naissance, suggérant que cette protéine est importante pour la construction des organes. Ici, les chercheurs ont voulu savoir si embigin joue un rôle similaire dans le rein, dont le développement commence par une simple excroissance qui se divise à plusieurs reprises pour former le futur système de collecte des urines et déclenche la formation d’unités filtrantes appelées néphrons.
Orientation de la ramification rénale précoce
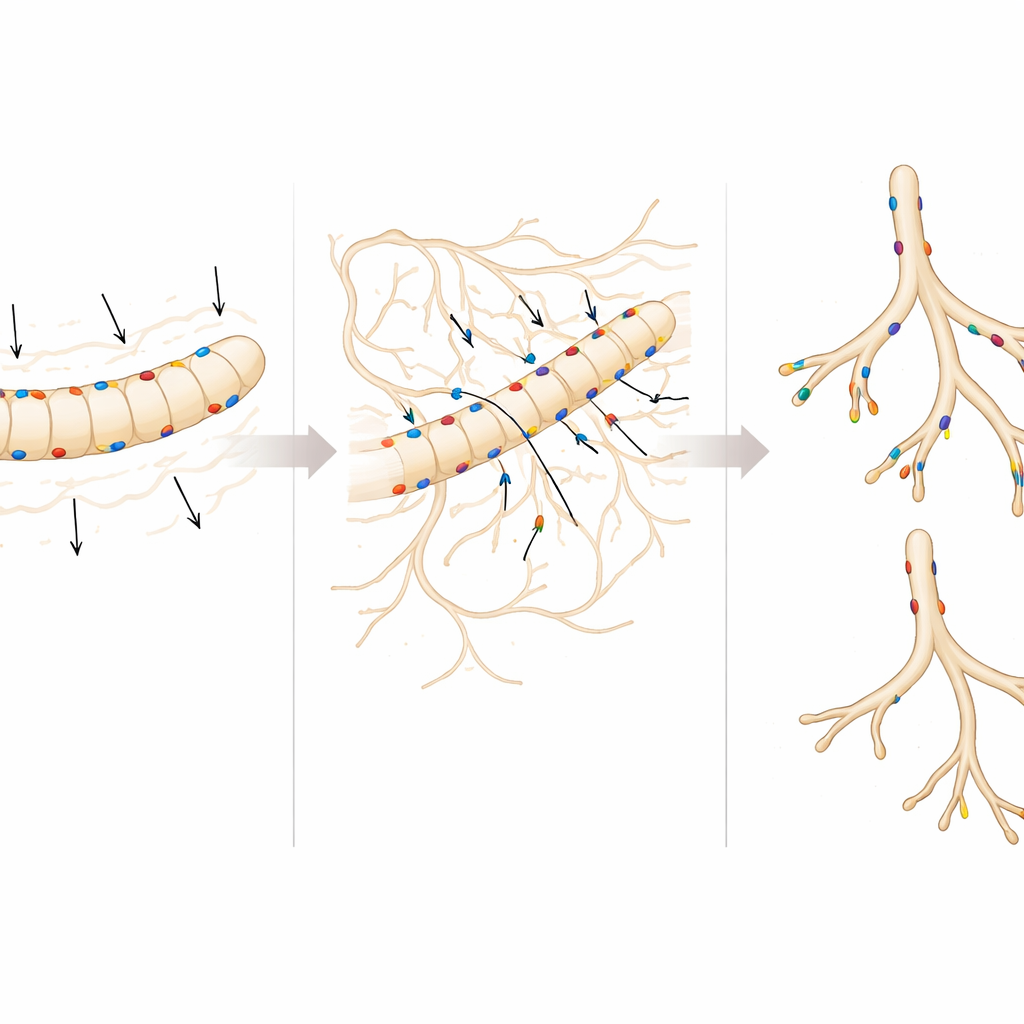
Par microscopie à fluorescence, l’équipe a constaté qu’embigin est fortement exprimée dans les tubes ramifiés du rein précoce — connus sous le nom de bourgeon urétéral — et dans les cellules en voie de différenciation en néphrons, mais pas dans les cellules souches rénales les plus primitives qui coiffent les pointes en croissance. Lorsque des reins embryonnaires issus de souris normales et dépourvues d’embigin ont été cultivés à un stade précoce, la différence était nette : les reins sans embigin produisaient beaucoup moins d’extrémités ramifiées, et les reins étaient globalement plus petits plus tard pendant la gestation. Toutefois, en comparant la taille du rein à la taille corporelle globale, les ratios étaient semblables, ce qui suggère qu’embigin contribue à la croissance générale autant qu’à la morphogenèse spécifique du rein.
Un développement retardé, non détruit
Pour comprendre les mécanismes moléculaires, les chercheurs ont mesuré l’activité génique dans des reins en développement. À un stade de mi-gestation, les reins sans embigin présentaient une activité réduite de dizaines de gènes liés à la formation des néphrons, au façonnage des tubes, au contrôle de la pression artérielle et à la gestion des fluides corporels. Plusieurs des gènes les plus affectés sont cruciaux pour des cellules spécialisées appelées podocytes, qui font partie de la barrière de filtration du rein. Pourtant, à un stade ultérieur, ces différences d’expression génique avaient en grande partie disparu et la structure rénale paraissait normale au microscope. Les souris adultes survivantes sans embigin ne présentaient pas de fuite de protéines dans les urines et n’avaient pas de défauts rénaux structuraux évidents, ce qui indique un retard de développement temporaire plutôt qu’un dommage permanent.
Signaux communs entre les tissus
L’équipe s’est ensuite tournée vers une lignée cellulaire épithéliale de souris, en silencant embigin pour voir quels gènes changeaient. Même si ces cellules ne provenaient pas du rein, la perte d’embigin modifiait à nouveau de nombreux gènes impliqués dans la morphogenèse des organes, la formation de tubes et des voies liées au rein. La comparaison des données de la lignée cellulaire avec celles du rein précoce a mis en évidence trois gènes — Pappa2, Acta2 et Tagln — qui étaient systématiquement réduits en l’absence d’embigin. Ces gènes sont associés au développement rénal, au tonus des vaisseaux sanguins et au mouvement cellulaire, des processus dépendant de la façon dont les cellules détectent et s’accrochent à leur matrice environnante. Une réanalyse de jeux de données de séquençage ARN unicellulaire provenant d’embryons très précoces a montré qu’embigin est déjà active dans les précurseurs rénaux les plus précoces, renforçant l’idée qu’elle soutient des décisions clés au début de la formation des organes.
Ce que cela signifie pour la construction des organes
Dans l’ensemble, les résultats présentent embigin comme un organisateur subtil mais important de la croissance rénale précoce. Elle ne semble pas absolument indispensable à l’obtention d’un rein fonctionnel — d’autres protéines peuvent finir par compenser — mais elle aide à assurer une ramification en temps voulu de l’arbre tubulaire précoce et l’activation correcte des réseaux géniques qui façonnent les néphrons et les structures de filtration sanguine. Pour le lecteur non spécialiste, le message est que des protéines de surface apparemment obscures peuvent avoir des effets étendus sur la morphogenèse des organes, et que mieux comprendre ces aides discrètes peut un jour améliorer notre compréhension des malformations rénales congénitales et guider des stratégies de croissance ou de réparation du tissu rénal.
Citation: Talvi, S., Jokinen, J., Rappu, P. et al. Embigin is involved in the regulation of early mouse kidney development. Sci Rep 16, 8403 (2026). https://doi.org/10.1038/s41598-026-39966-7
Mots-clés: développement rénal, embigin, <keyword>cellules souches, formation d'organes