Clear Sky Science · fr
Perspectives protéomiques sur un isolat clinique de M. tuberculosis présentant une plus grande propension à former des sous-populations viables mais non répliquantes lors d’un stress acide
Pourquoi cela compte pour le traitement de la tuberculose
La tuberculose reste l’une des maladies infectieuses les plus meurtrières au monde, et son traitement nécessite de longs mois d’antibiotiques. Une raison importante est que certains bacilles tuberculeux peuvent entrer dans un état de latence où ils restent vivants mais cessent de se multiplier, ce qui les rend difficiles à éliminer avec les médicaments standards. Cette étude examine comment une souche clinique réelle de Mycobacterium tuberculosis réagit à des conditions acides similaires à celles rencontrées à l’intérieur des cellules immunitaires, et comment cette réponse peut aider la bactérie à survivre au traitement.
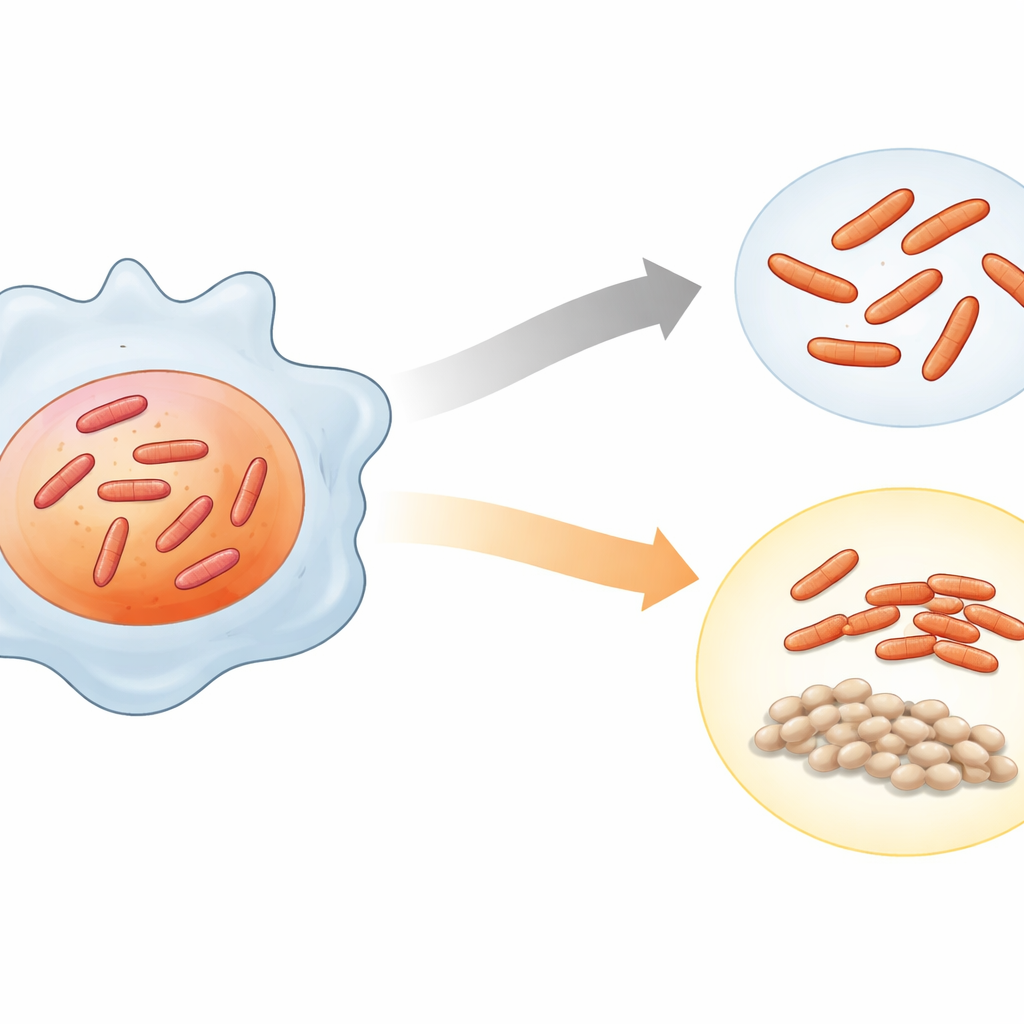
Un test de stress pour des bactéries d’origine patient
Les chercheurs se sont concentrés sur une souche clinique appelée S169, prélevée chez un patient resté à culture positive même après le traitement standard de six mois, malgré une sensibilité de la souche aux médicaments. Des travaux antérieurs avaient montré que cette souche a tendance à former des sous-populations « viables mais non répliquantes » (VBNR) — des bactéries vivantes mais qui ne se divisent pas activement. Pour reproduire les conditions hostiles à l’intérieur des cellules immunitaires, l’équipe a exposé les bactéries à un milieu acide en laboratoire, en les faisant passer d’un pH proche de la neutralité (6,5) à un pH plus acide (4,5) pendant deux jours.
Observer les bactéries ralentir sans mourir
Pour distinguer les cellules qui continuaient à se diviser de celles qui entraient en latence, les chercheurs ont utilisé un système ingénieux de double rapporteur fluorescent intégré à la bactérie. Un signal fluorescents indiquait que les cellules étaient vivantes ; l’autre s’estompait à chaque division. En conditions normales, le signal rouge se diluait avec la multiplication bactérienne. Sous stress acide, toutefois, une fraction notable de cellules a conservé une forte fluorescence rouge tout en restant viables, indiquant qu’environ une cellule sur six était devenue VBNR. Cela confirme que l’acidité seule peut pousser cette souche clinique vers un état de tolérance aux médicaments, de croissance ralentie ou nulle, similaire à ce qui est observé lors de l’infection.
Prenant un instantané protéique à l’intérieur des cellules stressées
Les scientifiques ont ensuite examiné des milliers de protéines à l’intérieur des bactéries pour voir comment l’environnement acide remodelait leur machinerie interne. Certains systèmes classiques de réponse au stress étaient activés, notamment un régulateur appelé TcrX et des méthyltransférases déjà associées à l’acide et à d’autres conditions hostiles. En revanche, de nombreuses protéines habituellement liées à la dormance et au stress — en particulier celles contrôlées par le régulon maître DosR — étaient en fait moins abondantes que chez des bactéries cultivées à pH neutre. Les protéines impliquées dans la réplication de l’ADN, la réparation et la division cellulaire étaient également réduites, cohérent avec le ralentissement de la croissance observé. Ce profil suggère que cette souche clinique gère le stress différemment de la souche de laboratoire standard, en s’appuyant sur un programme protéique distinct pour résister aux conditions acides.
Ce que les bactéries choisissent de relâcher
Ensuite, l’équipe a examiné les protéines présentes à l’extérieur des cellules dans le liquide de culture, en utilisant une méthode de préparation d’échantillons conçue pour capturer même les molécules sécrétées en faible abondance. Ils ont détecté un peu plus d’un millier de protéines et trouvé près de 600 dont les niveaux différaient entre les conditions normales et acides. Sous stress acide, moins de types de protéines apparaissaient globalement, et de nombreuses enzymes métaboliques étaient moins abondantes à l’extérieur de la cellule, reflétant un ralentissement général. En revanche, plusieurs lipoprotéines et protéases étaient plus abondantes, y compris des protéines connues pour aider les bactéries à résister à l’acidité et à moduler les interactions avec le système immunitaire de l’hôte. Ils ont également détecté plusieurs couples toxine–antitoxine et une enzyme sécrétée, la chorismate mutase, qui a été liée à la capacité des mycobactéries à empêcher la mort des cellules immunitaires infectées.
Ce que cela signifie pour les patients et la recherche future
Ensemble, ces résultats montrent que, sous stress acide, une souche clinique de tuberculose sensible aux médicaments peut générer une part notable de bactéries vivantes mais à peine répliquantes, tout en réorganisant à la fois ses protéines internes et celles qu’elle exporte dans son environnement. Il est important de noter que les profils observés dans cet isolat clinique diffèrent de ceux de la souche de laboratoire couramment utilisée, notamment dans les voies traditionnellement associées à la dormance. Pour un public non spécialiste, le message clé est que toutes les bactéries tuberculeuses ne se comportent pas de la même manière : certaines souches cliniques peuvent employer des stratégies alternatives pour se mettre à l’abri et résister à l’attaque antibiotique. Comprendre ces tactiques de survie spécifiques aux souches, et les protéines sécrétées susceptibles d’influencer la réponse immunitaire, pourrait aider à expliquer pourquoi certains patients échouent au traitement et orienter le développement de thérapies plus courtes et plus efficaces ainsi que de meilleurs cibles vaccinales.
Citation: Kriel, N.L., Coetzee, J., Mouton, J.M. et al. Proteomic insights into a M. tuberculosis clinical isolate with an increased propensity to form viable but non-replicating subpopulations during acid stress. Sci Rep 16, 8610 (2026). https://doi.org/10.1038/s41598-026-39941-2
Mots-clés: persistance de la tuberculose, stress acide, cellules viables mais non répliquantes, protéomique, isolats cliniques