Clear Sky Science · fr
La dynamique de l’actine médiée par caldesmon‑1 est essentielle à la différenciation ostéogénique des cellules interstitielles de la valve aortique
Pourquoi le raidissement des valves cardiaques compte
Avec l’âge, l’un des principaux portails du cœur — la valve aortique — peut graduellement se rigidifier et devenir aussi dure que de la pierre. Cette affection, appelée sténose aortique, oblige le cœur à pomper plus fort et peut conduire à une insuffisance cardiaque. Aujourd’hui, les seuls traitements fiables sont le remplacement valvulaire chirurgical ou par cathéter. L’étude résumée ici pose une question fondamentale mais cruciale : qu’est‑ce qui transforme peu à peu le tissu mou et souple de la valve en matière semblable à de l’os ? En mettant au jour un acteur moléculaire clé de ce processus, la recherche ouvre la voie à des médicaments futurs susceptibles de ralentir voire prévenir la calcification valvulaire, au lieu de se contenter de remplacer la valve endommagée.
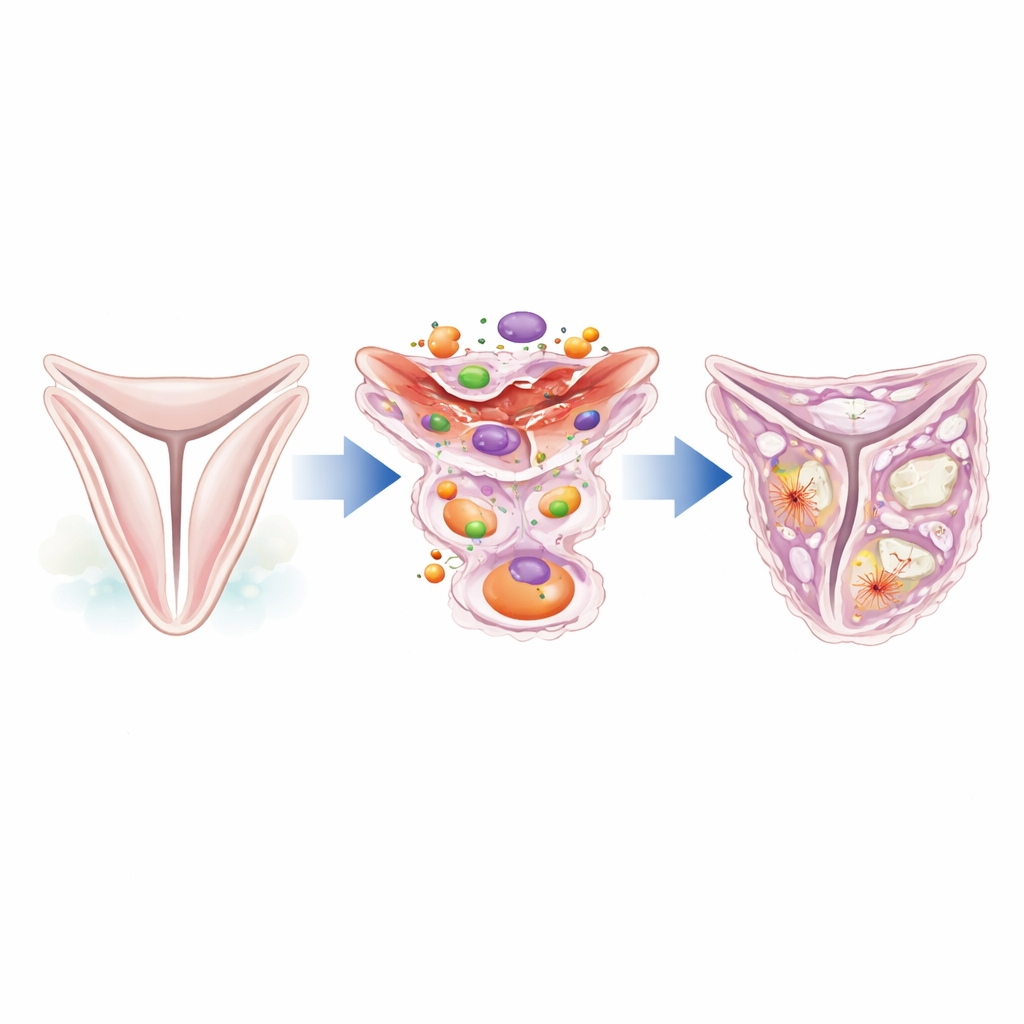
Regard de plus près sur les ouvriers discrets de la valve
Les feuillets de la valve aortique sont soutenus par une fine couche de cellules de soutien spécialisées appelées cellules interstitielles valvulaires. Dans une valve saine, ces cellules demeurent silencieuses et contribuent au maintien de la structure tissulaire. Sous l’effet du stress ou d’une lésion, cependant, elles peuvent changer d’identité et se comporter comme des cellules formatrices de cicatrices ou même comme des cellules productrices d’os. Les auteurs se sont intéressés à une protéine nommée caldesmon‑1, qui aide à contrôler l’armature interne des cellules formée par les filaments d’actine. En exploitant des données existantes de séquençage ARN unicellulaire provenant de valves humaines, ils ont constaté que la caldesmon‑1 est fortement augmentée dans les valves de patients atteints de sténose aortique par rapport aux valves normales, en particulier dans les cellules interstitielles présentes dans des régions épaissies et fibreuses.
Du tissu souple à des zones fibreuses et proches de l’os
Des études au microscope sur des échantillons de valves humaines ont révélé que la protéine caldesmon‑1 est abondante dans les feuillets malades et se retrouve en co‑localisation avec des marqueurs de cellules activées et contractiles ainsi que de cellules de type fibroblastique productrices de collagène. Ces cellules riches en caldesmon‑1 se regroupent autour des zones de fibrose et des premiers signes de calcification, ce qui suggère qu’elles participent à la fabrication de la matrice supplémentaire qui épaissit la valve. Des analyses complémentaires ont montré que ces cellules expriment des gènes typiques de types cellulaires proches du muscle lisse et prédisposés à l’ostéogenèse, et qu’elles sont de grands producteurs de protéines structurales telles que le collagène de type I. En d’autres termes, partout où la valve se raidit et se cicatrise, des cellules interstitielles positives pour la caldesmon‑1 sont présentes sur le terrain.
Comment une protéine qui contrôle la forme pousse les cellules vers l’os
Pour comprendre la relation de cause à effet, l’équipe a isolé des cellules interstitielles valvulaires humaines et utilisé de petits ARN interférents pour réduire l’expression de la caldesmon‑1. Sans cette protéine, les cellules perdaient leur forme allongée et en fuseau pour devenir plus rondes. Leurs filaments d’actine internes s’affinaient, et leur capacité à se diviser et à se déplacer de manière dirigée diminuait. Lorsque les chercheurs ont exposé ces cellules à un milieu de culture ostéogénique, c’est‑à‑dire stimulant la formation osseuse, les cellules normales ont formé facilement des dépôts calciques, tandis que les cellules appauvries en caldesmon‑1 ont montré beaucoup moins d’accumulation minérale. Un séquençage ARN à grande échelle a confirmé que de nombreux gènes impliqués dans la formation osseuse et le remodelage tissulaire, y compris des moteurs ostéogéniques bien connus comme RUNX2 et la phosphatase alcaline, étaient fortement activés par les conditions ostéogéniques mais ne s’élevaient pas lorsque la caldesmon‑1 était réduite.
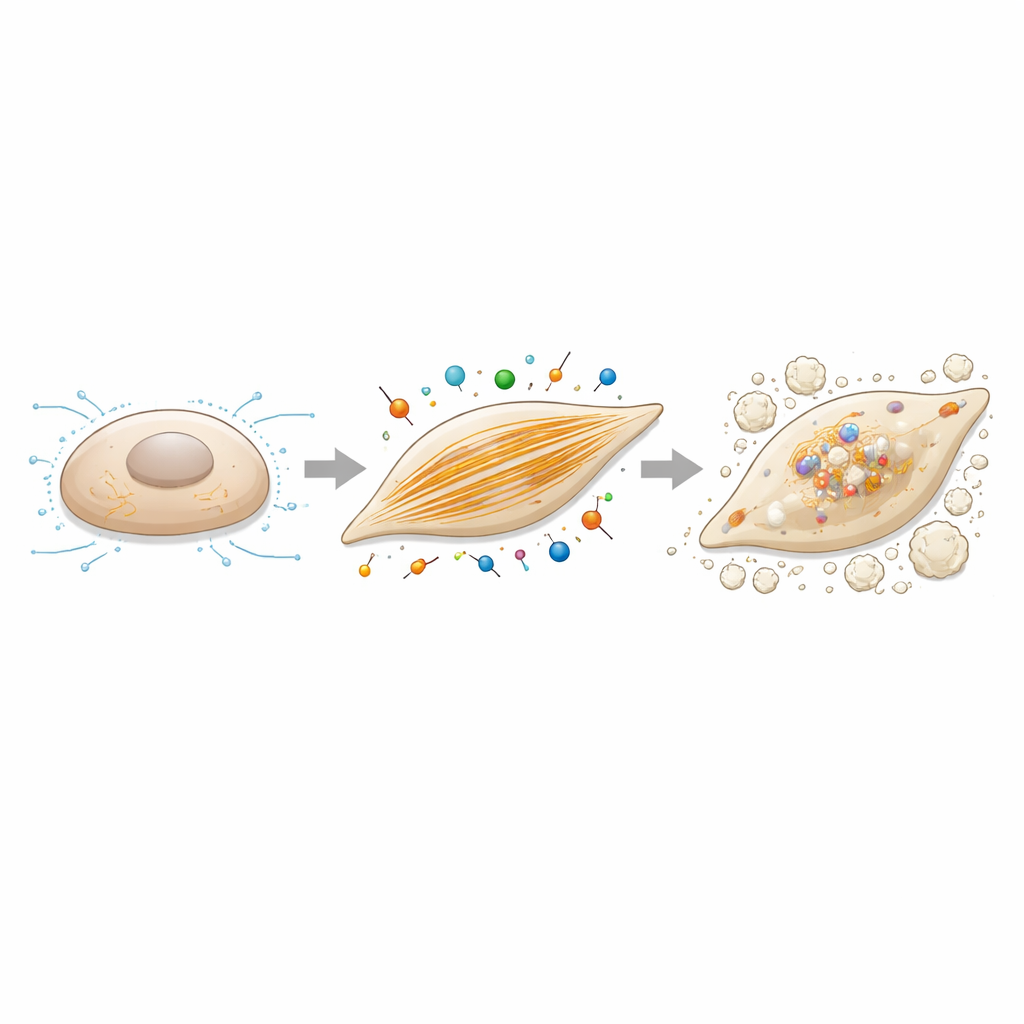
Les filaments d’actine comme levier de contrôle de la calcification
Parce que la caldesmon‑1 régule l’actine, les auteurs ont ensuite étudié si modifier directement l’assemblage de l’actine changerait la tendance des cellules à se calcifier. Ils ont traité des cellules interstitielles valvulaires avec de la cytochalasine B, un composé qui perturbe légèrement la croissance des filaments d’actine, tout en appliquant les mêmes conditions de culture favorisant l’ostéogenèse. À des doses qui ne compromettaient pas gravement la survie cellulaire, ce traitement a fortement réduit le dépôt de calcium et diminué l’expression des gènes associés à l’ossification, y compris caldesmon‑1 et RUNX2. Associées aux expériences d’inhibition, ces observations dressent un tableau cohérent : des réseaux robustes de filaments d’actine et les forces contractiles qu’ils supportent ne sont pas de simples spectateurs — ils pilotent activement le basculement des cellules de soutien silencieuses vers un état producteur d’os dans la valve.
Ce que cela signifie pour les traitements futurs
Pour le grand public, le message principal est que le raidissement de la valve aortique est un processus actif et régulé plutôt qu’une simple usure mécanique. Cette étude identifie la caldesmon‑1 comme un coordinateur central reliant le squelette interne de la cellule au programme génétique de production d’un tissu de type osseux. En aidant les cellules interstitielles valvulaires à acquérir une identité contractile, fibreuse et finalement ostéogénique, la caldesmon‑1 contribue directement à l’accumulation de dépôts durs qui rétrécissent la valve. Bien que toute thérapie ciblant cette protéine ou la dynamique de l’actine nécessitera des tests rigoureux pour éviter des effets indésirables dans d’autres tissus, les voies médiées par la caldesmon‑1 apparaissent désormais comme des candidates prometteuses pour des médicaments destinés à ralentir ou arrêter la calcification valvulaire avant qu’une intervention chirurgicale ne devienne nécessaire.
Citation: Komoda, M., Sakaue, T., Nakao, Y. et al. Caldesmon-1–mediated actin dynamics is essential for osteogenic differentiation of aortic valve interstitial cells. Sci Rep 16, 9385 (2026). https://doi.org/10.1038/s41598-026-39938-x
Mots-clés: calcification de la valve aortique, caldesmon‑1, cellules interstitielles valvulaires, cytosquelette d’actine, différenciation ostéogénique