Clear Sky Science · fr
RBP4 interfère avec la progression du carcinome épidermoïde de la langue en inhibant la voie de signalisation PI3K/AKT et en favorisant la polarisation des macrophages de type M1
Pourquoi le cancer de la langue réclame de nouvelles idées
Le cancer de la langue peut priver les patients de la parole, de la capacité de se nourrir et du goût ; même avec la chirurgie, la chimiothérapie et la radiothérapie, la survie à long terme demeure souvent décevante. Cette étude explore un allié inattendu présent dans le sang, une protéine transporteuse de vitamine A appelée RBP4, et montre comment elle peut à la fois ralentir la croissance des tumeurs de la langue et mobiliser les défenses immunitaires de l’organisme. En révélant comment cette molécule agit à l’intérieur des cellules cancéreuses et au sein des cellules immunitaires environnantes, la recherche ouvre la voie à des stratégies nouvelles susceptibles, un jour, de rendre les traitements plus efficaces et moins délétères.
Une protéine cachée dans les tumeurs de la langue
Les chercheurs ont commencé par analyser de larges bases de données génomiques sur le cancer pour identifier les gènes liés à l’immunité qui pourraient prédire l’évolution des patients atteints d’un carcinome épidermoïde de la langue. Parmi des centaines de candidats, RBP4, une protéine surtout connue pour transporter la vitamine A dans le sang, est apparue comme particulièrement intéressante. En comparant des échantillons tumoraux avec des tissus sains adjacents, l’équipe a constaté que les niveaux de RBP4 étaient systématiquement beaucoup plus faibles dans le cancer. Ce schéma a été confirmé dans plusieurs jeux de données indépendants et sur des prélèvements de 20 patients, ce qui suggère que la perte de RBP4 est une caractéristique commune de cette maladie.
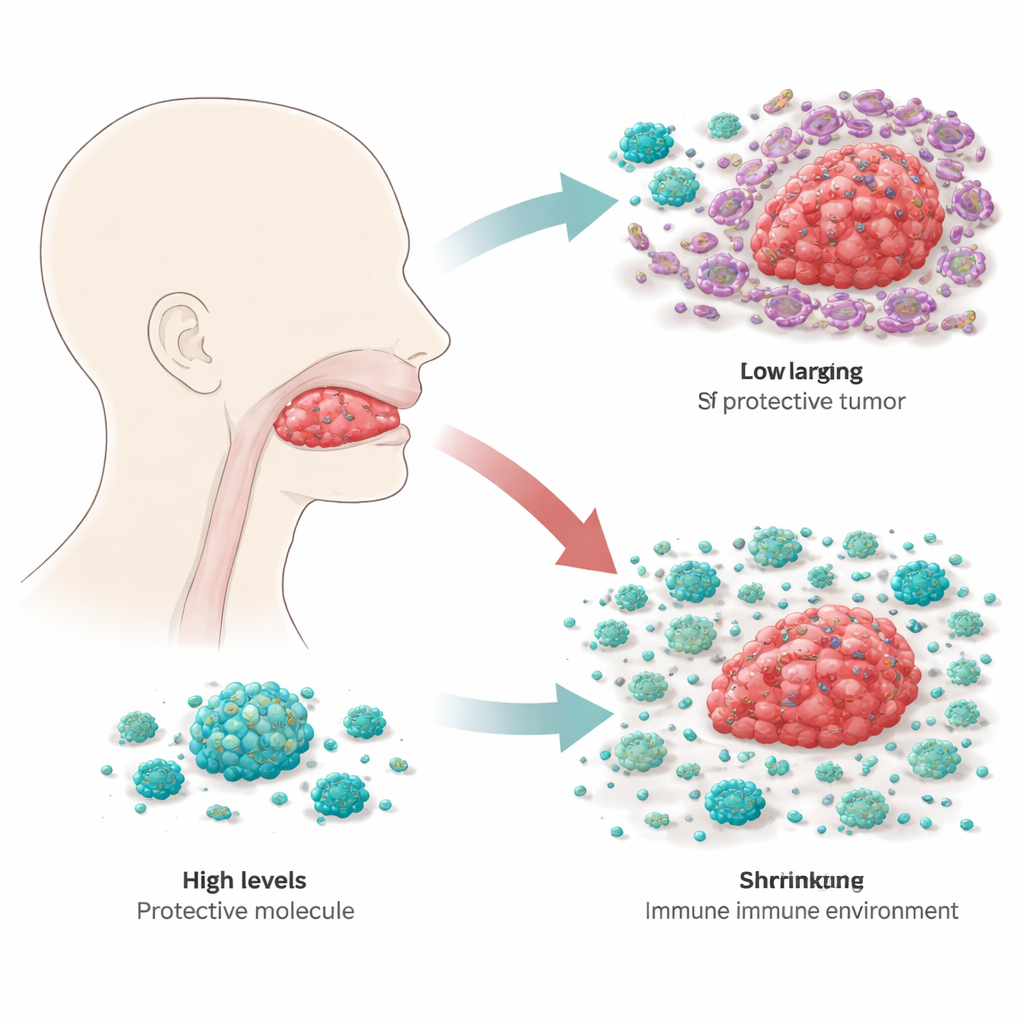
Ralentir la croissance tumorale de l’intérieur
Pour déterminer ce que RBP4 fait réellement dans les cellules cancéreuses de la langue, les scientifiques ont modifié des lignées tumorales pour qu’elles produisent soit un excès de RBP4, soit beaucoup moins. En culture, les cellules exprimant davantage de RBP4 se multipliaient plus lentement, tandis que celles où RBP4 était réduit se divisaient plus rapidement et montraient une meilleure mobilité et capacité d’invasion à travers des membranes artificielles, des comportements liés à la dissémination et à la rechute. Lorsque ces cellules modifiées ont été greffées chez la souris, les tumeurs riches en RBP4 restaient plus petites, alors que les tumeurs déficientes en RBP4 croissaient plus agressivement. En suivant des régulateurs clés de la croissance à l’intérieur des cellules, l’équipe a montré que RBP4 atténue une voie de croissance majeure connue sous le nom de PI3K–AKT–mTOR, que de nombreux cancers utilisent comme accélérateur interne. Lorsque RBP4 est élevé, cette voie est plus calme et les cellules tumorales sont moins aptes à adopter l’état plastique et mobile qui favorise leur migration.
Transformer les cellules immunitaires en combattants tumoraux
Le cancer ne se développe pas isolément ; il vit dans un voisinage de cellules immunitaires, de vaisseaux sanguins et de cellules de soutien appelé microenvironnement tumoral. Parmi elles, les macrophages—gros cellules immunitaires pouvant soit attaquer soit aider les tumeurs—jouent un rôle central. Les investigateurs ont observé que les tumeurs exprimant davantage de RBP4 contenaient également plus de macrophages de type « M1 », associés à l’inflammation et à la destruction tumorale, plutôt que de macrophages de type « M2 », qui favorisent souvent la croissance tumorale. En culture cellulaire, lorsque des macrophages étaient exposés soit à de la RBP4 purifiée soit à des cellules de cancer de la langue modifiées pour sécréter plus de RBP4, ils basculaient vers cet état M1, combattant la tumeur. Lorsque RBP4 était réduit dans les cellules cancéreuses, les macrophages avaient plutôt tendance à évoluer vers un profil plus favorable à la tumeur.
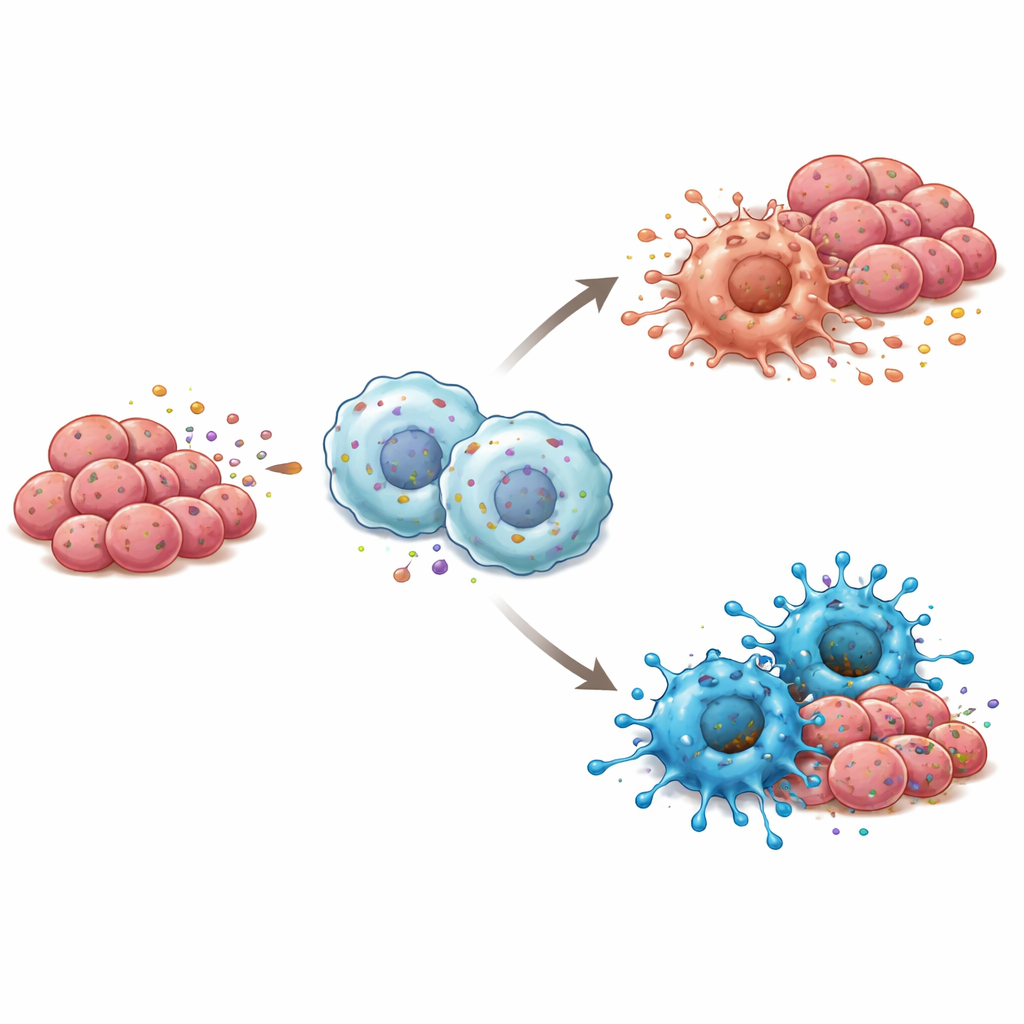
Voies de signalisation à l’origine du basculement immunitaire
Pour comprendre comment RBP4 pousse les macrophages à adopter une posture plus hostile envers les tumeurs, les chercheurs ont examiné quels systèmes d’alerte internes étaient activés dans ces cellules immunitaires. Ils ont découvert que RBP4 stimulait un capteur appelé TLR4 à la surface des macrophages et activait, en aval, NF-κB, un commutateur maître qui déclenche les réponses inflammatoires. Le blocage de TLR4 avec un inhibiteur chimique interrompait cette cascade et empêchait les macrophages d’adopter l’état M1, même en présence de RBP4. Chez la souris, des tumeurs formées à partir de cellules de cancer de la langue riches en RBP4 et mélangées à des macrophages croissaient plus lentement et contenaient davantage de cellules de type M1, avec une activité renforcée de TLR4 et NF-κB, renforçant l’idée que cette voie est centrale pour les effets immunitaires de RBP4.
Ce que cela pourrait signifier pour les soins futurs
Dans l’ensemble, ce travail décrit RBP4 comme un frein à double action sur le cancer de la langue : à l’intérieur des cellules tumorales, il réduit une voie de croissance hyperactive, et dans le voisinage de la tumeur, il aide à convertir les macrophages en défenseurs plus vigilants. Bien que de nombreuses questions demeurent—comme la façon exacte dont RBP4 interagit avec ses cibles et comment l’augmenter en toute sécurité—l’étude suggère que restaurer ou imiter les actions de RBP4 pourrait à la fois ralentir l’expansion tumorale et renforcer la pression immunitaire de l’organisme sur le cancer. Pour les patients, cela ouvre la perspective de thérapies futures qui ne se contentent pas d’enlever les tumeurs, mais qui reconfigurent aussi leur câblage interne et leur « écosystème » local pour limiter les récidives.
Citation: Yan, Y., Miao, N. & Wang, X. RBP4 interferes with tongue squamous cell carcinoma progression by inhibiting the PI3K/AKT signaling pathway and promoting macrophage M1-type polarization. Sci Rep 16, 9375 (2026). https://doi.org/10.1038/s41598-026-39915-4
Mots-clés: cancer de la langue, RBP4, microenvironnement tumoral, macrophages, voie PI3K AKT