Clear Sky Science · fr
Un cadre intelligent de santé pour le diagnostic du carcinome hépatocellulaire basé sur des apprenants agrégés à partir de données biomédicales utilisant l’intelligence artificielle explicable
Pourquoi des dépistages du foie plus intelligents sont importants
Le cancer du foie, en particulier une forme fréquente appelée carcinome hépatocellulaire, se développe souvent silencieusement jusqu’à devenir difficile à traiter. Les médecins recueillent déjà une grande quantité de résultats d’examens de routine chez les patients, mais transformer tous ces chiffres en un signal d’alerte précoce est complexe. Cette étude examine comment des programmes informatiques avancés peuvent trier les données médicales quotidiennes pour repérer les patients à haut risque, tout en expliquant leur raisonnement de manière compréhensible et fiable pour les cliniciens.
Transformer les tests de routine en alertes précoces
Les chercheurs se concentrent sur des patients présentant des affections chroniques du foie, qui courent un risque plus élevé de développer un cancer hépatique grave. Plutôt que de s’appuyer sur des examens coûteux ou des tests génétiques complexes, ils utilisent des mesures cliniques standard — comme la biochimie sanguine, les enzymes hépatiques et des informations de santé de base. Ces mesures sont d’abord soigneusement re‑échelonnées afin que toutes les caractéristiques se trouvent dans la même plage numérique. Cette étape simple mais cruciale de nettoyage aide les modèles informatiques à apprendre des motifs de façon plus fiable et évite qu’une valeur exceptionnellement élevée n’écrase les prédictions.
De nombreuses « secondes opinions » numériques travaillant ensemble
Plutôt que de dépendre d’un seul algorithme, l’équipe construit un ensemble, ou une équipe, de trois modèles d’apprentissage profond différents. Un modèle compresse les données pour découvrir les combinaisons de caractéristiques les plus informatives. Un second modèle est conçu pour reconnaître des motifs qui se déroulent comme des séquences, capturant comment plusieurs mesures ensemble peuvent suggérer un risque. Un troisième modèle empile plusieurs couches simples pour saisir des relations complexes et non linéaires cachées dans les données. Chaque modèle rend son propre jugement quant à l’appartenance d’un patient au groupe à haut risque ou à faible risque, et un combineur de niveau supérieur pèse et fusionne ces avis en une décision finale.
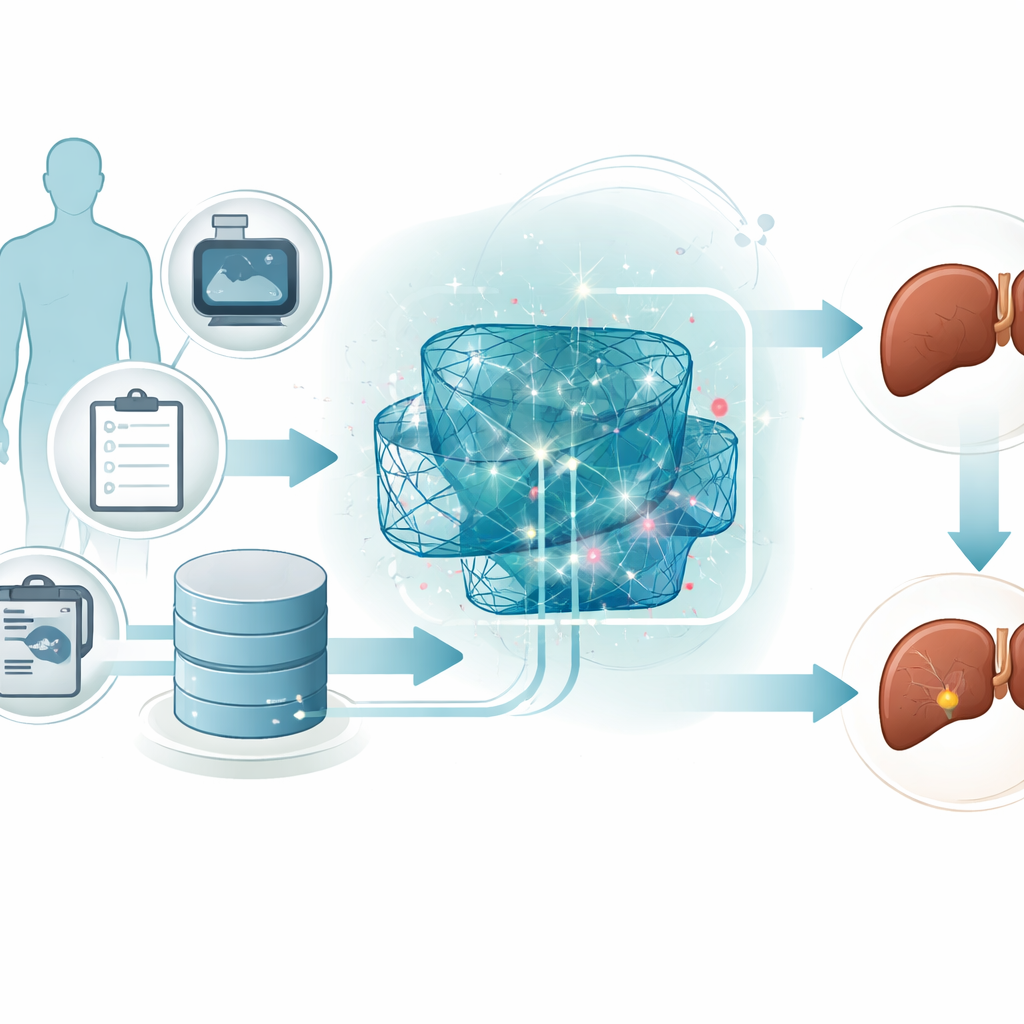
Ouvrir la boîte noire pour les médecins
Aussi puissants soient-ils, les systèmes d’apprentissage profond sont souvent critiqués pour fonctionner comme des « boîtes noires » mystérieuses. Pour y remédier, les auteurs ajoutent une couche d’intelligence artificielle explicable basée sur une méthode connue sous le nom de SHAP. Cette technique estime dans quelle mesure chaque variable d’entrée pousse une prédiction individuelle vers un résultat plus sûr ou plus risqué. Par exemple, certains niveaux d’enzymes hépatiques, des marqueurs de la fonction hépatique et des signes d’extension en dehors du foie ressortent comme particulièrement influents. Les médecins peuvent voir non seulement que le système signale un patient comme à haut risque, mais aussi quelles mesures spécifiques ont motivé cette décision et dans quelle direction, créant un partenariat plus transparent entre clinicien et machine.
Quelle est l’efficacité de l’approche ?
L’équipe teste son cadre sur un jeu de données public de 165 patients suivis pendant au moins un an, chacun étiqueté comme survivant ou non survivant. Malgré la taille modeste du jeu de données, le modèle combiné apprend à séparer les patients à haut risque de ceux à faible risque avec une précision remarquable : il classifie correctement environ 98 cas sur 100 lors des dernières phases d’entraînement. Comparée à une gamme de méthodes existantes — incluant des modèles statistiques classiques et plusieurs réseaux neuronaux modernes — cette approche non seulement atteint ou dépasse leurs performances en termes de précision, sensibilité et équilibre entre faux négatifs et faux positifs, mais le fait aussi avec un temps de calcul relativement faible. Une étude d’ablation, où les trois modèles composantes sont testés individuellement, montre que chacun apporte une valeur ajoutée, mais que leur combinaison donne les meilleurs résultats.
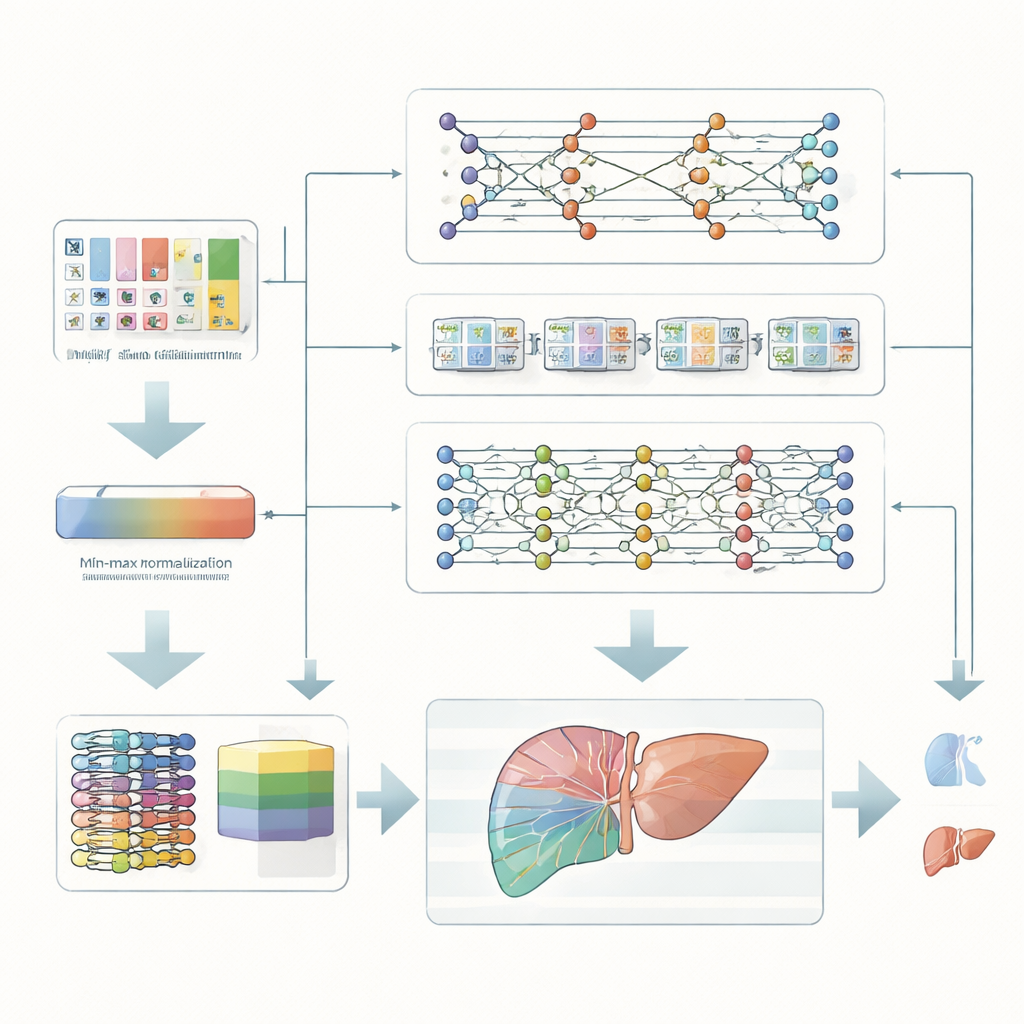
Ce que cela pourrait signifier pour les soins aux patients
Pour la pratique médicale quotidienne, ce travail ouvre la voie à des outils d’aide à la décision à la fois performants et compréhensibles. Un système construit selon ces principes pourrait aider à repérer des patients hépatiques qui dérivent silencieusement vers une zone de danger bien avant l’apparition des symptômes, en utilisant des données déjà collectées dans de nombreuses cliniques. Parallèlement, ses explications — mettant en avant les résultats d’examens et les signes cliniques les plus pertinents pour une personne donnée — pourraient aider les médecins à affiner les plans de traitement et à discuter des risques avec les patients. Bien que l’étude repose encore sur un jeu de données relativement petit et d’une seule source et n’intègre pas d’imagerie ni de données génétiques, elle propose une feuille de route pour des modèles de risque de cancer plus intelligents et transparents qui, avec des données plus larges et plus diversifiées, pourraient un jour devenir des alliés de routine dans la lutte contre le cancer du foie.
Citation: Alqaralleh, B.A.Y., Alksasbeh, M.Z., Kulakli, A. et al. An intelligent healthcare framework for hepatocellular carcinoma diagnosis based on aggregated learners from biomedical data utilising explainable artificial intelligence. Sci Rep 16, 9357 (2026). https://doi.org/10.1038/s41598-026-39871-z
Mots-clés: cancer du foie, IA médicale, diagnostic précoce, IA explicable, support à la décision clinique