Clear Sky Science · fr
Cadre intégratif transcriptomique et apprentissage automatique révélant des gènes candidats et des mécanismes potentiels de l’exposition à l’aflatoxine B1 dans le cancer du sein
Pourquoi un champignon alimentaire importe pour la santé mammaire
L’aflatoxine B1 est une toxine produite par certains champignons qui peuvent se développer sur des aliments courants comme le maïs et les arachides, en particulier dans les régions chaudes et humides. Elle est bien connue pour endommager le foie, mais les scientifiques s’inquiètent de plus en plus qu’elle puisse aussi influencer le cancer du sein. Cette étude pose une question simple mais cruciale : si des femmes ingèrent régulièrement de faibles quantités de cette toxine, cela pourrait-il modifier subtilement leur tissu mammaire de manière à augmenter le risque de cancer — et pouvons-nous détecter ces changements tôt grâce aux outils modernes de génétique et de science des données ?
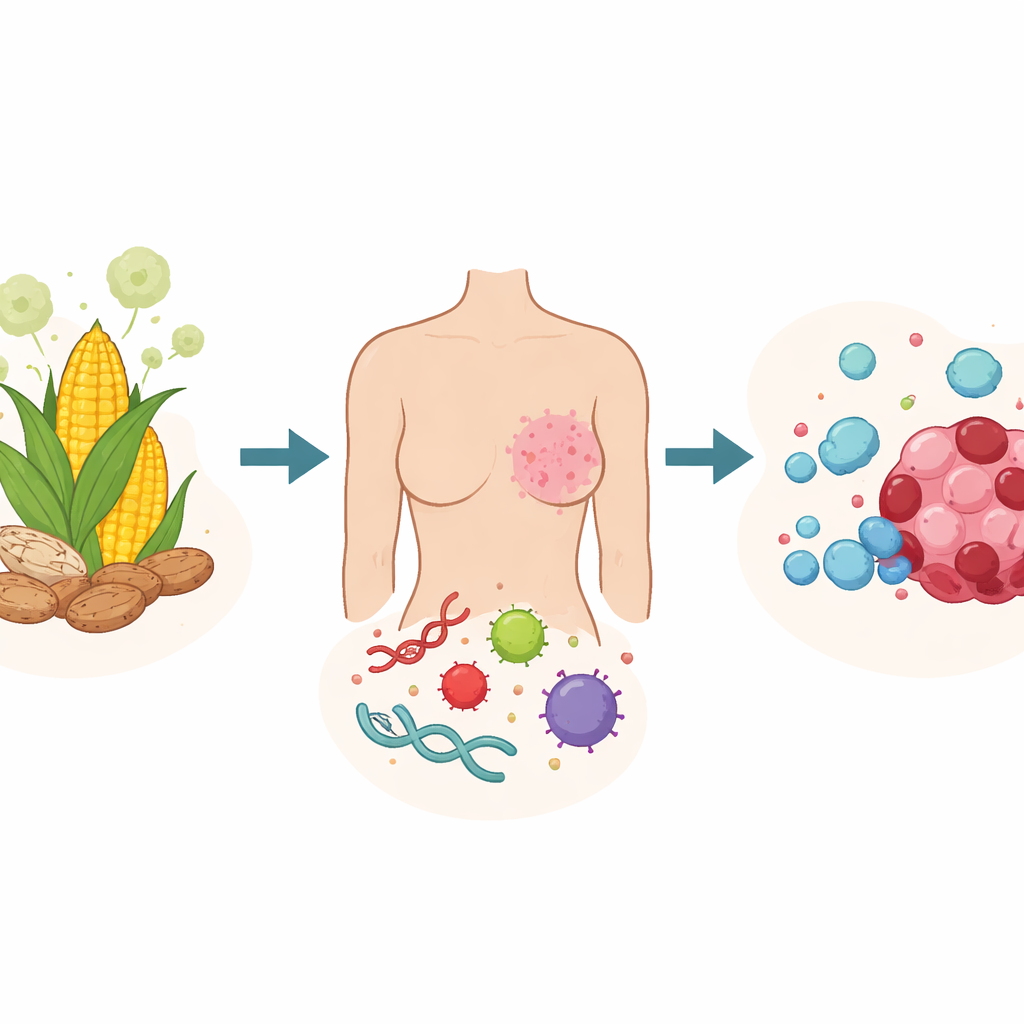
Relier une toxine cachée aux tumeurs mammaires
Les chercheurs ont commencé par rassembler une vaste collection de données génétiques existantes provenant de tumeurs du sein et de tissu mammaire sain. Ils ont combiné plusieurs jeux de données publics et corrigé soigneusement les différences techniques afin que tous les échantillons puissent être comparés équitablement. En parallèle, ils ont utilisé des bases de données chimiques pour prédire avec quels protéines humaines l’aflatoxine B1 est la plus susceptible d’interagir. En recoupant les cibles prédites de la toxine avec les gènes qui se comportent différemment dans le cancer du sein, ils ont réduit des milliers de possibilités à une petite liste de gènes situés au point de jonction entre l’exposition à l’aflatoxine et la biologie tumorale.
Identification d’un panel d’alerte à sept gènes
Pour transformer cette connaissance biologique en outil clinique, l’équipe a appliqué un large éventail de méthodes d’apprentissage automatique. Ces algorithmes ont filtré les gènes d’intersection pour déterminer quelle combinaison sépare le mieux les échantillons cancéreux des tissus mammaires non cancéreux. Après avoir testé 127 variantes de modèles, ils sont arrivés à un panel épuré de sept gènes. Ensemble, ces gènes ont permis à leur meilleur modèle de distinguer le cancer du non‑cancer avec une précision extrêmement élevée. Certains gènes, comme EGFR et MET, sont des acteurs bien connus de la croissance tumorale, tandis que d’autres — tels que PPARG, MME, NQO2 et NR3C2 — sont davantage liés à l’équilibre hormonal, à la détoxification et à l’inflammation.
Comment le système immunitaire et l’agencement tissulaire interviennent
Au‑delà de simples interrupteurs marche/arrêt, l’étude explore comment ces gènes façonnent l’environnement immunitaire local du tissu mammaire. À l’aide d’outils computationnels estimant quelles cellules immunitaires sont présentes dans des échantillons de tissu en vrac, les auteurs ont constaté que certaines cellules immunitaires de soutien, en particulier un type de macrophage activé, ont tendance à être plus abondantes dans les tumeurs. Certains des sept gènes, notamment MME et NR3C2, étaient systématiquement associés à des niveaux plus faibles de ces cellules inflammatoires, ce qui suggère que lorsque ces gènes protecteurs sont sous‑exprimés, le microenvironnement immunitaire tumoral peut devenir plus permissif à la progression cancéreuse. Les technologies d’ARN unicellulaire et spatiales ont ensuite apporté une cartographie microscopique, montrant où et dans quels types cellulaires chaque gène est exprimé dans de véritables sections tumorales.
Zoom sur les cellules, une par une
En examinant des milliers de cellules individuelles provenant de différents sous‑types de cancer du sein — tels que les tumeurs hormonosensibles, HER2‑positives et triple‑négatives — les chercheurs ont pu suivre comment l’activité génique évolue le long d’une sorte de « chronologie » approximative de la progression tumorale. Plusieurs des gènes protecteurs étaient les plus actifs dans des états cellulaires précoces et s’estompaient à mesure que les cellules évoluaient vers des profils plus agressifs. Un gène, MIF, a montré le schéma inverse, devenant plus proéminent dans les macrophages et les cellules tumorales de zones riches en activité immune, cohérent avec un rôle dans la promotion de l’inflammation et l’évasion immunitaire. Ces motifs se reflétaient dans les cartes spatiales de coupes tumorales, où la forte expression de certains gènes se regroupait dans des zones riches en tumeurs ou riches en cellules immunitaires, mettant en lumière un dialogue complexe entre cellules cancéreuses, cellules immunitaires et leur microenvironnement.
Ce que cela signifie pour les patientes et la sécurité alimentaire
En termes simples, ce travail suggère que l’aflatoxine B1 pourrait pousser le tissu mammaire vers un état plus favorable au cancer en perturbant un petit groupe influent de gènes qui contrôlent les signaux de croissance, la détoxification et le climat immunitaire local. Les mêmes sept gènes qui marquent cette perturbation forment également une signature diagnostique puissante qui, après des tests complémentaires sur des cohortes plus larges et plus diversifiées, pourrait aider les médecins à détecter le cancer du sein plus tôt et à mieux comprendre le risque individuel. Bien que l’étude ne prouve pas que l’exposition quotidienne à l’aflatoxine cause directement le cancer du sein, elle renforce l’argument en faveur d’un contrôle plus strict de la contamination alimentaire et offre une nouvelle boîte à outils génétique pour étudier comment les polluants environnementaux modulent discrètement le risque de cancer.
Citation: Wang, W., Liu, M. & Li, X. Integrative transcriptomic and machine learning framework reveals candidate genes and potential mechanisms of aflatoxin B1 exposure in breast cancer. Sci Rep 16, 8818 (2026). https://doi.org/10.1038/s41598-026-39844-2
Mots-clés: aflatoxine B1, cancer du sein, agents cancérigènes environnementaux, multi-omiques, biomarqueurs du cancer