Clear Sky Science · fr
Identification multi-omique des cibles clés pour la différenciation ostéogénique des cellules stromales mésenchymateuses de la moelle osseuse humaine sous stress oxydatif
Pourquoi des os exposés au stress comptent
En vieillissant ou en développant des maladies chroniques comme le diabète et l’ostéoporose, nos os perdent leur capacité à se réparer. Un coupable majeur est le « stress oxydatif » : une accumulation de molécules réactives qui endommagent les cellules. Cette étude pose une question pratique aux implications considérables pour les fractures et les implants osseux : qu’est‑ce qui dysfonctionne précisément à l’intérieur des cellules souches de la moelle osseuse humaine exposées au stress oxydatif, et peut‑on identifier un interrupteur moléculaire qui leur permettrait de conserver leur capacité à former du nouvel os ?
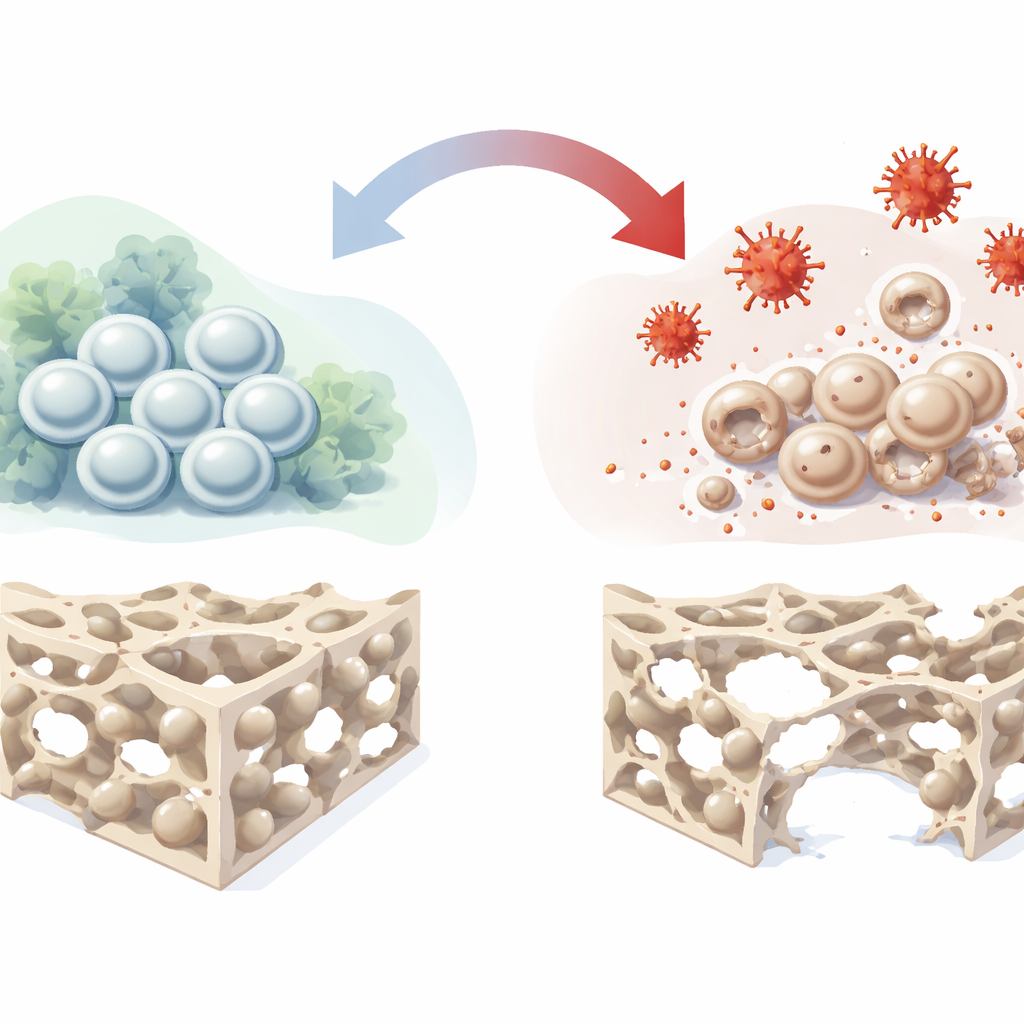
Les cellules souches qui fabriquent l’os
Au cœur de nos os résident des cellules stromales mésenchymateuses de la moelle osseuse, une population polyvalente capable de s’auto‑renouveler et de mûrir en ostéoblastes (cellules formant l’os), en chondrocytes (cellules cartilagineuses) ou en adipocytes (cellules graisseuses). Parce qu’elles contribuent naturellement à la réparation des tissus endommagés, elles sont un candidat majeur pour les thérapies de nouvelle génération visant à réparer les défauts osseux et l’ostéonécrose. Cependant, chez les patients réels, ces cellules se trouvent souvent dans des environnements hostiles marqués par une mauvaise vascularisation, un faible apport en oxygène, une inflammation et un stress oxydatif. Dans de telles conditions, leur capacité à se différencier en cellules osseuses s’affaiblit, limitant le succès des thérapies à base de cellules souches. Les auteurs ont cherché à recréer ce milieu hostile en laboratoire et à cartographier, en détail, la manière dont il perturbe la formation osseuse.
Recréer un environnement agressif en laboratoire
Les chercheurs ont utilisé le peroxyde d’hydrogène, une source courante d’espèces réactives de l’oxygène, pour imposer un stress oxydatif aux cellules souches de la moelle osseuse humaine cultivées in vitro. Ils ont titré la dose avec soin pour trouver un point d’équilibre où les cellules étaient stressées sans être tuées. À 400 micromoles par litre ou en dessous, les cellules conservaient leur morphologie fusiforme habituelle et restaient viables, bien que leur chimie interne ait clairement changé : les niveaux d’espèces réactives ont augmenté, la fonction mitochondriale a commencé à se modifier et l’équilibre entre protéines liées à la survie et à la mort a basculé vers l’adaptation au stress. À des doses plus élevées, les cellules perdaient leur architecture et mouraient en grand nombre. En utilisant la dose bien tolérée de 400 micromoles, l’équipe a ensuite déclenché la différenciation ostéogénique et observé ce qui se passait.
Comment le stress bloque la construction osseuse
Sous stress oxydatif, la capacité des cellules souches à devenir des ostéoblastes a diminué selon plusieurs tests complémentaires. L’activité ostéo‑précoce, suivie par l’enzyme phosphatase alcaline, a chuté à mesure que le stress augmentait. Plus tard, lorsque les cellules auraient dû déposer des minéraux, les plaques de culture montraient moins de nodules calciques et de moindre intensité. Des gènes et protéines clés liés à l’os, tels que RUNX2 et l’ostéopontine, étaient également réprimés. Pour examiner les mécanismes sous‑jacents, les scientifiques ont combiné deux approches « omiques » puissantes : le séquençage de l’ARN pour profiler les gènes dont l’activité variait, et une analyse protéomique à grande échelle pour voir quelles protéines changeaient réellement en abondance. Ces jeux de données ont révélé des centaines de modifications touchant le contrôle du cycle cellulaire, le comportement des chromosomes, le métabolisme et l’organisation de l’architecture extracellulaire, dessinant le tableau de cellules souches dont le rythme interne et le soutien structurel sont perturbés par le stress oxydatif.
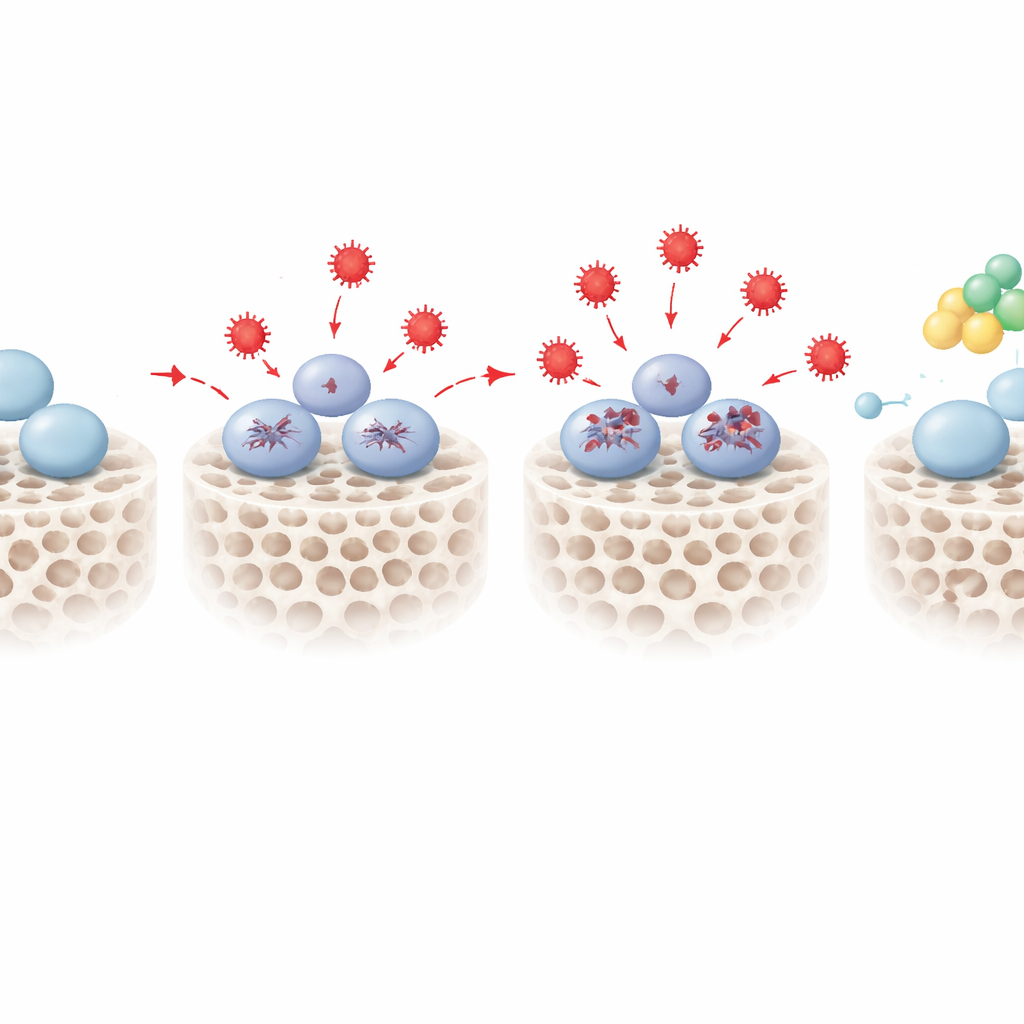
Découverte d’un commutateur protecteur nommé PENK
En superposant les cartes d’ARN et de protéines, l’équipe a réduit sa liste à 18 molécules qui changeaient de façon cohérente dans les cellules stressées et étaient liées à la fois aux réponses au stress et à la formation osseuse. Une molécule s’est distinguée : la proenképhaline, ou PENK, surtout connue comme précurseur de peptides opioïdes endogènes. Sous stress oxydatif, les niveaux de PENK augmentaient de manière dépendante de la dose. Lorsque les scientifiques ont diminué artificiellement l’expression de PENK par des outils génétiques, les cellules souches stressées ont vu leur capacité ostéogénique s’aggraver, avec une activité enzymatique précoce plus faible et moins de dépôt minéral. Lorsqu’ils ont surexprimé PENK, l’effet inverse est apparu : même dans les mêmes conditions oxydatives, les cellules ont récupéré une grande partie de leur capacité à former une matrice osseuse minéralisée. Des analyses de voies supplémentaires suggèrent que PENK pourrait agir en modulant certaines voies métaboliques, notamment le métabolisme des sphingolipides, qui relient l’équilibre redox aux décisions quant au maintien du potentiel des cellules souches ou à leur engagement vers une destinée osseuse.
Ce que cela signifie pour la réparation osseuse future
Cette étude montre que le stress oxydatif seul suffit à diminuer fortement la capacité des cellules stromales mésenchymateuses de la moelle osseuse humaine à former de l’os, et identifie PENK comme un facteur protecteur intrinsèque aidant ces cellules à résister à ce dommage. Pour un public non spécialiste, le message est clair : le succès des thérapies osseuses basées sur des cellules souches dépendra non seulement des cellules elles‑mêmes, mais aussi des milieux stressants dans lesquels on les implante et des interrupteurs moléculaires qui les aident à faire face. En mettant en lumière PENK comme cible prometteuse, ce travail oriente vers de futurs médicaments ou approches géniques susceptibles de renforcer la réparation osseuse chez des patients dont les tissus sont baignés de stress oxydatif, des personnes âgées à celles vivant avec des maladies métaboliques ou inflammatoires chroniques.
Citation: Dong, W., Zheng, Y., Zhou, Y. et al. Multi-omics identification of key targets for the osteogenic differentiation of human bone marrow mesenchymal stromal cells under oxidative stress. Sci Rep 16, 8215 (2026). https://doi.org/10.1038/s41598-026-39818-4
Mots-clés: régénération osseuse, stress oxydatif, cellules souches mésenchymateuses, différenciation ostéogénique, PENK