Clear Sky Science · fr
Biomarqueurs candidats pour identifier les patients atteints de mésothéliome à risque de thromboembolie veineuse après chirurgie
Pourquoi cette recherche importe pour les patients et leurs familles
Les personnes atteintes de mésothéliome pleural, un cancer de la membrane entourant les poumons, font souvent face à un danger caché après une intervention chirurgicale : des caillots sanguins graves dans les jambes ou les poumons. Ces caillots, appelés médicalement thromboembolie veineuse, peuvent être mortels dans les semaines qui suivent une opération. Aujourd’hui, les médecins disposent seulement d’outils approximatifs pour prédire qui présente le plus de risque. Cette étude constitue un premier pas important vers un simple test sanguin capable de repérer les patients vulnérables avant la chirurgie, afin que les équipes soignantes puissent les protéger par une surveillance renforcée et des traitements ciblés.
Une menace silencieuse après une chirurgie salvatrice
Aux États-Unis, quelques milliers de personnes sont diagnostiquées chaque année d’un mésothéliome pleural, et pour certains, une intervention majeure visant à retirer les tumeurs offre la meilleure chance de survie prolongée. Pourtant, jusqu’à environ un patient sur dix peut décéder dans le mois suivant la chirurgie, souvent à cause de caillots qui se forment dans les veines profondes et peuvent migrer vers les poumons. Les tests de laboratoire standard et les indicateurs de base, comme le nombre de plaquettes ou un test de coagulation couramment utilisé appelé D-dimères, ne sont pas assez spécifiques pour identifier quels patients atteints de mésothéliome développeront effectivement des caillots. En conséquence, de nombreux patients reçoivent le même traitement préventif, alors qu’une fraction seulement est réellement à haut risque. Un prédicteur plus précis pourrait aider les médecins à adapter les soins et à éviter à la fois les caillots dangereux et les traitements inutiles.
À la recherche de signaux d’alerte dans les protéines sanguines
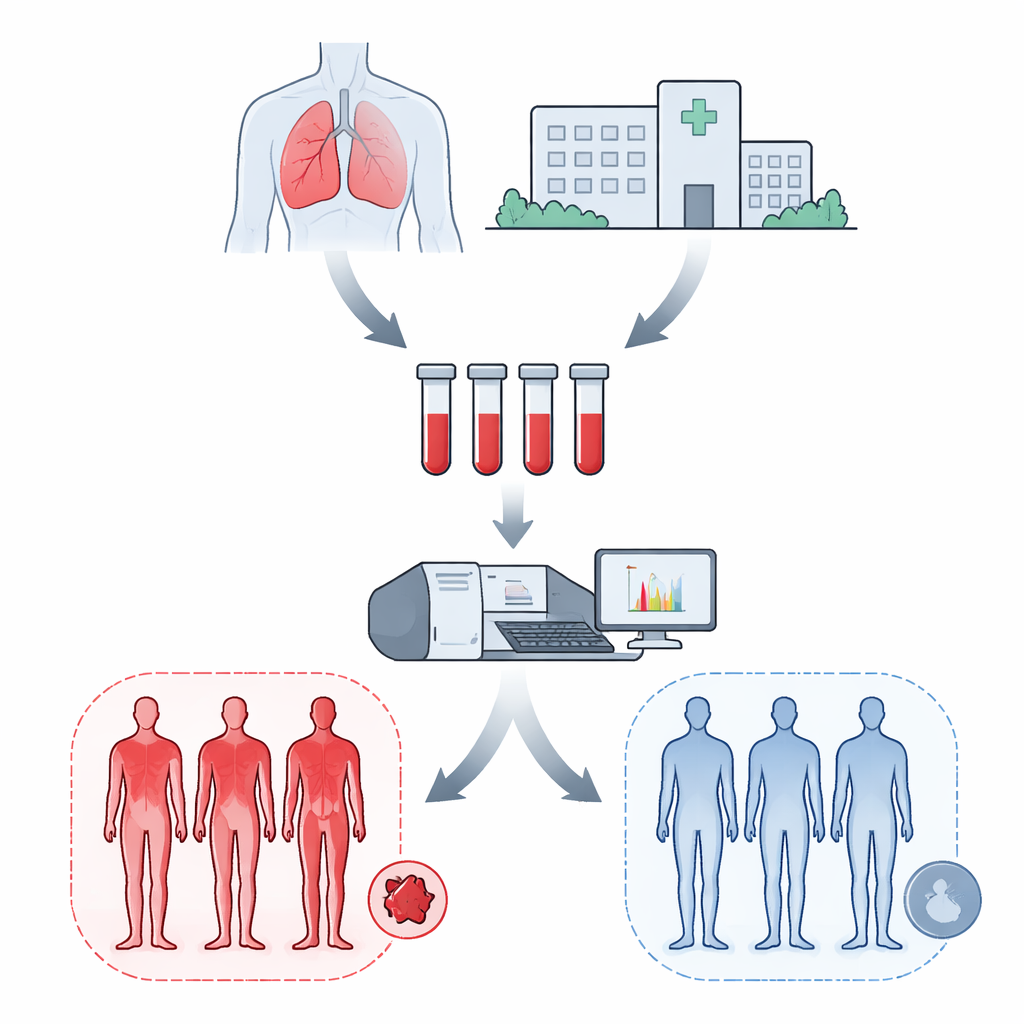
Les chercheurs se sont concentrés sur les protéines circulant dans le sang susceptibles d’évoluer de manière subtile mais révélatrice avant l’apparition des caillots. Ils ont étudié des échantillons de plasma sanguin provenant de seulement 18 personnes : six patients atteints de mésothéliome qui ont ensuite développé des caillots après la chirurgie, six patients mésothéliaux qui n’en ont pas développé, et six patients atteints de cancer du poumon qui n’ont pas non plus présenté de caillots. Tous les prélèvements ont été effectués avant la chirurgie, donc avant tout symptôme ou traitement lié aux caillots. Grâce à la spectrométrie de masse avancée, une technique capable de trier et de mesurer des milliers de protéines simultanément, l’équipe a établi un cliché détaillé des protéines plus ou moins abondantes dans chaque groupe de patients. Un pipeline d’analyse personnalisé nommé WASP les a aidés à nettoyer, normaliser et comparer ces profils protéiques complexes, malgré le faible nombre de sujets.
Restreindre les indices les plus prometteurs
Parmi près de 600 protéines détectées, les investigateurs ont comparé trois regroupements clés : les patients mésothéliaux qui ont développé des caillots et ceux qui n’en ont pas développé, ainsi que ces deux groupes comparés aux patients atteints de cancer du poumon sans caillots. En recoupant soigneusement ces comparaisons, ils ont identifié une liste restreinte de 33 protéines présentes uniquement chez les patients ayant développé des caillots et absentes dans les deux groupes témoins. Ils ont ensuite appliqué une seconde couche d’analyse, posant trois questions pour chaque candidat : ces protéines interagissent-elles entre elles au sein de réseaux biologiques connus ? Sont-elles impliquées dans des voies liées à la coagulation et à l’inflammation ? Et leurs niveaux sont-ils influencés par le stade du mésothéliome, ou restent-ils relativement stables selon l’avancement du cancer ?
Relier les réseaux protéiques au risque de coagulation
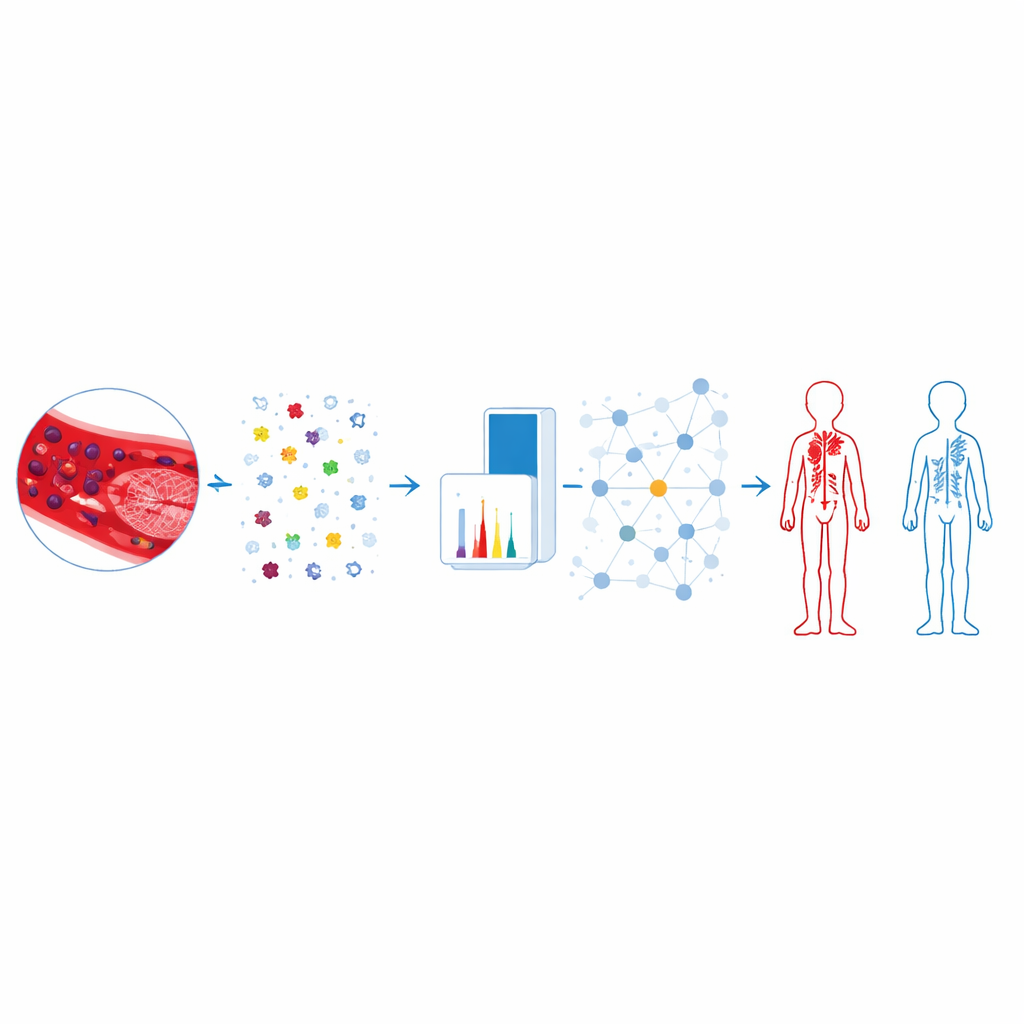
La cartographie des 33 protéines sur des réseaux d’interaction connus a révélé plusieurs grappes fortement connectées. Une grappe en particulier contenait des protéines liées aux systèmes du complément et de la coagulation — deux cascades imbriquées qui régulent à la fois les réponses immunitaires et la formation de caillots. Au sein de ce groupe, l’équipe a mis en avant des protéines telles que CFHR2, CFHR5, KNG1 et F12, qui se situent en amont de ces voies et ont déjà été associées au risque de coagulation dans d’autres études. Fait important, plusieurs de ces candidats variaient peu selon le stade du cancer dans de larges bases de données publiques, ce qui suggère que les modifications de leurs niveaux sanguins pourraient être davantage liées au risque de caillot qu’à la seule charge tumorale. D’autres candidats étaient associés à l’activité plaquettaire et au métabolisme, laissant entrevoir des mécanismes supplémentaires par lesquels des caillots pourraient se former chez ces patients.
Ce que cela signifie pour les soins futurs
Ce travail n’aboutit pas encore à un test clinique prêt à l’emploi, et les auteurs soulignent plusieurs limites, notamment le petit nombre de patients et l’absence de comparaison directe avec des outils existants comme le D-dimère sur des cohorts plus larges. Cependant, l’étude illustre une stratégie rigoureuse pour extraire des signaux pertinents à partir d’échantillons rares et difficiles à obtenir, et elle fournit une liste ciblée de candidats protéiques qui peuvent désormais être testés dans des cohortes plus larges et plus diverses. Si des études ultérieures confirment que certaines de ces protéines signalent de façon fiable les patients mésothéliaux à haut risque de caillots dangereux, les médecins pourraient utiliser un simple prélèvement sanguin préopératoire pour personnaliser la prévention : renforcer la surveillance et les traitements protecteurs pour ceux qui présentent le plus grand risque, tout en épargnant aux autres des procédures et médicaments supplémentaires dont ils n’ont peut-être pas besoin.
Citation: Shami-shah, A., Roth, S., Morton, S.R. et al. Candidate biomarkers to identify mesothelioma patients at risk of developing venous thromboembolism post-surgery. Sci Rep 16, 9313 (2026). https://doi.org/10.1038/s41598-026-39805-9
Mots-clés: mésothéliome pleural, thromboembolie veineuse, biomarqueurs sanguins, complications postopératoires