Clear Sky Science · fr
Conception, par vaccinologie inverse, d’un vaccin multépitope universel contre le virus chikungunya : approches phylogénétiques et immunoinformatiques
Pourquoi une nouvelle approche vaccinale compte
Le chikungunya est un virus transmis par les moustiques qui peut transformer une fièvre brève en des douleurs articulaires durant des mois, voire des années, privant des personnes de travail et mettant à rude épreuve les systèmes de santé dans les régions tropicales et subtropicales. Les vaccins existants sont prometteurs mais ont soulevé des inquiétudes de sécurité dans certains groupes et ne couvrent peut‑être pas toutes les variantes du virus circulant dans le monde. Cette étude explore un vaccin de nouvelle génération conçu par ordinateur qui vise à être plus sûr, plus largement protecteur et plus simple à produire, offrant un aperçu de la manière dont les outils numériques peuvent remodeler nos défenses contre des virus à évolution rapide.
Comprendre la menace transmise par les moustiques
Le virus chikungunya s’est largement répandu en Amérique, en Afrique et en Asie, provoquant des centaines de milliers de cas et des décès, en particulier lors d’épidémies. Au‑delà de la fièvre et de l’éruption initiales, de nombreux patients souffrent de problèmes articulaires persistants qui réduisent la qualité de vie et augmentent les coûts économiques. Le virus existe sous trois grandes lignées génétiques présentes dans différentes régions du globe. Parce qu’il mute au fil du temps, un vaccin protégeant une seule souche locale peut ne pas être efficace partout. Par ailleurs, l’un des vaccins vivants récemment autorisés a été suspendu dans certains pays après des problèmes de sécurité chez les personnes âgées, soulignant le besoin d’approches alternatives.
Établir une carte cible universelle
Plutôt que de cultiver le virus entier en laboratoire, les chercheurs se sont tournés vers des bases de données mondiales de séquences virales et des outils bioinformatiques puissants. À partir de près de 2 800 génomes de chikungunya, l’équipe a filtré plus de 1 400 séquences de haute qualité et construit un arbre phylogénétique détaillé montrant les relations entre les trois principales lignées. Ils ont ensuite créé une version « consensus » des protéines structurelles du virus — les parties situées à la surface virale et les plus visibles par le système immunitaire. En comparant des milliers de séquences, ils ont repéré des régions protéiques qui restent très similaires entre les lignées, même lorsque d’autres parties mutent. Ces régions conservées sont des cibles idéales parce qu’un vaccin fondé sur elles devrait rester efficace quand le virus évolue.
Concevoir un vaccin à plusieurs éléments
À partir des protéines conservées, l’étude a utilisé des outils en ligne spécialisés pour prédire de courts segments — appelés épitopes — que le système immunitaire humain est le plus susceptible de reconnaître. Certains de ces segments devraient déclencher la production d’anticorps par les cellules B, tandis que d’autres activent des lymphocytes T cytotoxiques et auxiliaires. Après sélection des candidats pour la puissance de réponse, l’absence de toxicité et le faible risque d’allergie, le design final comprenait 10 épitopes clés issus de plusieurs protéines virales. Ces courts segments ont été enchâssés dans une seule chaîne à l’aide de linkers flexibles et associés à un peptide humain, la bêta‑défensine, comme adjuvant immunostimulant. Les modèles informatiques ont suggéré que cette molécule combinée se replierait en une structure stable et serait reconnue par une large gamme de profils immunitaires humains dans de nombreuses populations.
Explorer la réponse immunitaire à l’écran
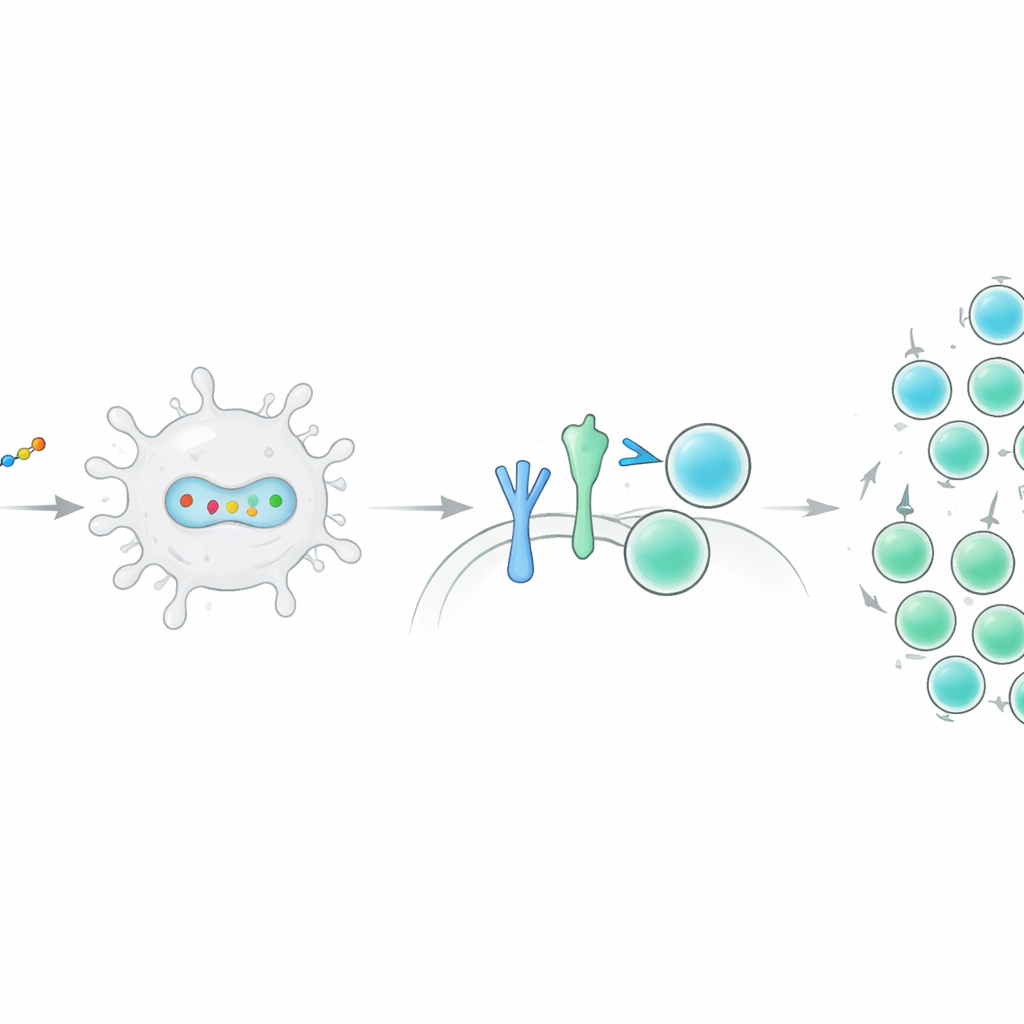
L’équipe a ensuite cherché à savoir si ce vaccin virtuel « parlerait » réellement au système immunitaire. À l’aide de simulations d’amarrage moléculaire, ils ont modélisé la manière dont la protéine conçue pourrait se lier à un détecteur clé, le récepteur de type Toll 3, qui aide les cellules immunitaires à repérer le matériel viral. Les résultats ont indiqué une liaison serrée et stable au site actif du récepteur, un bon signe que le composé pourrait déclencher les défenses initiales. Des simulations informatiques supplémentaires du système immunitaire sur une année, avec trois doses simulées, ont montré de fortes poussées d’anticorps et d’importantes expansions à la fois des cellules B et des cellules T, y compris des cellules mémoire persistantes longtemps après la vaccination. L’analyse d’optimisation des codons a suggéré que le vaccin pourrait être produit efficacement dans des systèmes bactériens courants, un avantage pour la fabrication.
Du plan informatique à la protection réelle
Dans l’ensemble, l’étude présente un plan vaccinal soigneusement conçu qui cible des éléments conservés et de grande valeur du virus chikungunya, les assemble en une seule molécule compacte et semble — in silico — provoquer des réponses immunitaires fortes et équilibrées dans des populations diverses. Pour les non‑spécialistes, le message clé est que, plutôt que de s’en tenir uniquement aux méthodes traditionnelles d’essais et d’erreurs, les scientifiques peuvent désormais exploiter des données virales mondiales et simuler des branches entières de la réponse immunitaire avant même d’entrer en laboratoire. Bien que ce vaccin contre le chikungunya n’existe pour l’instant que sous forme in silico et nécessite encore des tests rigoureux sur cellules et modèles animaux, il illustre une voie puissante vers des vaccins universels qui restent efficaces même si les virus continuent d’évoluer.
Citation: Hakim, M.S. Reverse vaccinology-based design of a universal multiepitope vaccine against chikungunya virus: Phylogenetic and immunoinformatics approaches. Sci Rep 16, 9284 (2026). https://doi.org/10.1038/s41598-026-39790-z
Mots-clés: virus chikungunya, vaccin universel, conception multépitope, vaccinologie inverse, immunoinformatique