Clear Sky Science · fr
Impact de l’oxydation des ARN en G-quadruplex sur leur dynamique conformationnelle et leur interaction avec TDP-43 associé à la SLA
Pourquoi c’est important pour la santé des nerfs
La sclérose latérale amyotrophique (SLA) est une maladie mortelle dans laquelle les cellules nerveuses qui contrôlent le mouvement meurent lentement, et pourtant les causes profondes de ce dommage sélectif restent mystérieuses. Cette étude pose une question simple mais essentielle : en vieillissant et en subissant un accroissement des dommages chimiques « rouille-like » au niveau cellulaire, cette usure de l’ARN — la copie active de nos gènes — perturbe-t-elle des signaux vitaux qui maintiennent les motoneurones en vie ? En se concentrant sur une forme d’ARN repliée particulière et une protéine clé liée à la SLA, TDP-43, le travail révèle comment de minuscules cicatrices chimiques pourraient contribuer à préparer le terrain pour la maladie. 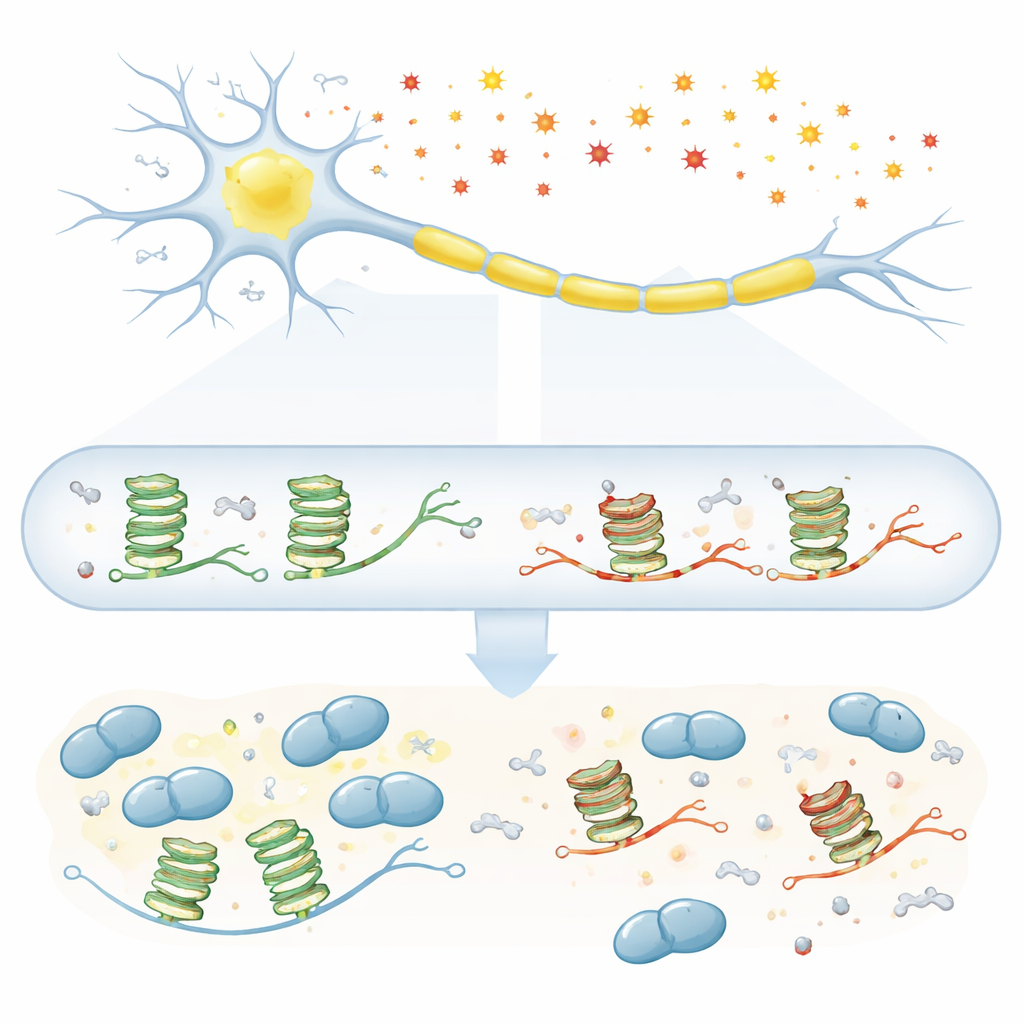
Un nœud d’ARN fragile au cœur des motoneurones
Les motoneurones dépendent d’un transport sur de longues distances d’ARN messagers le long de leurs axones afin que des protéines puissent être synthétisées in situ, près des connexions avec le muscle. Beaucoup de ces messages contiennent un « nœud » structural particulier appelé G-quadruplex, formé par des segments riches en guanine. Des protéines comme TDP-43 reconnaissent ce nœud et accrochent l’ARN à des granules de transport qui parcourent l’axone. Le problème est que la guanine est aussi la base la plus susceptible de s’oxyder lorsque les cellules sont soumises au stress des espèces réactives de l’oxygène, qui s’accumulent avec l’âge. Des indices antérieurs suggéraient que les G-quadruplex et TDP-43 jouent un rôle central dans la SLA, mais il restait incertain de savoir exactement comment l’oxydation de ces nœuds d’ARN pourrait perturber leur partenariat.
Observer le stress oxydatif déformer les formes d’ARN
Le chercheur a d’abord exposé des cellules de neuroblastome humain au peroxyde d’hydrogène, un agent oxydant courant, puis a examiné l’état des structures en G-quadruplex. Les signaux d’une sonde sensible aux G-quadruplex ont diminué à mesure que le stress oxydatif augmentait, indiquant que ces nœuds compacts d’ARN perdaient leur conformation normale. Pour définir la chimie en jeu, l’équipe a ensuite synthétisé des ARN formant des G-quadruplex et y a intentionnellement incorporé des quantités variables de 8-oxoguanine, une forme oxydée bien connue de la guanine retrouvée dans des neurones vieillissants et des tissus de SLA. À l’aide d’un ensemble d’outils biophysiques, ils ont montré que même des niveaux modestes de cette modification desserrent l’empilement ordonné du G-quadruplex, bien que l’issue exacte dépende de la séquence d’ARN environnante. 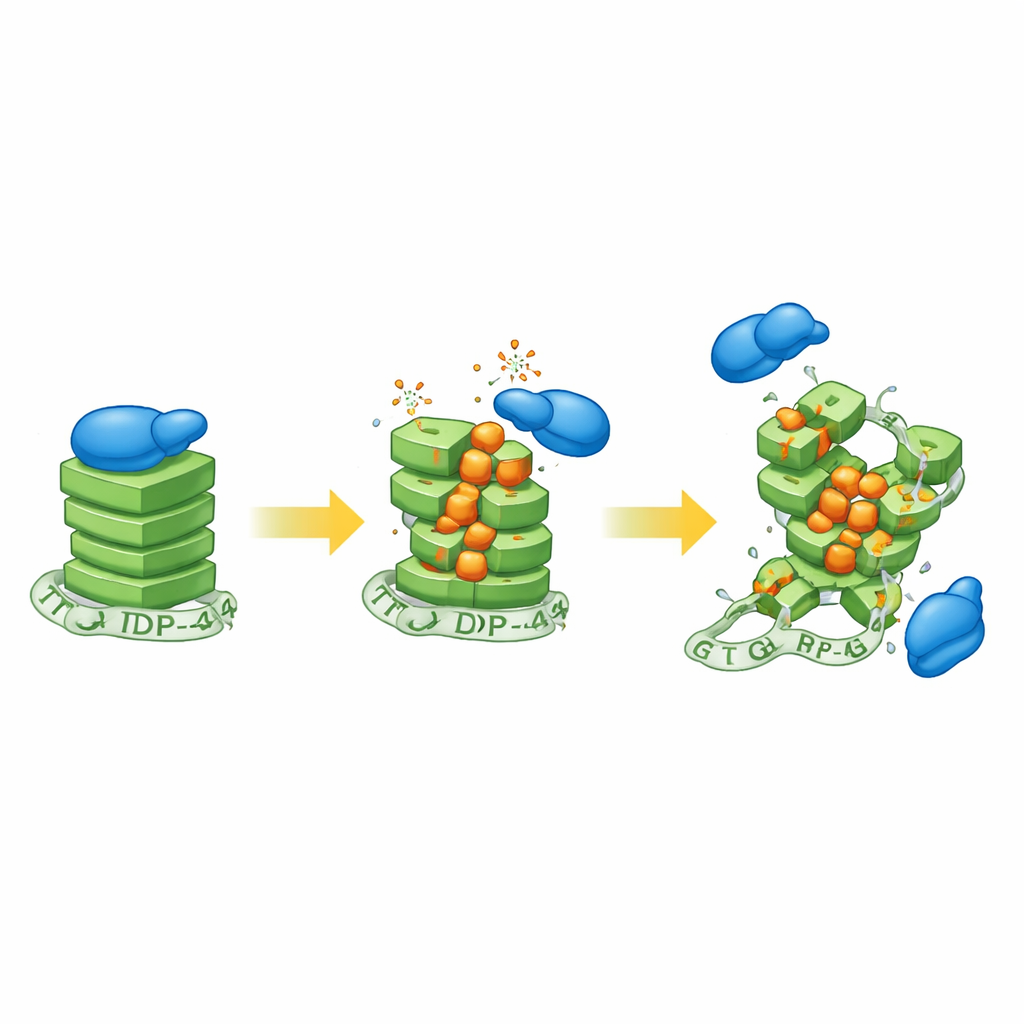
Nouveaux défauts : bases appariées de travers et brins mal associés
Une analyse plus fine a révélé deux types distincts de perturbations structurelles. Dans un G-quadruplex dérivé du message PSD-95, les guanines oxydées avaient tendance à s’apparier de manière inappropriée avec des adénines voisines, formant des « mésappariements » qui déforment subtilement le repliement. Ces mésappariements apparaissaient surtout à des niveaux d’oxydation intermédiaires, lorsque l’ARN pouvait encore s’assembler de façon transitoire en un G-quadruplex qui mettait en contact les mauvais partenaires. Dans un autre G-quadruplex issu du message CaMKIIα, une oxydation importante déstabilisait si fortement le nœud intramoléculaire habituel que les guanines intactes restantes cherchaient des partenaires sur d’autres brins d’ARN, favorisant des G-quadruplex intermoléculaires anormaux. De telles structures mal câblées pourraient emmêler différents ARN entre eux et perturber le trafic normal d’ARN à l’intérieur des neurones.
Quand l’ARN endommagé perd son partenaire protéique
L’étude a ensuite examiné comment ces nœuds déformés interagissent avec TDP-43. À l’aide d’essais de liaison par électrophorèse, le chercheur a montré que TDP-43 préfère fortement les G-quadruplex intacts et parallèles et lie de moins en moins l’ARN à mesure que des bases oxydées sont introduites. La structure de CaMKIIα, déjà très compacte, s’est révélée particulièrement sensible : même une faible oxydation a presque annihilé la liaison à TDP-43. Une seconde protéine, FUS — également liée à la SLA — a montré une perte d’affinité similaire mais un peu moins sévère, ce qui suggère que l’oxydation affaiblit globalement la capacité des protéines liant les G-quadruplex à s’attacher. Fait intrigant, lorsque TDP-43 était mélangé à de l’ARN légèrement oxydé, les données indiquaient que la protéine s’engageait sur une forme intermédiaire instable du G-quadruplex plutôt que sur un nœud complètement replié, laissant entrevoir une lutte dynamique entre stabilisation et effondrement.
Vulnérabilité accrue des protéines mutantes liées à la SLA
Le travail a en outre examiné dix variantes de TDP-43 trouvées chez des patients atteints de SLA, la plupart portant des modifications dans une queue flexible riche en glycine qui module la reconnaissance de l’ARN. Toutes ces variantes liaient déjà moins bien les G-quadruplex normaux que la protéine sauvage. Lorsque des ARN G-quadruplex oxydés ont été introduits en tant que compétiteurs, les mutants étaient encore moins capables que la protéine normale de reconnaître et de lier les structures endommagées. Certaines variantes situées dans des régions particulièrement propices au désordre étaient les plus affectées. Cela suggère un double coup chez les individus âgés porteurs de telles mutations : non seulement leur TDP-43 est intrinsèquement moins efficace, mais l’oxydation liée à l’âge érode encore sa capacité à escorter des messages cruciaux le long des axones des motoneurones.
Que signifie cela pour la compréhension de la SLA
En termes simples, cette étude montre que les dommages chimiques liés à l’âge modifient la forme de nœuds d’ARN délicats qui guident le transport des messages dans les motoneurones, et que ces nœuds déformés ne coopèrent plus correctement avec TDP-43 ou des protéines apparentées. Le résultat est une probabilité accrue d’un acheminement erroné ou d’un blocage des cargaisons d’ARN, précisément dans les axones longs et vulnérables qui contrôlent les muscles. Pour les personnes qui héritent aussi de mutations de TDP-43, cette affaiblissement induit par l’oxydation des interactions ARN–protéine peut pousser des neurones déjà stressés plus près de l’échec. En éclairant cette chaîne d’évènements subtile mais puissante — du stress oxydatif à l’altération de l’architecture de l’ARN jusqu’à la perturbation du transport — le travail met en avant l’oxydation des ARN en G-quadruplex comme un lien moléculaire prometteur entre le vieillissement et la SLA, et comme une cible potentielle pour des thérapies protectrices futures.
Citation: Ishiguro, A. Impact of G-quadruplex RNA oxidation on its conformational dynamics and interaction with ALS-associated TDP-43. Sci Rep 16, 8802 (2026). https://doi.org/10.1038/s41598-026-39767-y
Mots-clés: sclérose latérale amyotrophique, oxydation de l’ARN, G-quadruplex, TDP-43, dégénérescence des motoneurones