Clear Sky Science · fr
Identification de biomarqueurs liés aux lésions de la barrière hémato-encéphalique dans l’infarctus cérébral par analyse transcriptomique
Pourquoi cela importe pour l’AVC et la santé cérébrale
Lorsqu’une personne subit un AVC dû à l’obstruction d’un vaisseau sanguin cérébral, les médecins peuvent voir les lésions aux examens d’imagerie mais peinent parfois à prédire qui développera une aggravation par œdème, des hémorragies ou un handicap durable. Une grande partie de ces lésions survient au niveau du gardien protecteur du cerveau, la barrière hémato‑encéphalique, qui empêche normalement les substances nocives du sang de s’infiltrer dans le tissu nerveux fragile. Cette étude pose une question simple mais importante : existe‑t‑il des signaux moléculaires révélateurs qui indiquent quand cette barrière se détériore, et ces signaux pourraient‑ils un jour guider un meilleur diagnostic et traitement des patients victimes d’un AVC ?
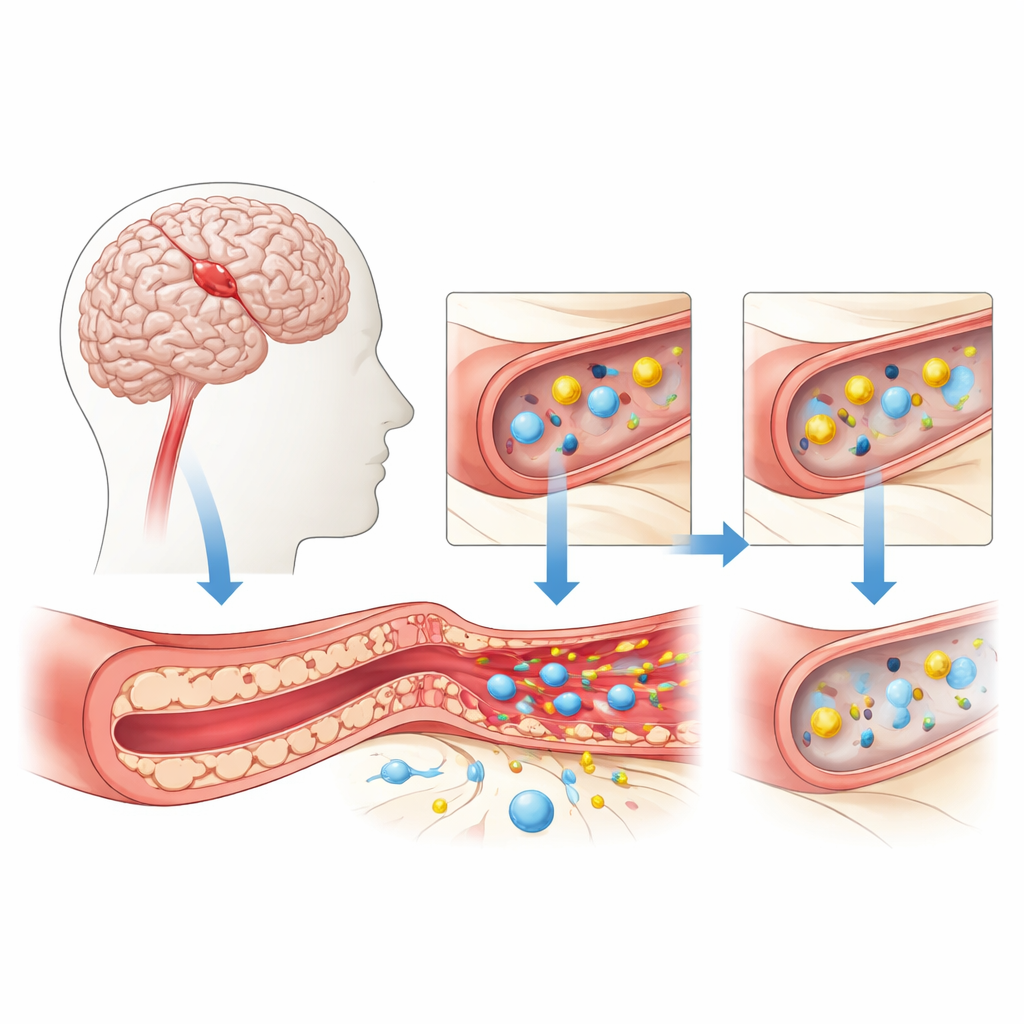
La barrière protectrice du cerveau sous stress
La barrière hémato‑encéphalique est formée par des cellules étroitement serrées qui tapissent les petits vaisseaux cérébraux. Ces cellules contrôlent avec soin ce qui peut passer du sang au cerveau, laissant entrer des nutriments vitaux comme l’oxygène et le glucose tout en bloquant les toxines et les cellules immunitaires potentiellement nocives. Lors d’un infarctus cérébral, ou AVC ischémique, le flux sanguin chute brutalement. Privées d’oxygène et de sucre, ces cellules des parois vasculaires se stressent et commencent à perdre leur étanchéité. Des interstices s’ouvrent entre elles, des liquides s’infiltrent dans le tissu environnant, et des messagers chimiques de l’inflammation envahissent la zone, ce qui peut aggraver l’œdème et les lésions cérébrales.
Recréer les lésions de l’AVC en laboratoire
Pour sonder ce qui se passe au sein de ces cellules barrières, les chercheurs ont utilisé une lignée cellulaire humaine bien connue qui mime le revêtement des vaisseaux cérébraux. Ils ont exposé ces cellules à un environnement pauvre en oxygène et sans glucose — appelé privation d’oxygène‑glucose — pour reproduire les conditions d’un AVC, puis ont rétabli des conditions normales pour simuler le traitement et la récupération. Ils ont mesuré la survie cellulaire, la fuite d’une enzyme indicative de dommage cellulaire, et la libération de molécules inflammatoires. Comme prévu, le traitement stressant a réduit la santé des cellules, augmenté les signaux inflammatoires tels que IL‑1β, IL‑6 et TNF‑α, et accru la fuite d’un marqueur de lésion appelé LDH. Lorsque l’oxygène et les nutriments ont été rétablis, nombre de ces changements délétères se sont atténués et les cellules ont retrouvé une partie de leur capacité à former des structures tubulaires dans un test de croissance.
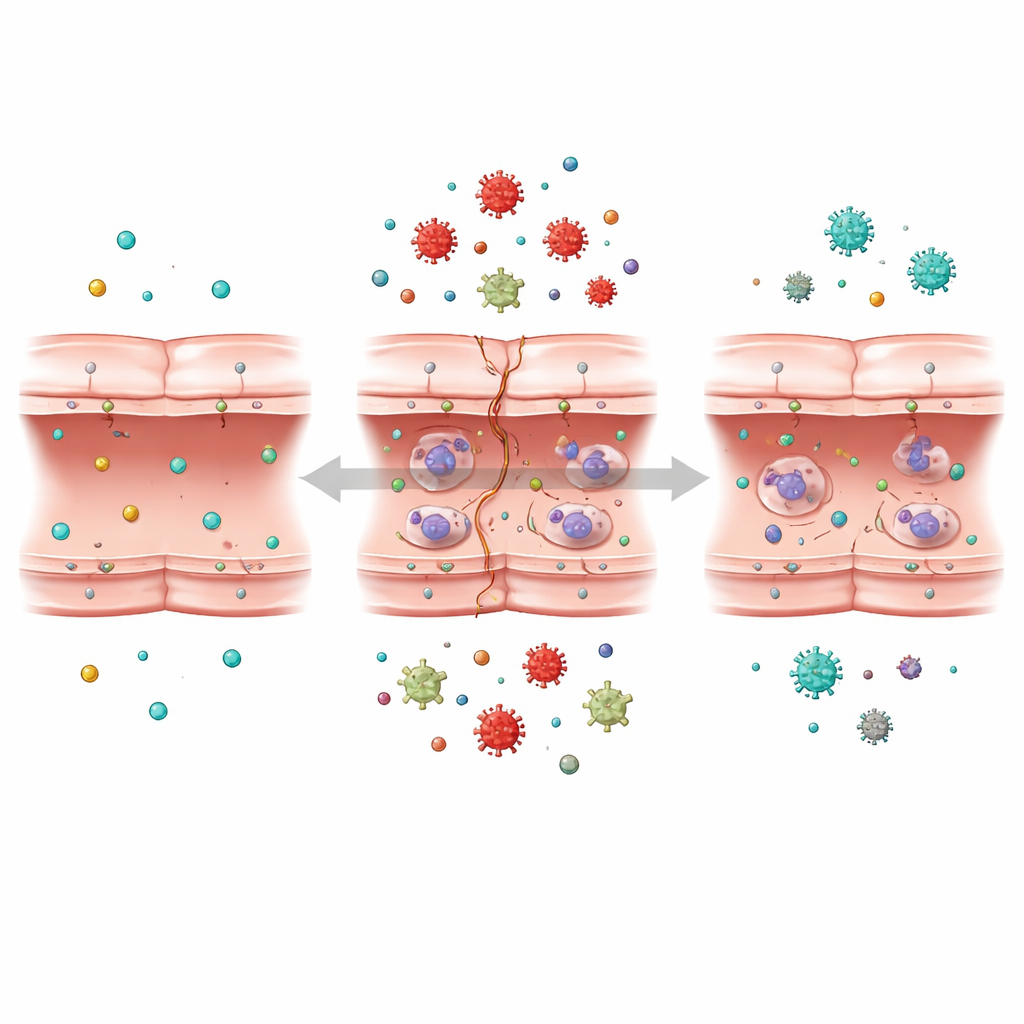
Écouter la conversation moléculaire de la cellule
L’équipe s’est ensuite tournée vers une technique puissante appelée transcriptomique, qui mesure l’activité de milliers de gènes simultanément. En comparant des cellules normales, des cellules privées d’oxygène et de glucose, et des cellules autorisées à récupérer, ils ont identifié plus d’un millier de gènes dont l’activité variait en réponse au stress de type AVC. À l’aide d’outils de données avancés et d’apprentissage automatique, ils ont regroupé des gènes au comportement similaire et recherché ceux les plus fortement liés aux lésions de la barrière. Ils ont trouvé que beaucoup des gènes les plus affectés étaient liés à trois structures cellulaires clés : le ribosome, qui assemble les protéines ; le réticulum endoplasmique, qui aide à les plier et à les traiter ; et les mitochondries, les petites centrales énergétiques qui fournissent l’énergie.
Les ribosomes émergent comme signaux révélateurs
À partir de ce vaste ensemble de gènes, les chercheurs ont utilisé un algorithme de forêt aléatoire — un type d’apprentissage automatique basé sur des arbres de décision — pour réduire la liste à un petit nombre de gènes particulièrement informatifs. Ils ont ensuite cartographié les interactions entre les protéines correspondantes. Cette analyse a mis en évidence six gènes centraux, pour la plupart liés au ribosome, l’usine à protéines de la cellule. Dans la condition de type AVC, ces gènes liés aux ribosomes étaient davantage activés, tandis que leur activité revenait vers la normale lorsque l’oxygène et le glucose étaient rétablis. Ce schéma suggère que des changements dans la machinerie de production protéique de la cellule peuvent constituer un signal précoce et sensible des lésions et de la récupération de la barrière hémato‑encéphalique.
Ce que cela pourrait signifier pour les soins futurs
Pour un public non spécialiste, l’idée principale est que cette étude identifie une nouvelle classe de « voyants » moléculaires qui s’allument lorsque la barrière protectrice du cerveau est lésée lors d’un AVC. Plutôt que de se concentrer uniquement sur des coupables bien connus, comme des enzymes qui dégradent la paroi vasculaire, le travail montre que les usines à protéines cellulaires réagissent fortement à la lésion puis se calment lorsque les conditions s’améliorent. Si des recherches ultérieures confirment que ces marqueurs liés aux ribosomes peuvent être détectés dans des échantillons de patients, par exemple le sang, les médecins pourraient un jour les utiliser pour estimer l’ampleur des lésions de la barrière, mieux chronométrer les traitements visant à réduire l’inflammation et l’œdème, et tester de nouveaux médicaments destinés à préserver ce gardien crucial de la santé cérébrale.
Citation: Liu, X., He, Y., Zhang, N. et al. Identification of blood-brain barrier injury-related biomarkers in cerebral infarction using transcriptomic analysis. Sci Rep 16, 8119 (2026). https://doi.org/10.1038/s41598-026-39763-2
Mots-clés: accident ischémique, barrière hémato-encéphalique, biomarqueurs, gènes ribosomiques, cellules endothéliales