Clear Sky Science · fr
L'inflammation chronique favorise la progression du cancer gastrique via la clivage de CX3CL1 médié par ADAM10
Pourquoi une irritation gastrique prolongée importe
Beaucoup de personnes vivent pendant des années avec une irritation gastrique persistante causée par une infection, l'alimentation ou d'autres problèmes de santé. Cette irritation chronique de bas niveau, désignée comme inflammation chronique, est un facteur de risque silencieux pour le cancer de l'estomac (gastrique), l'un des cancers les plus mortels au monde. L'étude résumée ici pose une question ciblée : comment l'inflammation chronique pousse-t-elle les tumeurs gastriques précoces à croître plus rapidement et à se disséminer ? En suivant un signal chimique précis et l'enzyme qui l'active, les chercheurs mettent au jour un point faible potentiel que des traitements futurs pourraient cibler.
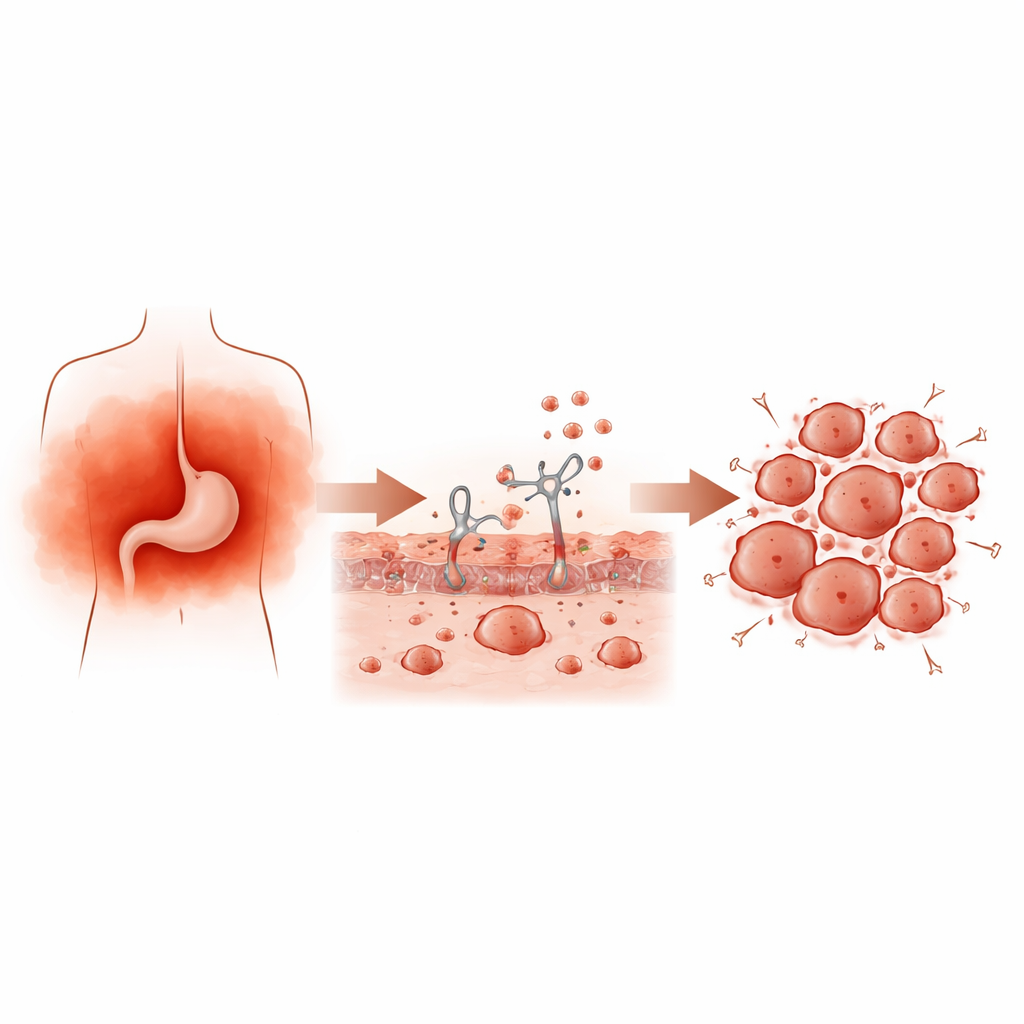
De l'irritation à des tumeurs à croissance accélérée
Pour reproduire l'inflammation prolongée, l'équipe a exposé à plusieurs reprises des souris à des substances déclenchant des réactions immunitaires, puis a implanté des cellules de cancer gastrique sous la peau. Par rapport aux animaux témoins, les souris présentant une inflammation chronique ont développé des tumeurs plus grosses et plus lourdes, remplies de cellules en division et d'infiltrats cellulaires immunitaires. Dans des expériences en culture cellulaire, le sérum sanguin prélevé sur des rats présentant différents niveaux d'inflammation a stimulé la croissance et la formation de colonies des cellules humaines de cancer gastrique de manière plus vigoureuse. Ensemble, ces résultats montrent que des signaux inflammatoires circulants dans l'organisme peuvent accélérer directement la croissance tumorale.
À la recherche du signal perturbateur clé
La suite a consisté à identifier quelles molécules messagères inflammatoires faisaient le plus de dégâts. À l'aide d'une large puce protéique, les chercheurs ont comparé de nombreux cytokines dans les tumeurs de souris inflammées et non inflammées et ont trouvé neuf molécules clairement augmentées. En recoupant avec des jeux de données publics de patients, ils ont focalisé l'attention sur un candidat remarquable : CX3CL1, une chimiokine qui aide au guidage des cellules immunitaires. Les niveaux de CX3CL1 étaient plus élevés dans les tumeurs gastriques que dans le tissu gastrique normal, particulièrement augmentés dans les tumeurs plus avancées, et associés à une survie moindre chez les patients. Des mesures dans des tumeurs de souris ont confirmé que l'inflammation chronique élevait localement les niveaux de CX3CL1, suggérant que ce signal unique pourrait contribuer à expliquer le lien entre inflammation et pronostic défavorable.
Quelles cellules émettent et reçoivent le signal ?
En utilisant le séquençage ARN unicellulaire, les investigateurs ont cartographié l'activité génique cellule par cellule à l'intérieur des tumeurs. Ils ont découvert que CX3CL1 était produit principalement par les cellules cancéreuses elles‑mêmes plutôt que par les cellules immunitaires ou stromales environnantes. Son récepteur partenaire, CX3CR1, était présent sur plusieurs types cellulaires, mais sous inflammation chronique il est devenu plus proéminent sur les cellules tumorales. Une sous‑population tumorale spécifique, accrue dans les tumeurs inflammées, présentait une forte expression de CX3CL1 et des signes d'augmentation de la production protéique et de la prolifération. En tests de laboratoire, l'ajout de CX3CL1 purifié directement aux cellules de cancer gastrique augmentait leur survie, leur capacité à former des colonies et leur mobilité. Le blocage de CX3CR1 atténuait ces effets, indiquant que les cellules cancéreuses envoyaient et répondaient à ce signal favorisant la croissance.
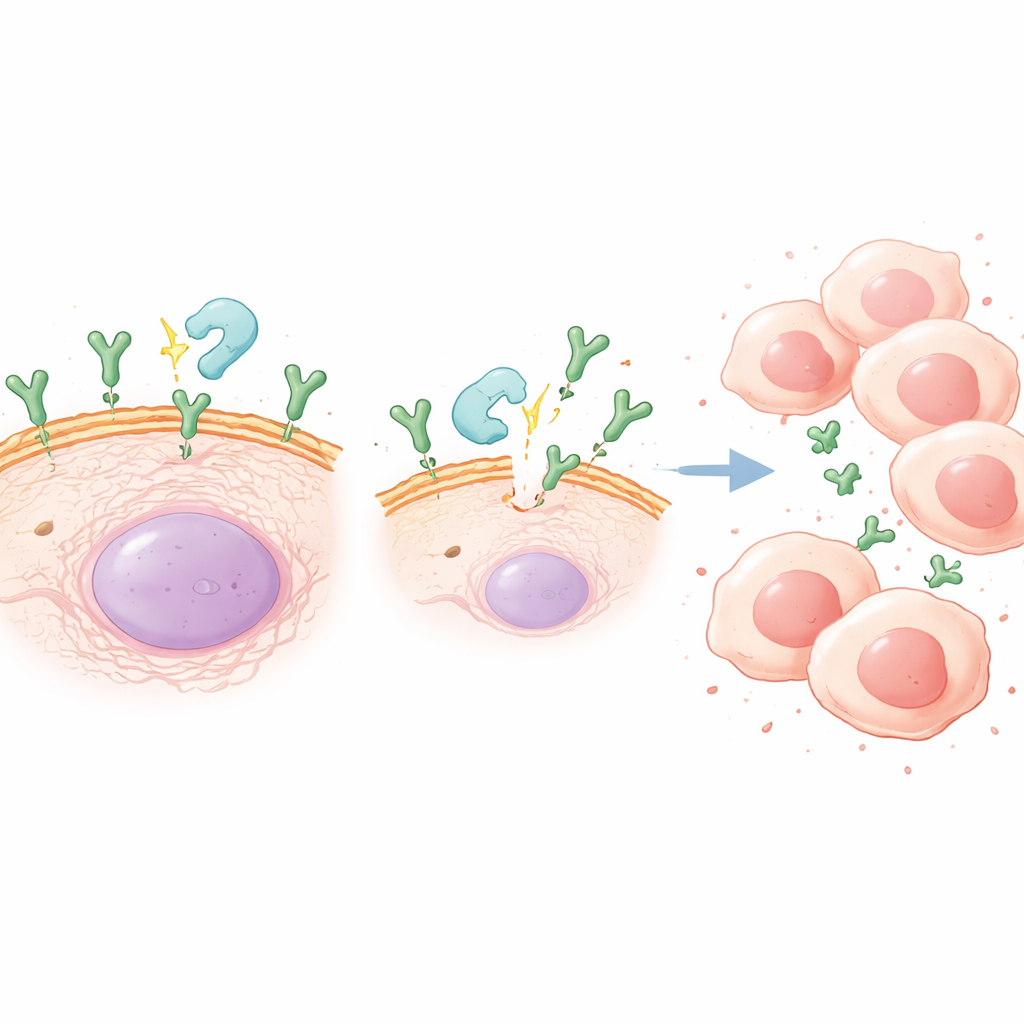
L'enzyme qui augmente le danger
CX3CL1 existe sous une forme ancrée à la membrane cellulaire et sous une forme soluble qui peut se diffuser dans les tissus. La forme soluble est générée lorsqu'une enzyme appelée ADAM10 clive la version membranaire. L'étude a montré que l'inflammation chronique augmentait les niveaux d'ADAM10 dans les tumeurs de souris et dans des cellules de cancer gastrique exposées à un stimulus inflammatoire en laboratoire. Lorsque les chercheurs ont traité les cellules avec un inhibiteur d'ADAM10, la quantité de CX3CL1 soluble dans le milieu environnant a diminué et les augmentations de croissance et de mobilité des cellules cancéreuses induites par l'inflammation ont été largement inversées. Chez des souris présentant une inflammation chronique, le blocage d'ADAM10 a ralenti la progression tumorale et réduit les niveaux de CX3CL1 dans les tumeurs, renforçant l'idée que cette étape enzymatique de « shedding » est critique.
Ce que cela signifie pour les patients souffrant de problèmes gastriques chroniques
Pris ensemble, les travaux décrivent une chaîne d'événements simple : l'inflammation persistante dans et autour de l'estomac active ADAM10 dans les cellules du cancer gastrique ; ADAM10 libère alors davantage de CX3CL1 soluble, qui à son tour se répercute sur les cellules tumorales pour les aider à se multiplier et à migrer. Pour un non‑spécialiste, c'est comme si un environnement irrité apprenait aux cellules tumorales à à la fois crier et écouter un message favorisant la croissance. Parce que ADAM10 et CX3CL1 sont des molécules identifiables suscitant déjà un intérêt pharmacologique, ce nouvel axe « ADAM10/CX3CL1 » décrit offre une cible tangible pour des thérapies visant à ralentir ou prévenir la progression du cancer gastrique liée à l'inflammation.
Citation: Song, Z., Liu, Y., Wang, Z. et al. Chronic inflammation promotes gastric cancer progression via ADAM10-mediated cleavage of CX3CL1. Sci Rep 16, 9169 (2026). https://doi.org/10.1038/s41598-026-39743-6
Mots-clés: cancer gastrique, inflammation chronique, chimio‑attractants, microenvironnement tumoral, ADAM10