Clear Sky Science · fr
La variation p.Arg676Cys de Sema5A associée aux troubles du spectre autistique active la signalisation Arf6/FE65 et provoque une morphogenèse cellulaire aberrante
Comment une infime modification peut perturber le câblage du cerveau
Le trouble du spectre autistique affecte la façon dont les personnes communiquent, interagissent et réagissent au monde qui les entoure, mais les étapes biologiques menant d’un changement d’ADN à une altération des fonctions cérébrales restent souvent mystérieuses. Cette étude examine l’un de ces changements génétiques dans une protéine « guide » du cerveau appelée Sema5A et montre, avec un niveau de détail inhabituel, comment un seul acide aminé remplacé dans cette protéine peut pousser les jeunes neurones à développer des branches excessivement longues et emmêlées. Comprendre cette erreur microscopique de câblage pourrait, à terme, aider les chercheurs à concevoir des traitements qui ramèneraient les cellules nerveuses vers une forme plus saine.
Des cellules cérébrales qui s’étendent trop loin
Lors du développement cérébral, les jeunes neurones envoient de longues extensions fines qui recherchent les partenaires appropriés, formant les circuits sous-jacents à la pensée et au comportement. Cette croissance doit être finement contrôlée : un nombre insuffisant de ramifications empêche les connexions ; un excès peut rendre les circuits bruyants ou mal câblés. Des travaux antérieurs avaient montré qu’une variante de Sema5A liée à l’autisme, où un acide aminé en position 676 passe de l’arginine à la cystéine, provoque la croissance de processus anormalement longs chez des neurones en culture. La nouvelle étude visait à découvrir quels interrupteurs internes et protéines auxiliaires ce Sema5A mutant utilise pour entraîner une telle prolifération incontrôlée.
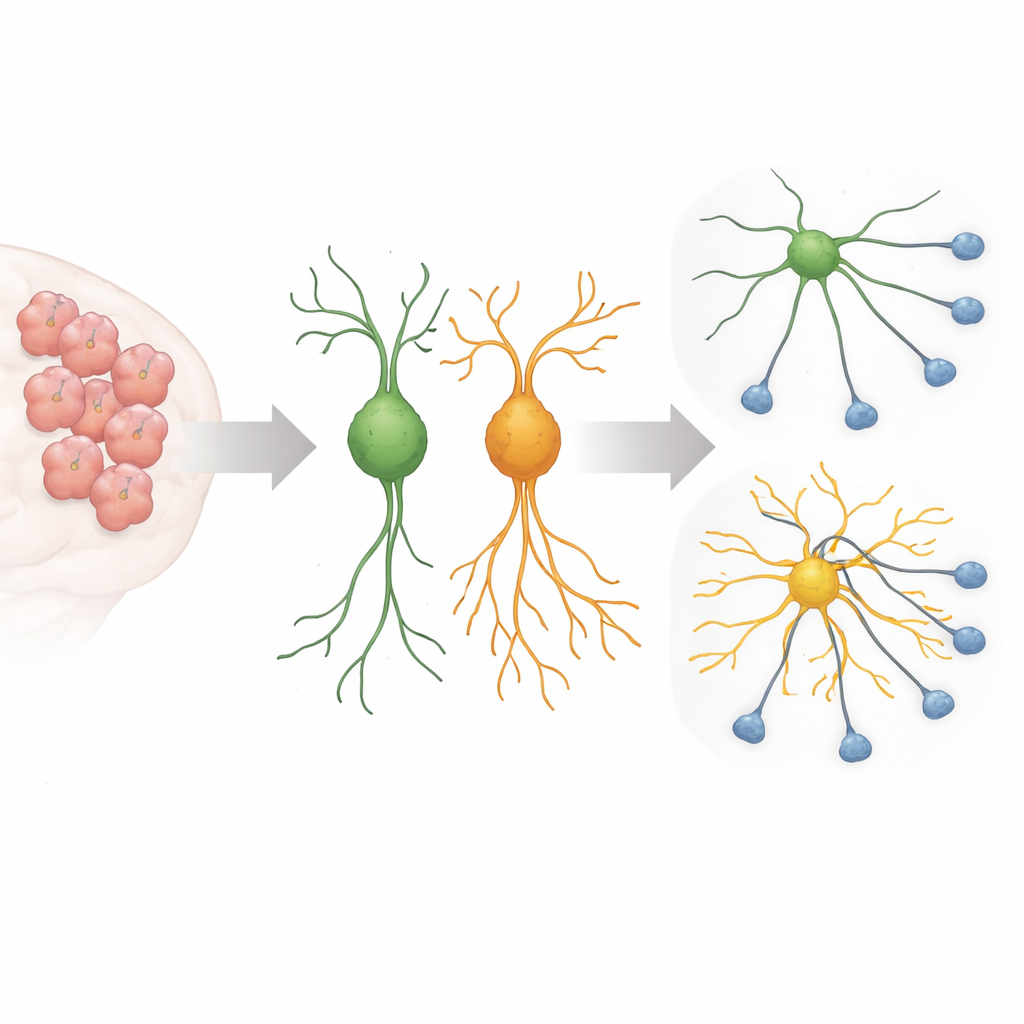
Un signal trompeur à l’intérieur de la cellule
Les chercheurs se sont concentrés sur un petit interrupteur moléculaire appelé Arf6 et sur une protéine échafaudage nommée FE65, toutes deux connues pour participer à la structuration des membranes cellulaires et du cytosquelette qui soutient les extensions cellulaires. En utilisant un système CRISPR–Cas13 pour réduire sélectivement ces protéines dans des cellules neuronales de souris et des cellules cérébrales primaires de souris, ils ont constaté que l’abaissement d’Arf6 ou de FE65 réduisait fortement la croissance excessive provoquée par le Sema5A mutant. Les processus longs et filamenteux se sont raccourcis vers des longueurs plus typiques, et les marqueurs de maturation neuronale ont diminué, suggérant que l’effet de la mutation dépend largement de cette voie de signalisation particulière.
Connexion au moteur de la forme cellulaire
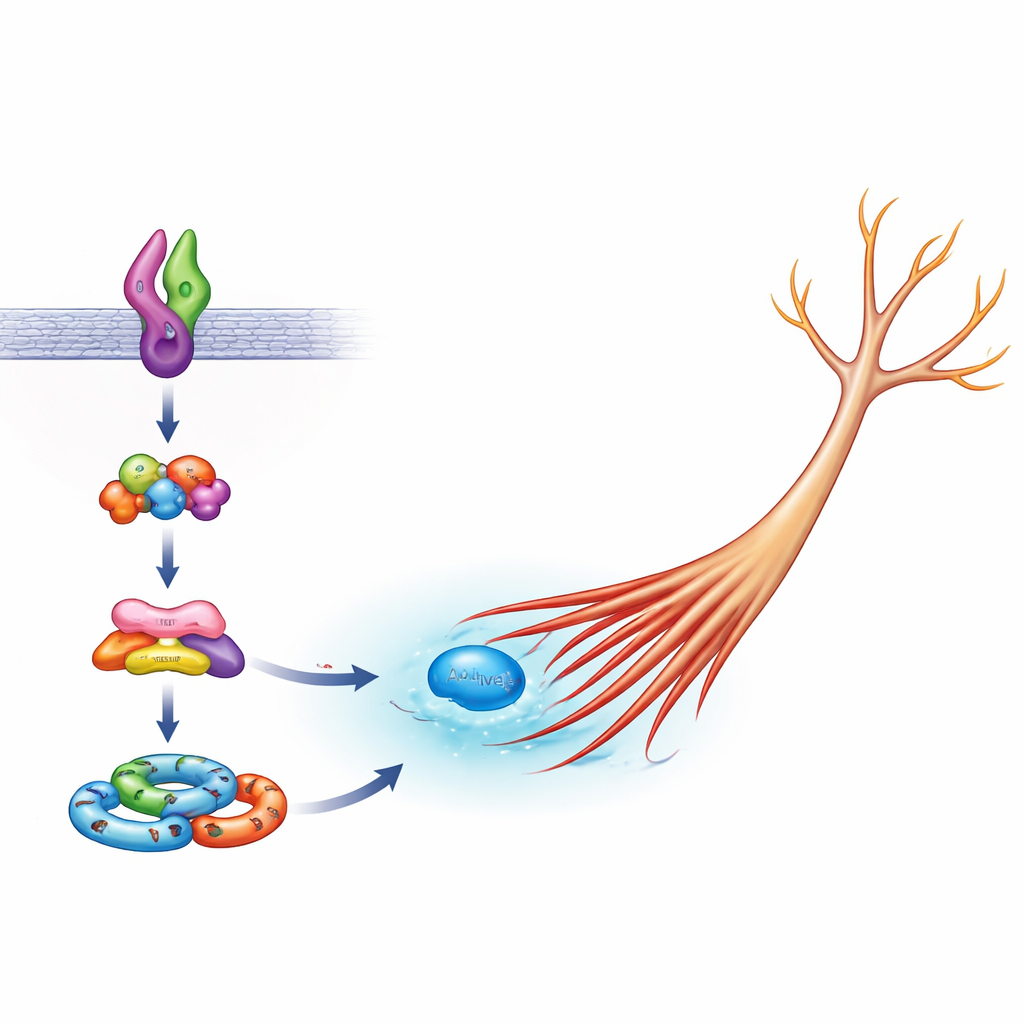
À l’intérieur des neurones, une famille de molécules agit comme un « moteur » de la forme en contrôlant l’actine, le principal filament structurel des branches cellulaires. Un membre clé de cette famille, Rac1, s’active normalement pour aider l’extension des neurites, mais une activité excessive peut entraîner une croissance incontrôlée. L’équipe a montré que, dans les cellules portant la Sema5A normale, Arf6 est nécessaire pour l’activation ordinaire de Rac1 lors d’une croissance saine, tandis que FE65 n’est pas indispensable. En présence de la Sema5A mutante, cependant, Arf6 et FE65 deviennent tous deux critiques : réduire l’un ou l’autre, ou inonder la cellule uniquement avec la région de FE65 qui se lie à son partenaire ELMO2, ramenait l’activité anormalement élevée de Rac1 vers la normale. Cela implique que la version néfaste de Sema5A exploite spécifiquement un complexe Arf6–FE65–ELMO2–DOCK5 pour surstimuler Rac1 et pousser les neurites à s’allonger excessivement.
Un pôle encombré de partenaires de signalisation
Pour comprendre comment ces éléments s’imbriquent, les scientifiques ont également examiné des « signalosomes » basés sur ELMO2 — des amas de protéines qui s’assemblent pour relayer les signaux de croissance. Lorsque Arf6 ou FE65 était réduit, les cellules exprimant la Sema5A mutante formaient moins de ces complexes ELMO2 dans leur corps et au niveau des pointes en croissance, ce qui corrobore l’idée qu’Arf6 et FE65 contribuent à construire la machinerie transformant la mutation de Sema5A en un changement physique de la forme cellulaire. Ce travail s’inscrit dans un tableau plus large où de petits interrupteurs moléculaires comme Arf6 et Rac1, aidés par des échafaudages tels que FE65, jouent le rôle de plaques tournantes reliant de nombreux gènes associés à l’autisme à l’architecture finale des circuits cérébraux.
Pourquoi cette chaîne microscopique est importante
Pour un non-spécialiste, l’abondance d’acronymes et de noms protéiques peut sembler éloignée de l’expérience vécue de l’autisme. Pourtant, cette étude offre un pont concret : elle retrace comment une modification génétique précise de Sema5A peut suractiver une chaîne spécifique de molécules auxiliaires, provoquant l’allongement excessif des branches des neurones et pouvant conduire à un câblage cérébral atypique. En identifiant Arf6, FE65 et le complexe de signalisation ELMO2 comme des maillons cruciaux de cette chaîne, le travail met en lumière des cibles médicamenteuses potentielles. En principe, des médicaments qui régulent doucement cette voie suractive pourraient un jour aider à corriger les altérations de la forme cellulaire associées aux formes d’autisme liées à Sema5A, ajoutant une pièce importante au puzzle plus large des troubles du neurodéveloppement.
Citation: Takahashi, M., Yako, H., Miyamoto, Y. et al. Autism spectrum disorder-associated Sema5A p.Arg676Cys drives Arf6/FE65 signaling and aberrant cell morphogenesis. Sci Rep 16, 9423 (2026). https://doi.org/10.1038/s41598-026-39722-x
Mots-clés: trouble du spectre autistique, mutation Sema5A, morphogenèse neuronale, signalisation Rac1, voie Arf6 FE65