Clear Sky Science · fr
Effets létaux des structures d’ivermectine sur les vecteurs du paludisme et analyse in silico des interactions avec leurs canaux ioniques chlorure activés par le glutamate
Transformer un antiparasitaire en tueur de moustiques
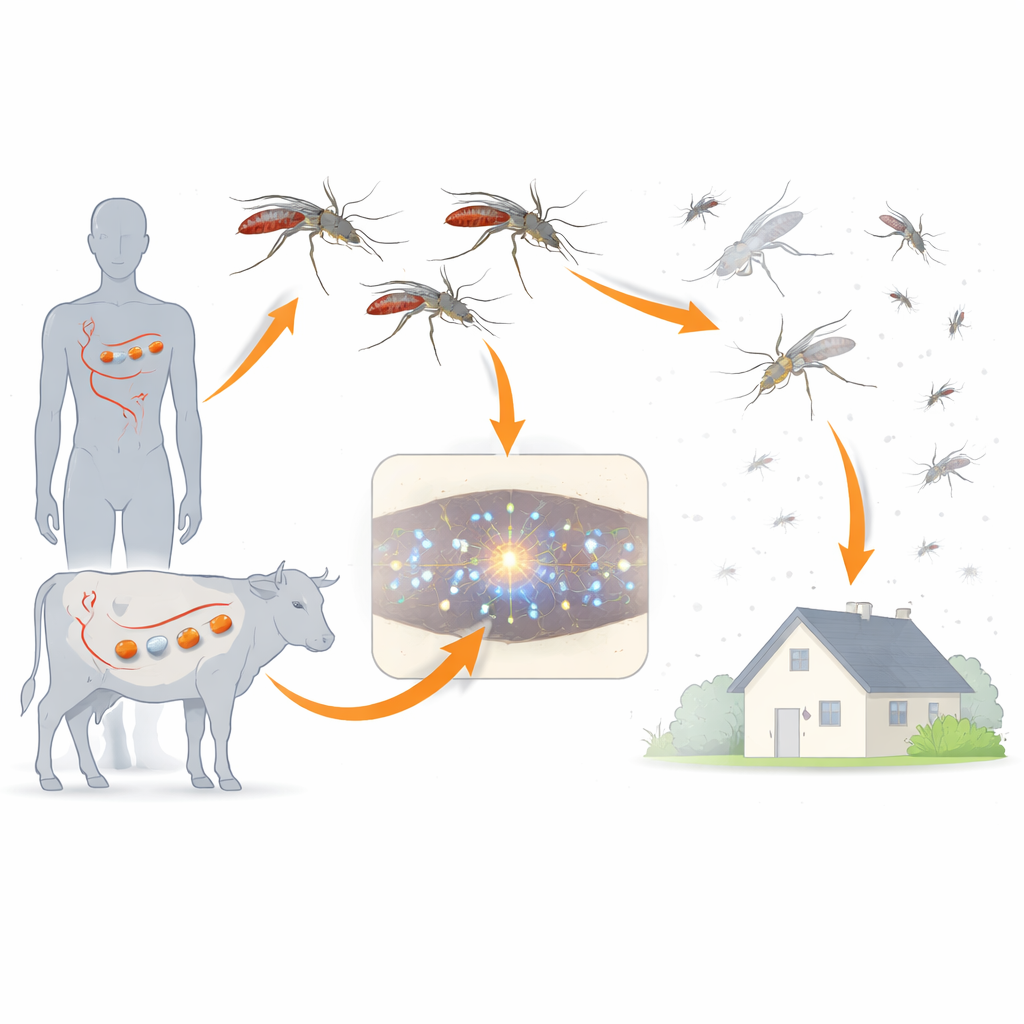
L’ivermectine est surtout connue comme médicament contre les vers parasites chez l’humain et le bétail, mais elle a un effet secondaire surprenant : les moustiques qui s’alimentent de sang traité meurent souvent. Cela ouvre une piste intrigante pour le contrôle du paludisme : administrer l’ivermectine aux personnes ou aux animaux pourrait-il réduire suffisamment les populations locales de moustiques pour diminuer la transmission ? Cette étude explore en profondeur comment l’ivermectine et des molécules apparentées tuent les moustiques Anopheles vecteurs du paludisme, et quelles modifications pourraient un jour permettre aux moustiques d’échapper à cet effet.
Pourquoi tuer des moustiques par le sang est important
Les méthodes classiques de lutte contre le paludisme reposent sur des moustiquaires et des pulvérisations d’insecticide, qui visent les moustiques de l’extérieur. L’ivermectine propose une stratégie différente : lorsque les humains ou les animaux prennent le médicament, leur sang devient mortel pour les moustiques hématophages. Les chercheurs se sont concentrés sur deux vecteurs importants du sud-est asiatique, Anopheles dirus et Anopheles minimus, qui diffèrent fortement dans leur sensibilité létale à l’ivermectine. En comparant ces espèces, l’équipe a cherché à comprendre pourquoi le médicament est plus mortel pour certains moustiques que pour d’autres et comment la structure chimique influence cette toxicité.
Tester quelles parties de la molécule comptent
L’ivermectine est une molécule volumineuse centrée sur un grand cycle portant deux anneaux de sucre. L’équipe a comparé l’ivermectine complète (avec ses deux sucres) à une version ne conservant qu’un seul sucre (appelée monosaccharide) et à un cœur dépourvu de sucres (aglycone). Ils ont intégré ces composés, à différentes concentrations, dans des repas sanguins distribués à des milliers de moustiques et ont suivi la survie pendant dix jours. L’ivermectine complète était fortement létale, en particulier pour An. minimus, tandis que le monosaccharide était beaucoup moins actif et que l’aglycone n’avait presque aucun pouvoir mortel à des doses réalistes. Autrement dit, la suppression d’un anneau sucre transformait un puissant tueur de moustiques en un composé bien plus faible, et la suppression des deux effaçait presque l’effet.
Regarder à l’intérieur du portillon nerveux du moustique
L’ivermectine agit sur une minuscule porte des cellules nerveuses et musculaires appelée canal chlorure activé par le glutamate (GluCl). Lorsqu’on force l’ouverture de cette porte, des ions chlorure affluent, l’activité électrique s’effondre et le moustique devient paralysé puis meurt. À l’aide de prédictions avancées de structures protéiques et d’un docking informatique, les chercheurs ont construit des modèles tridimensionnels du canal GluCl des Anopheles et ont simulé la manière dont l’ivermectine et ses variantes s’y logent. Ils ont découvert que, chez les moustiques, une partie spécifique de la boucle protéique près du pore — contenant une thréonine en position 304 — peut former une liaison hydrogène avec le deuxième anneau sucre de l’ivermectine. Cette liaison, ainsi que des attractions faibles voisines, semble stabiliser une conformation liée au médicament qui maintient le canal ouvert.
Pourquoi certaines formes tuent et d’autres non
Les simulations ont révélé un schéma constant : l’ivermectine complète et trois principaux produits de dégradation de l’ivermectine trouvés chez l’humain s’insèrent profondément dans le canal, permettant à leur deuxième anneau sucre d’interagir étroitement avec la boucle clé. Ces formes présentaient toutes une liaison prédite forte et, dans des travaux antérieurs, se sont révélées aussi létales pour les moustiques que le médicament parent. Le monosaccharide, dépourvu de ce deuxième sucre, pouvait encore toucher la boucle faiblement mais ne pouvait pas former la même liaison stabilisante, ce qui correspond à son pouvoir létal beaucoup plus faible. L’aglycone ne contactait pas du tout la boucle, en accord avec son incapacité à tuer les moustiques lors des tests d’alimentation. Parmi toutes les structures, une interaction commune avec une autre partie du canal (dans la sous-unité opposée) a également émergé comme importante, suggérant que plusieurs points de contact agissent ensemble pour verrouiller le portillon en position ouverte.
Perspectives sur la résistance et des outils améliorés
Les résultats indiquent que le deuxième anneau sucre de l’ivermectine — et sa capacité à se lier à une boucle spécifique du canal GluCl du moustique — est central dans son effet létal. Cette image plus précise de l’ajustement de la molécule dans le canal met en évidence des points faibles potentiels où de futures mutations pourraient réduire l’affinité et conduire à une résistance. Elle suggère aussi des pistes pour que les chimistes modifient des molécules de type ivermectine afin de préserver ou d’accroître leur puissance contre les moustiques. Bien que l’étude repose sur des modèles informatiques qui nécessitent encore une confirmation expérimentale, elle renforce l’intérêt des stratégies basées sur l’ivermectine comme élément de la boîte à outils de lutte contre le paludisme et pointe des caractéristiques moléculaires qu’il conviendra de surveiller lors du déploiement de telles stratégies.
Citation: Nguyen, M.N., Jones, A.K., Hotwagner, D. et al. Lethal effects of ivermectin structures on malaria vectors and in silico analysis of interactions with their glutamate-gated chloride ion channels. Sci Rep 16, 8141 (2026). https://doi.org/10.1038/s41598-026-39698-8
Mots-clés: ivermectine, vecteurs du paludisme, Moustiques Anopheles, canaux ioniques, résistance aux insecticides