Clear Sky Science · fr
Les exosomes de CSMOs régulent l’apoptose des cellules endothéliales microvasculaires pulmonaires via circRNA_43350/miR-342-5p dans la BPCO
Pourquoi protéger les fragiles vaisseaux sanguins pulmonaires est important
La bronchopneumopathie chronique obstructive, ou BPCO, prive lentement les personnes de souffle et d’autonomie. La fumée de cigarette n’irrite pas seulement les voies respiratoires, elle endommage aussi le réseau délicat de minuscules vaisseaux sanguins qui entourent les alvéoles où l’oxygène passe dans le sang. Dans cette étude, les chercheurs se sont demandé si des « colis » naturels libérés par des cellules souches de la moelle osseuse pouvaient protéger ces vaisseaux pulmonaires vulnérables contre les lésions induites par la fumée, et pourquoi cette protection semble diminuée dans la BPCO. Leurs résultats révèlent une petite boucle génétique circulaire qui agit comme une éponge moléculaire, absorbant un signal nuisible et aidant les vaisseaux pulmonaires à survivre.
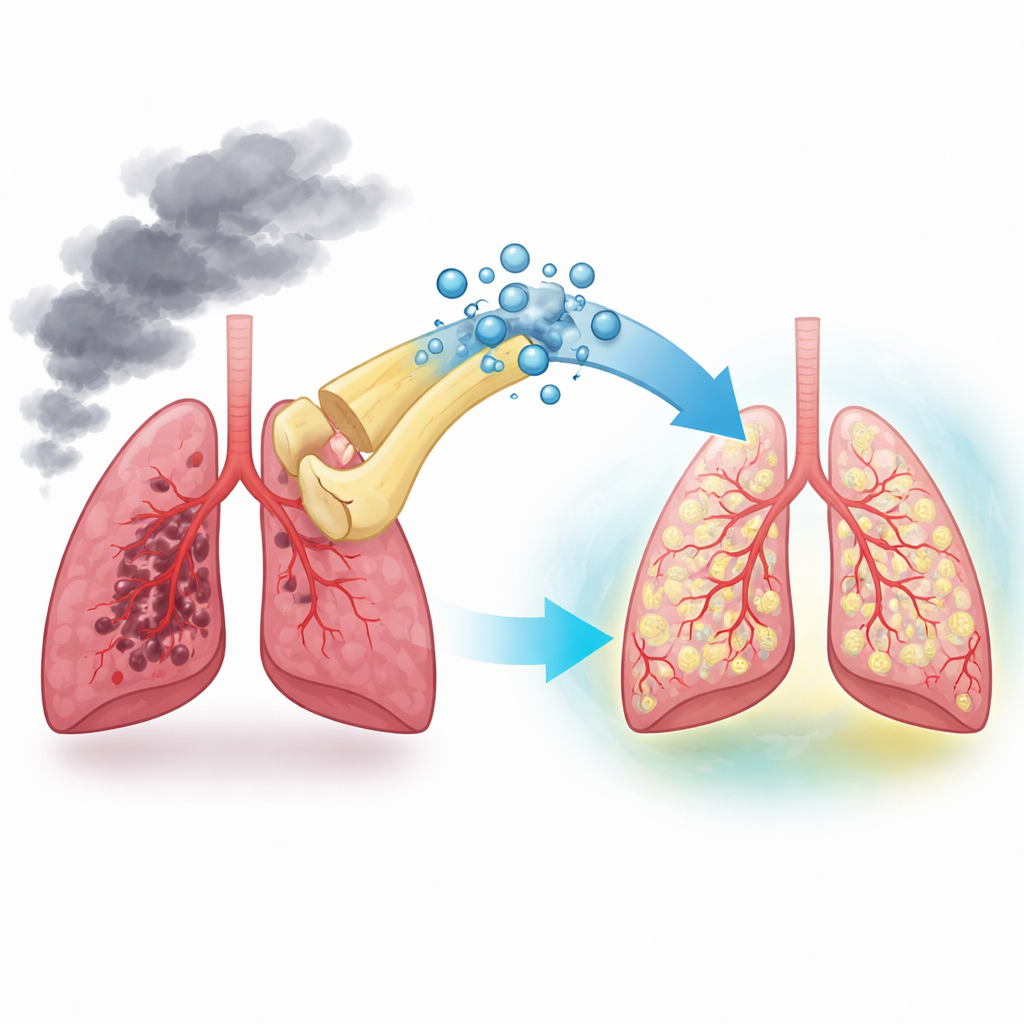
De petites enveloppes réparatrices issues des cellules souches
Les cellules souches mésenchymateuses de la moelle osseuse sont connues pour leur capacité à calmer l’inflammation et à soutenir la réparation tissulaire, non seulement en se différenciant en d’autres types cellulaires mais aussi en émettant de minuscules vésicules appelées exosomes. Ces exosomes contiennent des protéines et du matériel génétique et peuvent être absorbés par d’autres cellules comme des instructions prêtes à l’emploi. Les chercheurs ont d’abord isolé des exosomes provenant de cellules souches de moelle osseuse de souris et ont confirmé qu’ils présentaient la forme et la taille attendues. Ils ont ensuite montré que ces exosomes étaient facilement ingérés par les cellules endothéliales microvasculaires pulmonaires — les cellules qui tapissent les petits vaisseaux pulmonaires endommagés dans la BPCO.
Les exosomes atténuent les lésions causées par la fumée dans les poumons
Pour reproduire la BPCO liée au tabagisme, l’équipe a exposé des cellules des vaisseaux pulmonaires en culture à un extrait de fumée de cigarette et a mis au point un modèle murin d’emphysème induit par la fumée. Dans les deux systèmes, la fumée augmentait fortement la mort cellulaire dans l’endothélium et provoquait des alvéoles élargies et détruites dans les poumons. Lorsque des exosomes provenant de cellules saines ont été ajoutés, l’équilibre des protéines clés de survie a basculé en faveur de la protection, moins de cellules endothéliales ont subi la mort programmée, et les lésions de type emphysème dans les poumons des souris ont été partiellement inversées. Ces résultats montrent que des facteurs véhiculés par les exosomes de cellules souches saines peuvent protéger directement les vaisseaux pulmonaires et atténuer les lésions structurelles du poumon.
Une boucle génétique circulaire au cœur de la protection
Les chercheurs ont ensuite fouillé le contenu des exosomes pour trouver des différences entre les conditions saines et celles de la BPCO, en se concentrant sur les ARN circulaires, une classe récemment découverte de molécules génétiques stables et en boucle. Parmi près de 14 000 ARN circulaires détectés, l’un nommé circRNA_43350 s’est distingué : il était abondant dans les exosomes et le tissu pulmonaire des souris saines mais fortement réduit chez celles atteintes de BPCO. L’augmentation artificielle des niveaux de circRNA_43350 dans des cellules endothéliales exposées à la fumée a réduit leur taux de mortalité et rétabli un profil plus favorable de protéines de survie. Chez les souris BPCO, l’administration supplémentaire de circRNA_43350 dans les voies respiratoires a atténué les modifications de type emphysème et réduit la mort cellulaire de l’épithélium pulmonaire, indiquant un rôle protecteur central pour cet ARN circulaire.
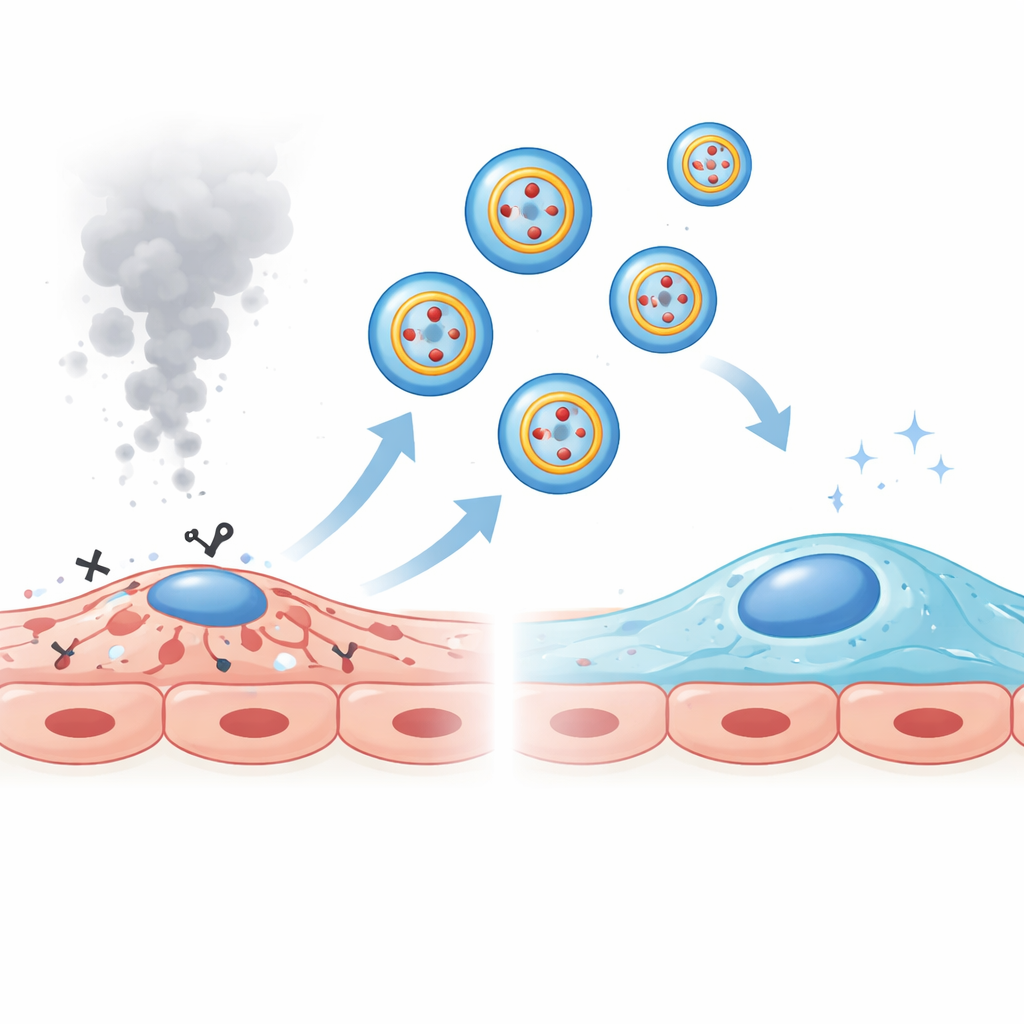
Une éponge moléculaire qui absorbe un signal nuisible
Les ARN circulaires fonctionnent souvent en se liant à de petits ARN régulateurs appelés microARN, les empêchant d’inhiber leurs gènes cibles. À l’aide d’outils de prédiction et de tests rapporteurs moléculaires, l’équipe a montré que circRNA_43350 se lie directement à un microARN nommé miR-342-5p. Chez les patients, chez les souris BPCO et dans les cellules endothéliales traitées par la fumée, les niveaux de miR-342-5p étaient supérieurs à la normale, et le blocage de ce microARN réduisait la mort des cellules endothéliales. Les chercheurs ont démontré que circRNA_43350 et miR-342-5p se restreignent mutuellement : un excès de circRNA_43350 abaisse miR-342-5p et protège les cellules, tandis qu’un excès de miR-342-5p diminue le bénéfice du circRNA_43350 et favorise la mort cellulaire. Cette lutte indique que, lorsque circRNA_43350 est perdu des exosomes dans la BPCO, miR-342-5p est libéré et peut pousser les cellules vasculaires pulmonaires vulnérables vers la lésion.
Ce que cela signifie pour les thérapies futures de la BPCO
Ensemble, ces résultats dessinent un tableau dans lequel des cellules saines de la moelle osseuse envoient des exosomes protecteurs chargés de circRNA_43350 vers les poumons, où cet ARN circulaire neutralise l’excès de miR-342-5p et aide les petits vaisseaux sanguins à survivre au stress induit par la fumée de cigarette. Dans la BPCO, les exosomes contiennent moins de circRNA_43350, affaiblissant ce bouclier et permettant davantage de lésions et le développement d’un emphysème. En identifiant cette boucle microscopique de réparation, ce travail offre une nouvelle voie thérapeutique : des exosomes modifiés ou d’autres traitements visant à restaurer circRNA_43350 ou à freiner miR-342-5p pourraient un jour aider à préserver la structure pulmonaire et la capacité respiratoire des personnes vivant avec la BPCO.
Citation: Zeng, Y., Song, Q., Yang, L. et al. BMSCs exosomes regulate pulmonary microvascular endothelial apoptosis via circRNA_43350/miR-342-5p in COPD. Sci Rep 16, 8183 (2026). https://doi.org/10.1038/s41598-026-39678-y
Mots-clés: BPCO, cellules endothéliales pulmonaires, exosomes de cellules souches mésenchymateuses, ARN circulaire, microARN