Clear Sky Science · fr
Ciblage de types neuronaux spécifiques dans le cerveau de primates non humains à l’aide d’un immunotoxine recombinant murin spécifique de CD25
Pourquoi cette étude cérébrale est importante
Comprendre comment des groupes spécifiques de cellules cérébrales contrôlent le mouvement, les émotions et le comportement est essentiel pour traiter des troubles tels que la maladie de Parkinson et l’autisme. Mais le cerveau est une forêt dense de cellules entrelacées, et la plupart des outils abattent de nombreux arbres à la fois. Cette étude présente une méthode pour éliminer uniquement un type choisi de neurone dans le cerveau d’un singe, avec des dommages collatéraux minimaux, ouvrant la voie à des expériences beaucoup plus précises sur la façon dont des circuits particuliers façonnent le comportement et la maladie.
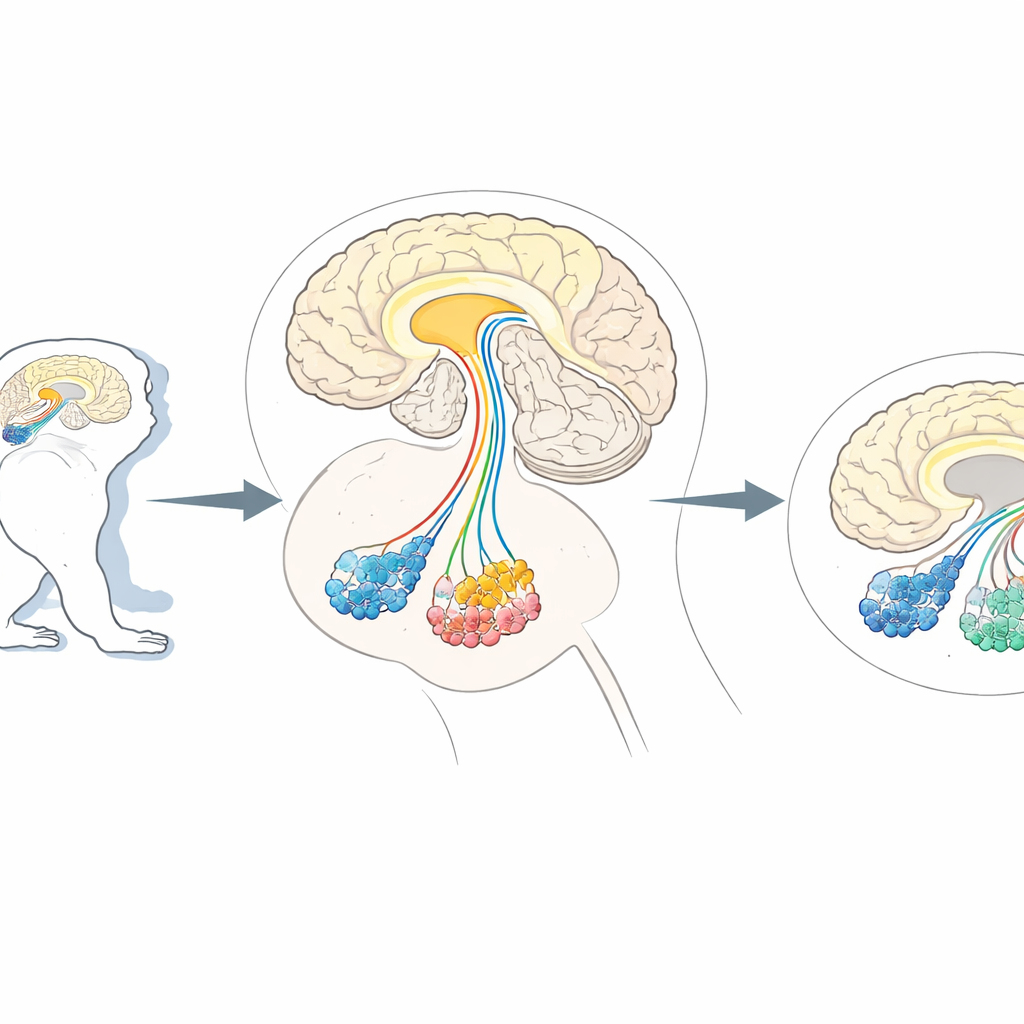
Besoin d’un « élagage » cellulaire précis
Les chercheurs se tournent souvent vers les primates non humains, comme les ouistitis et les macaques, parce que leur organisation cérébrale ressemble beaucoup à la nôtre. Ces animaux sont des modèles précieux pour des affections affectant les fonctions cérébrales supérieures, des troubles parkinsoniens des mouvements aux altérations du comportement social de type autistique. Les méthodes existantes peuvent silencier ou stimuler des voies spécifiques, mais supprimer réellement un seul type de neurone dans ces cerveaux complexes sans nuire aux autres est resté difficile. Des travaux antérieurs chez la souris utilisaient une astuce : des neurones sélectionnés étaient modifiés pour exprimer un marqueur de surface cellulaire appelé CD25, reconnaissable par une toxine conçue qui tue uniquement les cellules marquées. Cependant, ce même marqueur existe naturellement dans le système immunitaire des primates et possiblement dans des cellules cérébrales, ce qui augmente le risque que la toxine attaque des cibles indésirables chez les singes.
Concevoir un scalpel moléculaire plus sûr
Les auteurs se sont donné pour objectif de construire un nouveau scalpel moléculaire adapté à l’usage chez les primates. Plutôt que de cibler la version humaine de CD25, ils se sont concentrés sur la version murine, beaucoup moins similaire au CD25 naturel des singes. Ils ont d’abord immunisé un lapin avec la protéine CD25 murine et utilisé une méthode sur puce pour isoler des cellules de lapin produisant des anticorps qui se lient fortement au CD25 murin mais pas à la forme humaine. Parmi celles-ci, ils ont identifié un anticorps remarquable, appelé RMAb-52, présentant une très forte affinité. Ils ont ensuite assemblé les parties clés de cet anticorps avec un fragment toxique de la bactérie Pseudomonas pour créer une seule protéine immunotoxine ingénierée, nommée anti-mCD25-PE38.
Mettre l’outil à l’épreuve
Dans des expériences en éprouvette, la nouvelle immunotoxine s’est liée au CD25 murin bien plus fortement qu’au CD25 humain, confirmant sa sélectivité. Appliquée à des cellules en culture modifiées pour porter le CD25 murin, la toxine a fortement réduit leur survie à des doses très faibles, tout en laissant indemnes les cellules exprimant le CD25 humain. Ensuite, l’équipe est passée aux ouistitis vivants. À l’aide d’un vecteur viral spécial qui remonte les fibres nerveuses (transport rétrograde), ils ont délivré le gène du CD25 murin dans des neurones producteurs de dopamine qui envoient des signaux d’une région profonde du cerveau appelée la substance noire vers le striatum, une voie cruciale pour le contrôle des mouvements. Après avoir laissé le virus activer l’expression du marqueur dans ces neurones, ils ont injecté la protéine anti-mCD25-PE38 directement dans la zone ciblée du mésencéphale.
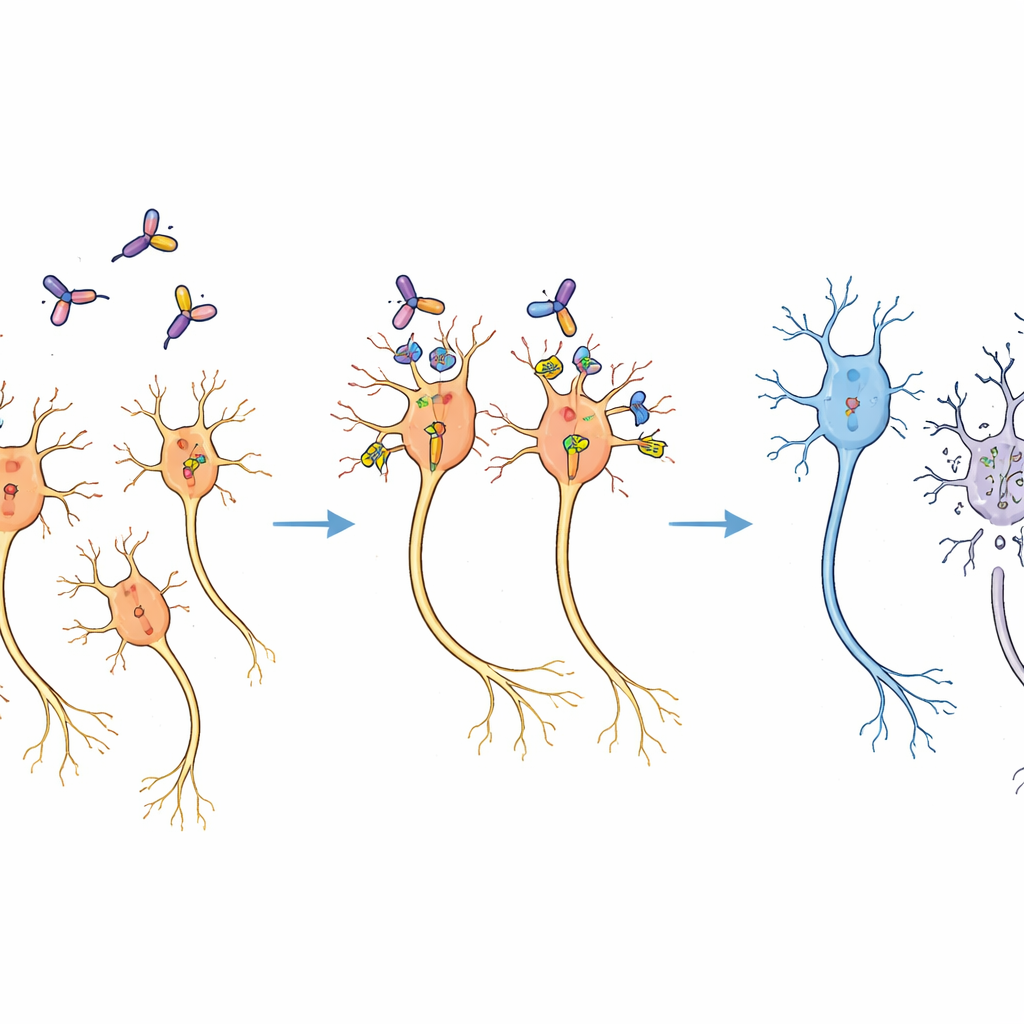
Perte sélective sans dommages étendus
Deux semaines après le traitement, les coupes cérébrales des ouistitis livrent un message clair. Du côté ayant reçu l’immunotoxine, le nombre de neurones dopaminergiques était réduit à environ deux tiers de celui du côté non traité, comme l’ont montré des colorations pour une enzyme de synthèse de la dopamine. Pour autant, les tissus cérébraux environnants semblaient normaux au microscope, et d’autres régions cérébrales ayant reçu le vecteur viral ne présentaient pas de perte cellulaire évidente. Des expériences pilotes avaient déjà établi une plage de doses évitant les lésions tissulaires non spécifiques, et la dose choisie se situait bien dans cette fenêtre de sécurité. Le schéma de perte correspondait à la diffusion attendue du virus et de la toxine, indiquant que les neurones étaient éliminés spécifiquement parce qu’ils avaient été modifiés pour exprimer le CD25 murin, et non parce que la toxine endommageait des cellules de manière indiscriminée.
Ce que cela signifie pour la recherche cérébrale future
Pour un lecteur non spécialiste, le message principal est que les chercheurs ont conçu un bouton de suppression hautement sélectif pour des populations neuronales choisies dans les cerveaux de primates. En combinant un système de délivrance virale rétrograde avec une immunotoxine spécifique de la souris, ils peuvent éliminer des voies définies — par exemple, des circuits dopaminergiques impliqués dans la maladie de Parkinson — tout en épargnant les cellules voisines. Cette stratégie évite les réactions croisées dangereuses avec le CD25 propre de l’animal et devrait être particulièrement utile lorsque ce récepteur naturel est présent ou augmenté dans la maladie. À long terme, cette approche aidera les scientifiques à cartographier comment des voies individuelles dans le câblage cérébral contribuent au mouvement, à la prise de décision et aux symptômes psychiatriques, nous rapprochant de traitements ciblés qui ajustent des circuits défaillants plutôt que d’affecter largement l’ensemble du cerveau.
Citation: Kobayashi, T., Kato, S., Kimura, S. et al. Targeting of specific neuronal types in the non-human primate brain by using a murine CD25-specific recombinant immunotoxin. Sci Rep 16, 8247 (2026). https://doi.org/10.1038/s41598-026-39662-6
Mots-clés: neurosciences des primates non humains, ciblage par immunotoxine, neurones dopaminergiques, circuits cérébraux du ouistiti, modèles de la maladie de Parkinson