Clear Sky Science · fr
Une boîte à outils multimodale chez le poisson zèbre pour étudier la barrière hémato‑encéphalique en santé et en maladie
Pourquoi les vaisseaux cérébraux poreux comptent
Lorsque les vaisseaux sanguins du cerveau ou de l’œil commencent à fuir, du liquide et des protéines s’infiltrent dans le tissu nerveux environnant, provoquant un gonflement qui peut brouiller la vision ou altérer les fonctions cognitives. Ce type « d’engorgement » — appelé œdème vasogénique — intervient dans la perte de vision liée au diabète, l’accident vasculaire cérébral, les traumatismes crâniens et certaines formes de démence. Pourtant, les scientifiques manquent encore de méthodes simples et peu coûteuses pour observer en temps réel la défaillance de cette barrière protectrice. Cette étude présente un modèle polyvalent chez le poisson zèbre qui permet aux chercheurs de voir, mesurer et sonder la façon dont l’hyperglycémie affaiblit la barrière vasculaire cérébrale, accélérant potentiellement la recherche de nouveaux traitements.
Un tout petit poisson avec un avantage clair
Les larves de poisson zèbre offrent une fenêtre unique sur le cerveau vivant. Contrairement aux mammifères, leur corps est transparent en début de vie, et leurs vaisseaux cérébraux peuvent être rendus fluorescents sous le microscope. Les auteurs ont tiré parti de cet avantage en se concentrant sur la barrière hémato‑encéphalique, le joint étanche entre le sang et le tissu cérébral qui ressemble à la barrière hémato‑rétinienne interne protégeant nos yeux. Parce que les mêmes types cellulaires et de nombreuses protéines protectrices sont partagés entre le cerveau et la rétine, l’équipe a utilisé la barrière cérébrale du poisson zèbre comme substitut pour étudier des maladies telles que l’œdème maculaire diabétique et d’autres troubles neurovasculaires, mais dans un système plus rapide, plus éthique et moins coûteux que les modèles traditionnels chez le rongeur.
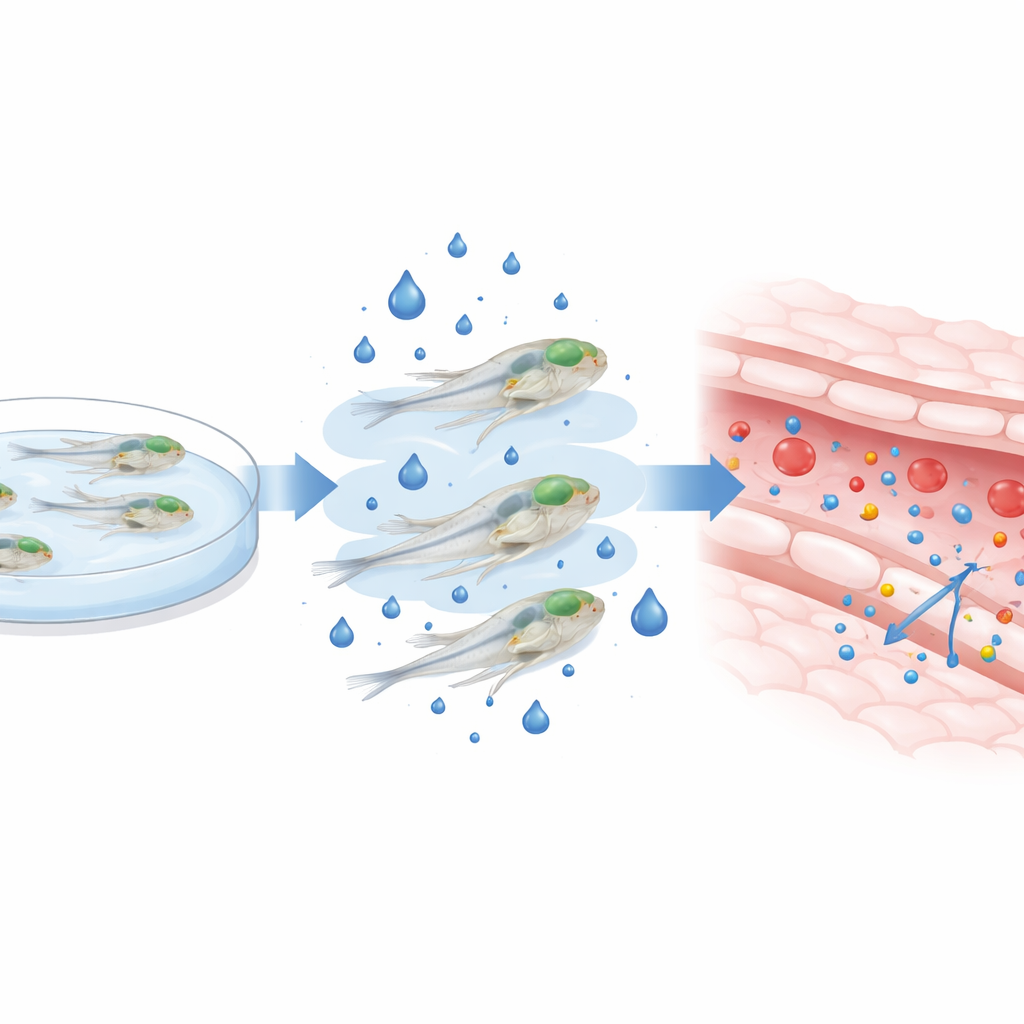
Élever la glycémie chez de jeunes poissons zèbres
Pour reproduire l’hyperglycémie observée dans le diabète, les chercheurs ont élevé des larves de poisson zèbre dans de l’eau contenant un excès de glucose entre trois et cinq jours après la fécondation — une fenêtre critique où la barrière cérébrale est encore en maturation. Ils ont confirmé que ce bain sucré externe augmentait les taux de glucose internes de plusieurs fois sans tuer les larves ni modifier leur morphologie générale. Avec les poissons toujours vivants et nageant, ils ont injecté dans la circulation des colorants fluorescents de différentes tailles et utilisé des microscopes confocaux à haute résolution pour suivre la quantité de colorant qui s’échappait des vaisseaux cérébraux vers le tissu environnant. Après deux jours d’exposition à un glucose élevé, tant les petites que les grosses molécules colorantes ont fui davantage dans le cerveau, particulièrement à la dose de sucre la plus élevée, indiquant que la barrière était devenue plus perméable.
Que se passe‑t‑il au niveau de la paroi vasculaire
Au‑delà de la simple mesure des fuites, l’équipe a construit une « boîte à outils » multimodale pour examiner ce qui déraillait au sein même de la paroi vasculaire. Ils ont mesuré le diamètre d’une artère cérébrale clé et constaté que l’hyperglycémie provoquait une dilatation du vaisseau — un changement précoce également observé chez les personnes atteintes de rétinopathie diabétique. En utilisant des poissons zèbres génétiquement modifiés pour faire briller des protéines spécifiques, ils ont montré que le glucose élevé réduisait les niveaux de claudine‑5, un composant majeur des jonctions serrées entre cellules vasculaires voisines, et augmentait les niveaux de PLVAP, une protéine associée aux vaisseaux immatures et susceptibles de fuir qui transportent des matériaux à travers la couche cellulaire. La microscopie électronique, capable de révéler des structures à l’échelle nanométrique, a confirmé un élargissement subtil aux jonctions entre cellules, bien que les petites cavités de transport appelées cavéoles aient été trop rares pour être quantifiées de manière fiable lors de cette première analyse.
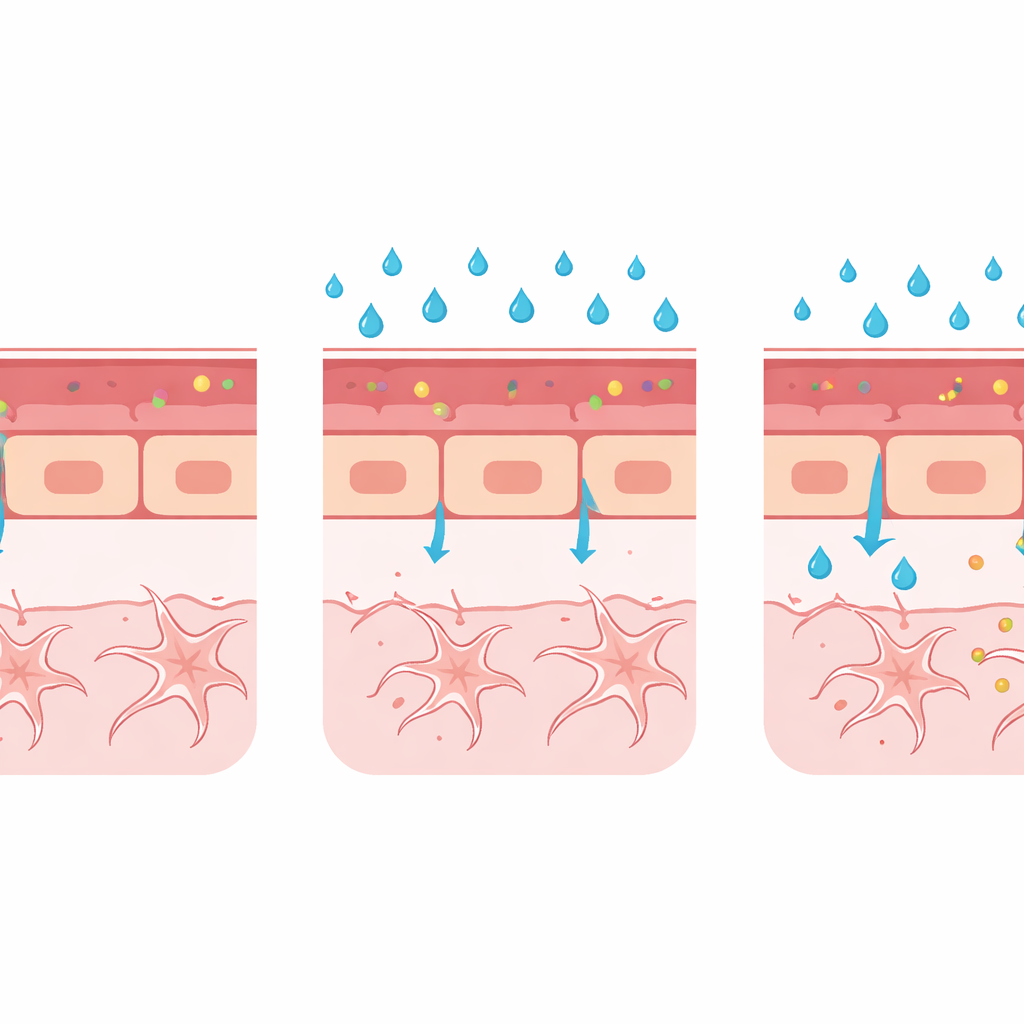
Une plateforme flexible pour la recherche future sur les maladies
Dans l’ensemble, ces changements — augmentation des fuites de colorant, vaisseaux élargis, jonctions cellulaires affaiblies et augmentation de PLVAP — dessinent un tableau cohérent : l’hyperglycémie peut retarder ou perturber la formation correcte de la barrière dans le cerveau en développement. Le modèle ne reproduit pas encore la rupture d’une barrière pleinement mature, comme celle observée dans les maladies humaines chroniques, mais il excelle pour montrer comment des conditions nocives pendant le développement peuvent empêcher la barrière de se sceller correctement. Parce que les techniques sont compatibles avec une gamme de lignées rapporteurs fluorescentes et d’imagerie avancée, la même plateforme peut être étendue pour étudier d’autres déclencheurs de défaillance de la barrière, tels que des molécules inflammatoires, des cellules de soutien altérées comme les péricytes et les cellules gliales, ou des perturbations de voies de signalisation clés.
Ce que cela signifie pour les patients
Pour les non‑spécialistes, le message central est que ce travail fournit un terrain d’essai vivant, pratique, pour observer la défaillance de la paroi protectrice du cerveau sous stress, en utilisant de petits poissons transparents plutôt que de plus grands mammifères. En suivant en temps réel comment l’hyperglycémie remodèle la structure et la fonction des vaisseaux, les chercheurs peuvent plus rapidement identifier quelles molécules et quels types cellulaires cibler pour préserver l’intégrité de la barrière. À terme, de telles connaissances pourraient orienter le développement de nouveaux médicaments ou stratégies thérapeutiques pour prévenir ou réduire les fuites de liquide dans les yeux et le cerveau — contribuant ainsi à préserver la vision et à protéger les fonctions cognitives des personnes atteintes de diabète et d’autres maladies neurovasculaires.
Citation: Bakker-van Bugnum, N., Snijders, E.E., Hogendorp, E.F. et al. A zebrafish multimodal toolbox to study the blood-brain barrier in health and disease. Sci Rep 16, 9422 (2026). https://doi.org/10.1038/s41598-026-39616-y
Mots-clés: barrière hémato‑encéphalique, modèle poisson zèbre, complications du diabète, fuite vasculaire, maladie neurovasculaire