Clear Sky Science · fr
Caractérisation génomique et in vitro de deux bactériophages lytique infectant la souche multi‑résistante Erwinia sp. AnSW2-5
Pourquoi les bactéries qui ravagent les cultures nous concernent tous
Partout dans le monde, les agriculteurs luttent contre des maladies bactériennes qui font pourrir les fruits, flétrir les feuilles et dévaster les récoltes. De nombreuses épidémies sont désormais causées par des souches qui ne répondent plus aux antibiotiques courants, menaçant à la fois l’approvisionnement alimentaire et les moyens de subsistance qui en dépendent. Cette étude explore une alternative émergente : l’utilisation de virus qui attaquent les bactéries, appelés bactériophages, pour neutraliser en toute sécurité un agent pathogène végétal particulièrement tenace trouvé dans un sol associé à un usage intensif d’antibiotiques.
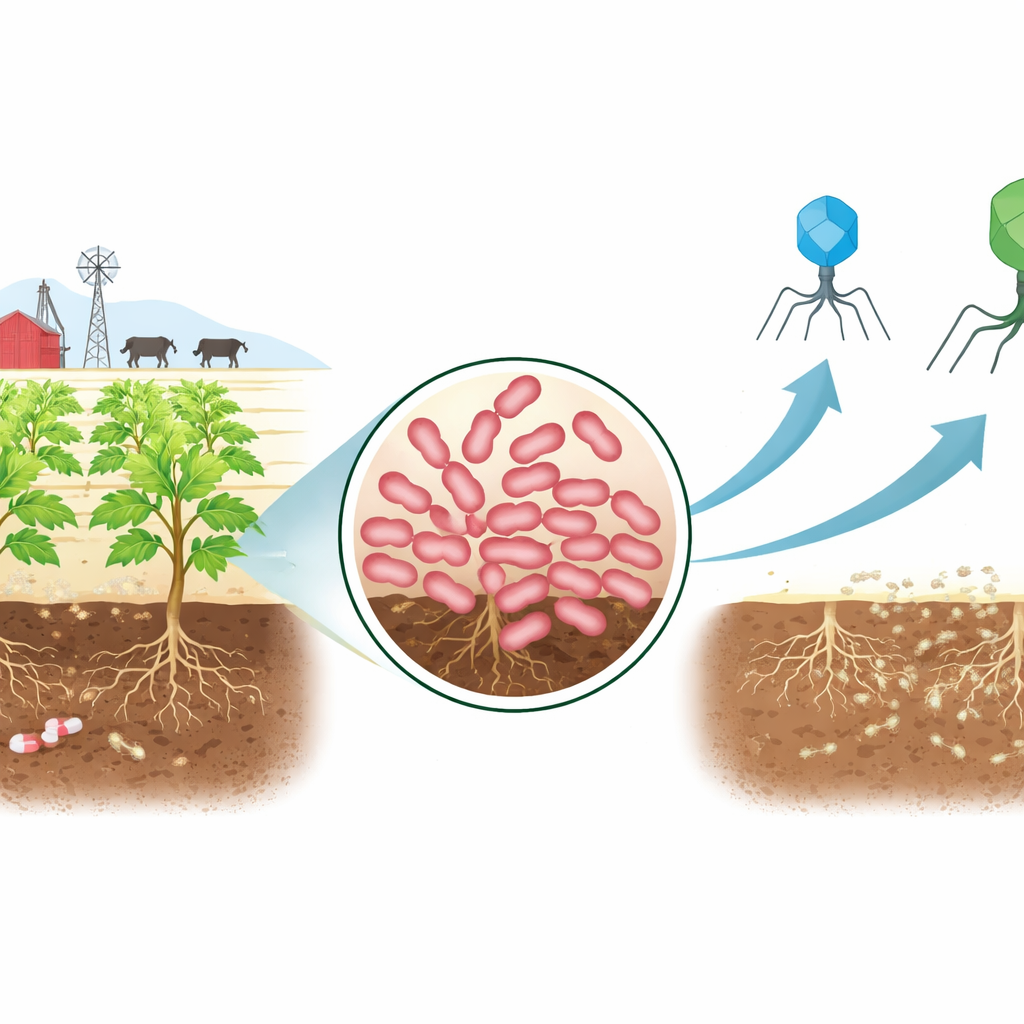
Un nouvel envahisseur coriace dans la ferme
Les chercheurs ont commencé par prélever des échantillons de sol dans un enclos à bovins connu pour recevoir des déchets d’élevage et des antibiotiques. De cet environnement exigeant, ils ont isolé une souche d’Erwinia, un groupe bactérien qui comprend des responsables notoires de la brûlure bactérienne des pommiers et de la pourriture molle des pommes de terre. Les tests ont montré que cette souche, nommée AnSW2-5, résistait à plusieurs grandes familles d’antibiotiques, y compris des médicaments utilisés contre un large éventail d’infections. L’analyse génétique a confirmé la raison : son ADN porte plusieurs gènes de résistance connus et des pompes moléculaires puissantes qui expulsent les antibiotiques de la cellule. Parallèlement, les comparaisons de génomes ont révélé que cette souche est distincte des espèces d’Erwinia décrites précédemment, ce qui en fait un modèle utile pour étudier le contrôle de nouveaux agents pathogènes végétaux difficiles à traiter.
Deux minuscules prédateurs aux forces différentes
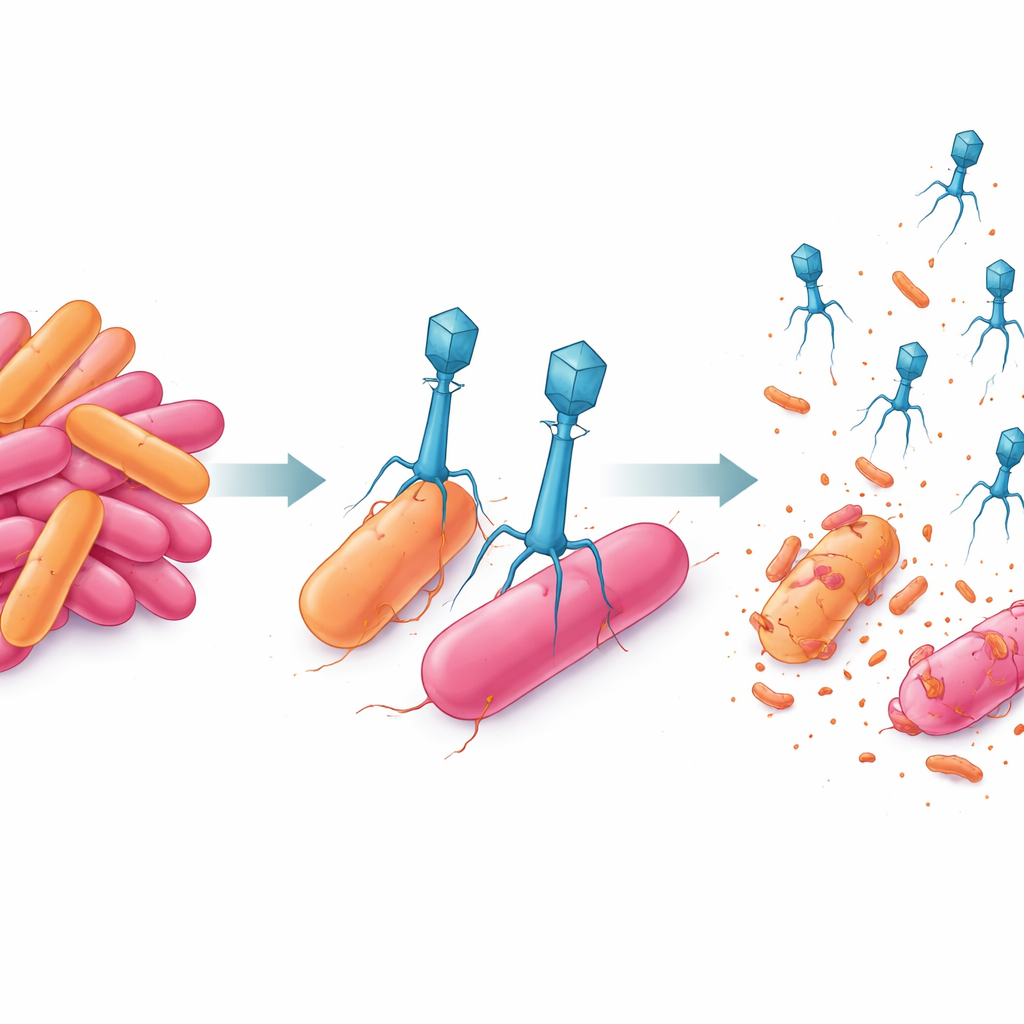
Pour trouver des ennemis naturels de cette bactérie multi‑résistante, l’équipe s’est tournée vers de l’eau douce prélevée sur le même site et l’a enrichie en bactériophages capables d’infecter AnSW2-5. Ils ont isolé deux candidats prometteurs, désignés P‑A et P‑K. Au microscope électronique, P‑A apparaissait compact avec une queue courte, une morphologie associée à une infection rapide et directe. P‑K, en revanche, présentait une queue contractile plus longue avec une structure de base complexe, suggérant une manière plus puissante de percer son hôte. Le séquençage de leurs génomes a montré que les deux phages sont strictement lytique : ils envahissent, se répliquent et font éclater la cellule, plutôt que de s’intégrer discrètement dans l’ADN bactérien. Pourtant, ils le font avec des boîtes à outils génétiques très différentes — le génome épuré de P‑A favorise une attaque rapide, tandis que le génome plus volumineux de P‑K code pour une machinerie structurale et de réplication plus élaborée.
Comment l’équipe virale attaque
Lorsque les scientifiques ont suivi le cycle de vie de chaque phage en laboratoire, ils ont constaté que P‑A frappe rapidement : il ne lui faut qu’environ 20 minutes avant l’apparition de nouvelles particules virales, et chaque bactérie infectée libère environ 70 descendants. P‑K met plus de temps — environ 35 minutes avant de commencer à produire de nouveaux phages — mais chaque cellule infectée produit près de 110 nouvelles particules. Dans des tests en co‑culture où bactéries et phages évoluent ensemble pendant trois jours, chaque phage pris isolément ralentissait la croissance bactérienne mais ne l’empêchait pas complètement. Les bactéries ont finalement repris du terrain, reflétant l’apparition de survivants résistants. Cependant, lorsque P‑A et P‑K ont été combinés en un seul cocktail, ils ont réduit la population bactérienne de plus de 80 % et l’ont maintenue supprimée pendant l’ensemble des 72 heures de l’expérience.
Empêcher la résistance de prendre pied
Une des observations les plus marquantes concernait l’effet de la paire de phages sur l’émergence de mutants résistants. Lorsqu’elles étaient exposées à P‑A ou P‑K seuls, une petite fraction de bactéries — approximativement une sur un million à une sur dix millions — parvenait à échapper et à se développer malgré l’attaque des phages. Mais lorsque les deux phages étaient utilisés ensemble, les colonies résistantes sont devenues si rares qu’elles sont tombées en dessous de la limite de détection de l’expérience. Cela suggère que les deux virus ciblent probablement des éléments différents à la surface bactérienne ou perturbent la cellule de manières complémentaires. Pour qu’une seule bactérie survive, elle devrait surmonter les deux à la fois, un événement pratiquement impossible. En termes pratiques, cela rend le cocktail beaucoup plus robuste face aux astuces évolutives qui condamnent souvent les antibiotiques.
Ce que cela pourrait signifier pour les récoltes futures
Pris dans leur ensemble, les résultats montrent que des paires soigneusement choisies de bactériophages peuvent faire plus que simplement réduire des bactéries végétales dangereuses — elles peuvent aussi limiter la capacité des bactéries à évoluer vers la résistance. En combinant un phage d’action rapide avec un autre qui produit un nombre plus élevé de descendants, les chercheurs ont créé une équipe virale qui a contrôlé une souche d’Erwinia multi‑résistante pendant plusieurs jours tout en empêchant l’apparition de variants détectables. Bien que ces essais aient été menés en laboratoire plutôt que dans des vergers ou des champs, ils ouvrent la voie à un avenir où des mélanges ciblés de phages feraient partie de la gestion intégrée des ravageurs, aidant les agriculteurs à protéger les cultures avec une dépendance beaucoup moindre aux antibiotiques traditionnels.
Citation: Baek, K., Goh, J. & Choi, A. Genomic and in vitro characterization of two lytic bacteriophages infecting multidrug-resistant Erwinia sp. strain AnSW2-5. Sci Rep 16, 8172 (2026). https://doi.org/10.1038/s41598-026-39563-8
Mots-clés: biocontrôle par bactériophages, maladies bactériennes des plantes, résistance aux antibiotiques en agriculture, thérapie par phages pour Erwinia, cocktails de phages