Clear Sky Science · fr
Nouveaux conjugués benzimidazole‑alkanesulfonate comme inhibiteurs des cholinestérases avec validation in vitro et in silico
Pourquoi cette recherche importe pour la mémoire et le vieillissement
La maladie d’Alzheimer érode lentement la mémoire, l’autonomie et la qualité de vie de millions de personnes dans le monde ; les traitements actuels soulagent surtout les symptômes sans freiner véritablement les lésions sous‑jacentes. Cette étude explore une nouvelle famille de molécules synthétiques conçues pour mieux protéger un messager cérébral clé impliqué dans l’apprentissage et la mémoire, tout en combattant le stress oxydatif nocif. En combinant des éléments de plusieurs classes médicamenteuses efficaces au sein d’une seule structure, les chercheurs cherchent à se rapprocher de traitements plus performants contre la maladie d’Alzheimer.
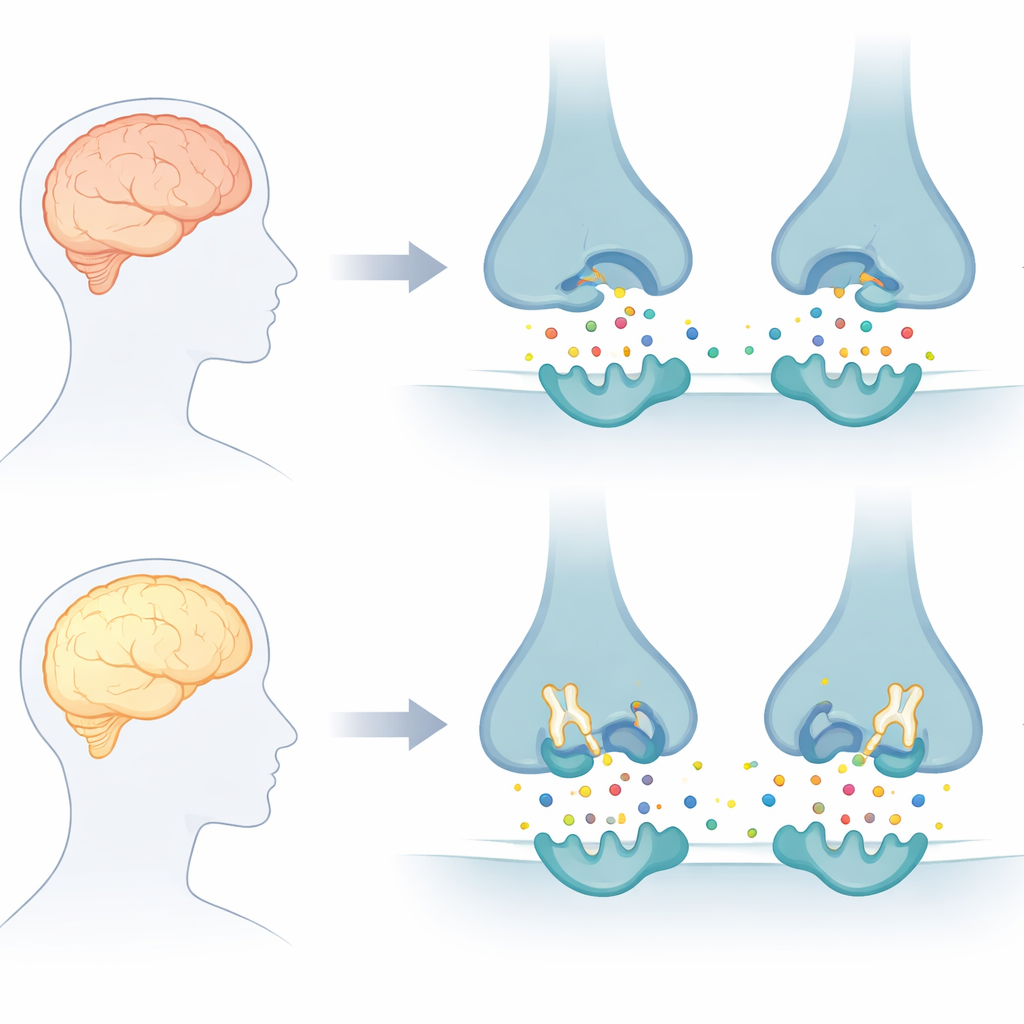
Le signal cérébral qui s’éteint trop vite
Les cellules cérébrales en bonne santé communiquent grâce à des messagers chimiques, dont l’un des plus importants est l’acétylcholine. Dans la maladie d’Alzheimer, l’acétylcholine est dégradée trop rapidement par deux enzymes, l’acétylcholinestérase et la butyrylcholinestérase, ce qui contribue aux pertes de mémoire et à la confusion. Les médicaments actuels ciblent principalement une seule de ces enzymes et n’agissent que temporairement, d’où un soulagement à court terme plutôt qu’une protection durable. Les auteurs de cet article se sont donc concentrés sur la conception d’inhibiteurs « doubles » capables de cibler les deux enzymes simultanément et de donner potentiellement plus de temps à l’acétylcholine pour remplir son rôle.
Construire une clé moléculaire plus intelligente
Pour élaborer ces inhibiteurs doubles, l’équipe a utilisé une stratégie appelée hybridation moléculaire : elle a assemblé des fragments issus de trois familles de blocs chimiques déjà connus pour interagir favorablement avec les cholinestérases. Ces portions comprenaient un noyau benzimidazole fréquent dans les médicaments, un groupe sulfonate capable de se lier fortement aux poches enzymatiques, et un linker hydrazone qui relie les parties avec une certaine flexibilité. Le résultat est une série de composés apparentés, désignés 4a à 4r, dont les structures ont été soigneusement confirmées par des techniques chimiques standard telles que la spectroscopie infrarouge et la résonance magnétique nucléaire.
Tester l’inhibition enzymatique et le pouvoir antioxydant
Les nouveaux composés ont d’abord été dépistés en éprouvette pour évaluer leur capacité à ralentir les deux cholinestérases. La plupart des membres de la série ont montré des effets inhibiteurs modérés à forts, mais cinq d’entre eux — 4b, 4h, 4i, 4q et 4r — se sont distingués par leur capacité à inhiber l’acétylcholinestérase. Lorsque les chercheurs ont déterminé des valeurs de puissance plus précises, plusieurs de ces molécules ont égalé voire dépassé le donépézil, l’un des médicaments de référence prescrits contre l’Alzheimer. L’équipe a aussi évalué si les meilleurs inhibiteurs enzymatiques pouvaient neutraliser les radicaux libres, ces molécules instables qui endommagent les cellules cérébrales. Les composés 4q et 4r ont montré une activité antioxydante particulièrement forte dans plusieurs tests, atteignant ou dépassant les performances de la vitamine C de référence.
Observer la serrure enzymatique
Comme ces expériences ont été réalisées hors du corps, les scientifiques ont eu recours à la modélisation informatique pour prédire le comportement possible des molécules en tant que médicaments. À l’aide d’outils in silico largement utilisés, ils ont estimé les propriétés d’absorption, de distribution et de métabolisme, puis simulé l’ajustement des composés dans la structure tridimensionnelle de l’acétylcholinestérase. Les études de docking suggèrent que la portion benzimidazole de chaque molécule se loge près de l’ouverture externe de l’enzyme, tandis que l’extrémité portant le sulfonate s’étend profondément vers le centre catalytique où l’acétylcholine est normalement dégradée. Notamment, 4q et 4r ont formé plusieurs interactions stabilisantes à l’intérieur de la poche enzymatique et ont montré une force de liaison calculée supérieure à celle du donépézil, en accord avec leurs bonnes performances en éprouvette.
Ce que cela signifie pour les futurs traitements de l’Alzheimer
Pris ensemble, ces résultats montrent que cette nouvelle classe de conjugués benzmidazole‑alkanesulfonate peut inhiber fortement l’acétylcholinestérase, présenter des propriétés antioxydantes utiles et se lier à sa cible enzymatique d’une manière cohérente avec les principes actuels de conception de médicaments. Bien que ces molécules soient encore loin d’être prêtes pour une utilisation clinique — elles n’ont pas encore été testées chez l’animal ou l’humain — elles offrent une esquisse prometteuse pour des traitements de nouvelle génération combinant inhibition enzymatique et protection contre le stress oxydatif. Avec des raffinements et des tests biologiques complémentaires, certains membres de cette famille pourraient un jour contribuer à des médicaments qui préservent mieux la mémoire et les fonctions cognitives du cerveau vieillissant.
Citation: Omar, M.A., Al-Ashmawy, A.A.K., Abd El Salam, H.A. et al. New benzimidazole-alkanesulfonate conjugates as cholinesterase inhibitors with in vitro and in silico validation. Sci Rep 16, 8946 (2026). https://doi.org/10.1038/s41598-026-39534-z
Mots-clés: Maladie d’Alzheimer, inhibiteurs de l’acétylcholinestérase, dérivés de benzimidazole, composés antioxydants, conception de médicaments