Clear Sky Science · fr
Modélisation structurale et analyse par docking des mutations non-sens et canoniques associées à la résistance chez Escherichia coli soudanais
Pourquoi cela compte pour la santé quotidienne
Les infections résistantes aux antibiotiques ne sont plus des curiosités médicales rares ; elles menacent de plus en plus les traitements de routine des infections urinaires, des interventions chirurgicales et des soins intensifs. Cette étude examine de près des bactéries Escherichia coli provenant du Soudan et pose une question précise : comment de petits changements génétiques dans des protéines bactériennes modifient-ils l’action des antibiotiques courants ? En employant la modélisation structurale assistée par ordinateur plutôt que des expériences de laboratoire coûteuses, les auteurs mettent au jour des schémas de résistance discrets que les tests standards et les bases de données mondiales peuvent manquer — en particulier dans les contextes à ressources limitées où la résistance augmente le plus rapidement. 
Examen de la boîte à outils bactérienne
Les chercheurs se sont concentrés sur les mutations « missense » — des substitutions d’une seule lettre d’ADN qui remplacent un acide aminé par un autre dans une protéine. Ils ont analysé des génomes complets de 55 isolats d’E. coli collectés au Soudan et se sont focalisés sur les protéines bactériennes cibles directes des grandes classes d’antibiotiques, notamment les fluoroquinolones, les macrolides et la rifampicine. Ces cibles comprennent des enzymes qui enroulent l’ADN (gyrase et topoisomérase IV), le ribosome responsable de la synthèse protéique, et l’ARN polymérase. Sur 71 mutations trouvées dans ces protéines, 19 ont été signalées par plusieurs outils de prédiction comme susceptibles d’altérer la fonction protéique, et, de façon remarquable, la plupart semblaient être des variations nouvelles non encore répertoriées dans les bases de données mondiales de résistance.
Nouveaux points sensibles dans des cibles familières
Certaines des modifications les plus importantes se sont regroupées dans une protéine ribosomale appelée L22, qui contribue à former le tunnel par lequel les protéines fraîchement synthétisées sortent du ribosome. Cette région sert aussi de site de fixation pour les macrolides comme l’érythromycine. L’étude a identifié un ensemble dense de mutations de L22 jusque-là non rapportées, nombreuses au sein d’une même souche, qui se situent le long de ce tunnel et aux points de contact avec l’ARN ribosomique. Les analyses informatiques suggèrent que plusieurs de ces changements déstabilisent la structure locale ou la rendent plus flexible, ce qui pourrait remodeler le tunnel et faire en sorte que les molécules de macrolides s’y ajustent moins bien. Parallèlement, des mutations de résistance « canoniques » plus connues sont apparues dans les protéines de traitement de l’ADN ParC et ParE ainsi que dans l’ARN polymérase, confirmant que les souches soudanaises partagent certains marqueurs mondiaux de résistance tout en possédant leurs propres particularités locales.
Comment les changements de forme affaiblissent l’accrochage des antibiotiques
L’équipe est allée au-delà des simples listes de séquences pour interroger la manière dont ces mutations pourraient modifier l’ajustement tridimensionnel entre les antibiotiques et leurs cibles. Grâce à des simulations de docking moléculaire, ils ont comparé la fixation des différents médicaments sur les protéines normales et mutées. Pour la topoisomérase IV ParC, des mutations clés proches du site de contact avec le médicament ont considérablement affaibli la liaison prédite de la fluoroquinolone trovafloxacine, reflétant une prise plus lâche au niveau de la jonction enzyme–ADN–médicament. Dans la protéine voisine ParE, des mutations ont réduit de façon modeste la liaison de la novobiocine. En revanche, une mutation nouvelle dans la gyrase GyrA semble déstabiliser la structure de l’enzyme sans modifier de façon notable l’affinité de la fluoroquinolone moxifloxacine, ce qui suggère que la résistance peut parfois émerger en perturbant subtilement la performance enzymatique plutôt qu’en expulsant simplement le médicament. 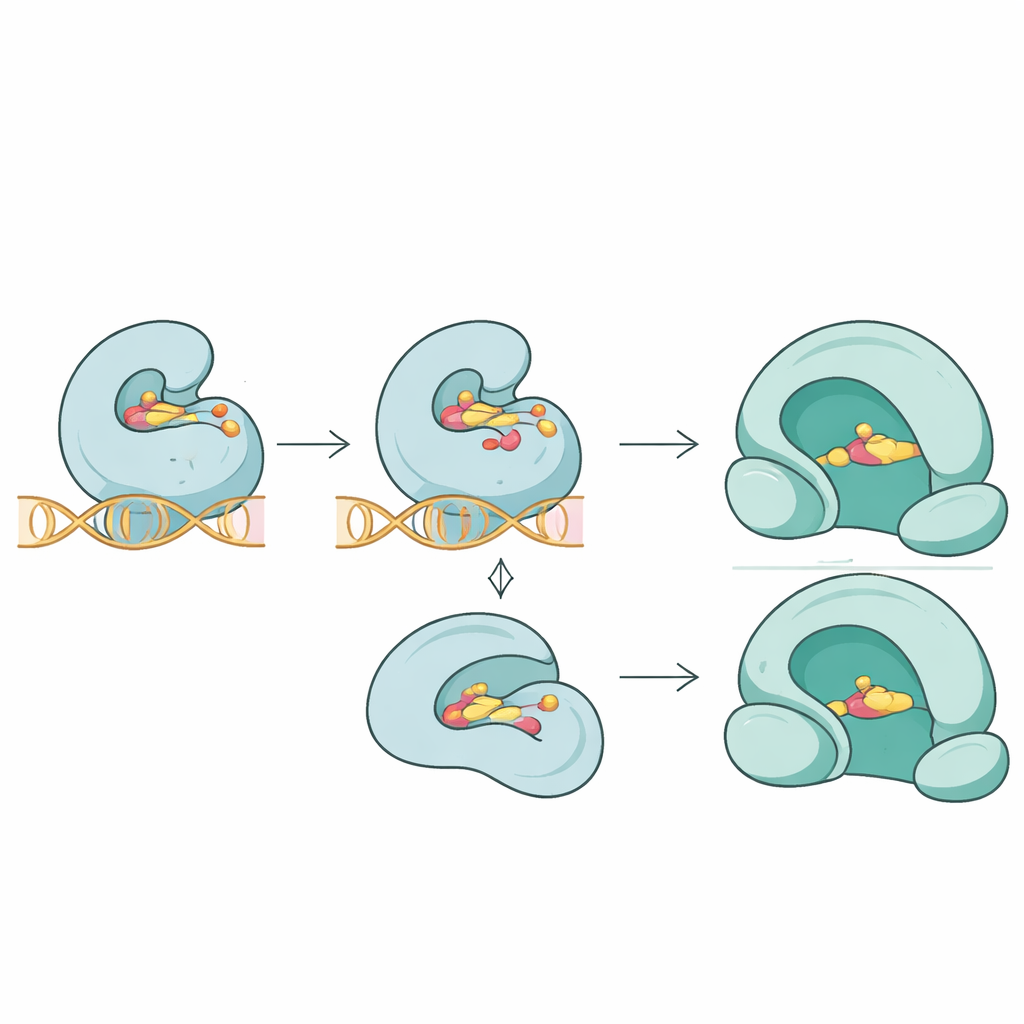
Effets mixtes selon les médicaments
Toutes les mutations n’ont pas eu le même impact. Les modifications classiques conférant une résistance à la rifampicine dans la protéine RpoB de l’ARN polymérase ont peu perturbé la liaison d’un inhibiteur plus récent et structurellement distinct qui cible un site voisin, suggérant que des médicaments futurs pourraient être conçus pour contourner les schémas de résistance existants. Pour la protéine ribosomale L22, les études de docking avec l’érythromycine ont révélé un ensemble d’issues hétérogènes : certaines mutations ont affaibli la liaison, d’autres ont eu peu d’effet, et l’une a même légèrement amélioré l’ajustement prédit. Ces résultats soulignent que la résistance est rarement totale ou inexistante ; chaque mutation influe différemment sur la stabilité protéique, la flexibilité et la fixation du médicament, et l’effet global sur le traitement dépend de la façon dont ces changements se combinent dans une cellule bactérienne vivante.
Ce que cela signifie pour les patients et la surveillance
Pour le grand public, le message clé est que les bactéries dans des régions comme le Soudan évoluent vers la résistance par des voies à la fois bien connues et moins documentées. Les voies bien connues impliquent des mutations classiques déjà suivies par les programmes internationaux, mais cette étude montre que de nombreuses mutations supplémentaires, enrichies localement, peuvent aussi affaiblir les antibiotiques de façons plus subtiles. En cartographiant ces changements sur des structures protéiques détaillées, les auteurs fournissent une courte liste de mutations qui devraient être testées en laboratoire et prises en compte dans des panels diagnostiques régionaux. Concrètement, leur travail plaide pour que la modélisation informatique intelligente aide les pays à capacité de laboratoire limitée à mieux suivre l’émergence de la résistance, soutenant en fin de compte des choix thérapeutiques plus fiables et inspirant la conception de médicaments capables de garder une longueur d’avance sur l’évolution bactérienne.
Citation: Sage, E.E., Ibrahim, S.A.E., Firdaus-Raih, M. et al. Structural modeling and docking analysis of canonical and novel resistance-associated missense mutations in Sudanese Escherichia coli. Sci Rep 16, 8995 (2026). https://doi.org/10.1038/s41598-026-39491-7
Mots-clés: résistance aux antimicrobiens, Escherichia coli, mutations non-sens, bioinformatique structurale</keyword:> <keyword>Soudan