Clear Sky Science · fr
Impact de la chimiothérapie néoadjuvante sur la fonctionnalité des cellules stromales mésenchymateuses dérivées du tissu adipeux et leurs effets modulateurs sur les fibroblastes chez des patients en oncologie
Pourquoi cela compte pour les survivants du cancer
De nombreuses personnes ayant reçu un traitement contre le cancer rencontrent par la suite des problèmes de cicatrisation lente et des complications après chirurgie. Parallèlement, les médecins explorent de plus en plus l’utilisation des cellules réparatrices dérivées de la propre graisse du patient pour aider à la récupération des tissus. Cette étude pose une question pratique et urgente : après une chimiothérapie, ces cellules réparatrices sont-elles encore utilisables, et si ce n’est pas le cas, quelles cellules sont réellement les plus affectées ?
Les réparateurs cachés du corps
Le tissu adipeux n’est pas qu’un réservoir d’énergie. Il abrite une population riche de cellules réparatrices polyvalentes appelées cellules stromales mésenchymateuses dérivées du tissu adipeux, ou CSMA-TAd. Ces cellules ne restent pas inactives : elles libèrent un mélange de molécules de signalisation qui peuvent apaiser l’inflammation, stimuler la formation de nouveaux vaisseaux sanguins et encourager les cellules voisines à croître et reconstruire le tissu endommagé. Juste au‑dessus de la graisse, dans la peau, se trouvent les fibroblastes — des cellules opératrices qui migrent dans les plaies et déposent du collagène, l’échafaudage protéique qui confère de la résistance au tissu neuf. Ensemble, les CSMA-TAd et les fibroblastes déterminent en grande partie la capacité de la peau à récupérer après une blessure ou une intervention chirurgicale.
Tester les cellules réparatrices issues de la graisse avant et après traitement
Les chercheurs ont prélevé de petits échantillons de peau et de graisse chez 66 patients subissant une intervention chirurgicale, certains ayant reçu une chimiothérapie au préalable et d’autres non. À partir de la graisse, ils ont isolé les CSMA-TAd et confirmé que ces cellules conservaient l’apparence et le comportement attendus des cellules réparatrices : elles présentaient les marqueurs de surface caractéristiques et pouvaient se différencier en cellules de type osseux, cartilagineux et adipeux en laboratoire. À partir de la peau, ils ont isolé des fibroblastes. L’équipe a ensuite comparé la croissance, le cycle cellulaire, la sécrétion de molécules de signalisation et l’expression des gènes liés à la cicatrisation et à la régénération des CSMA-TAd et des fibroblastes exposés ou non à la chimiothérapie.
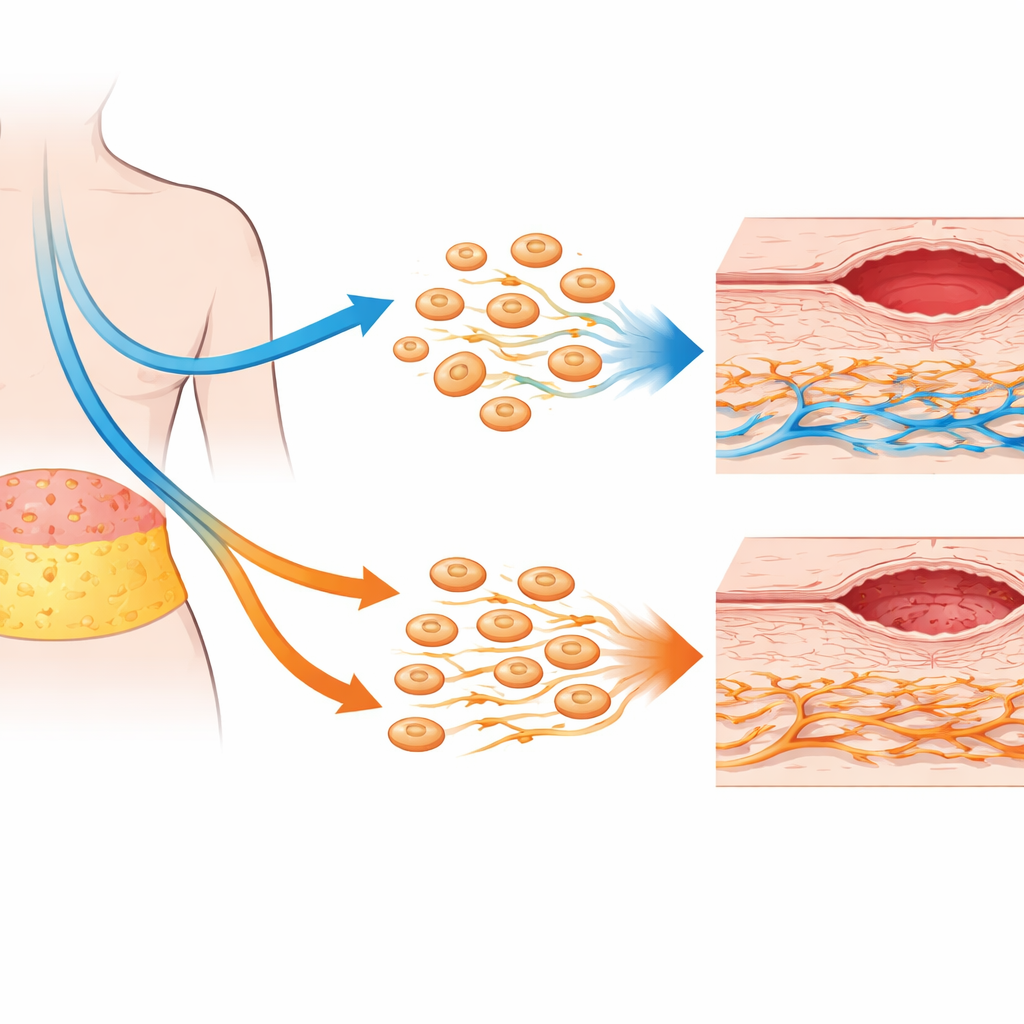
Les cellules réparatrices adipeuses restent étonnamment robustes
Contrairement aux craintes selon lesquelles la chimiothérapie pourrait diminuer l’efficacité des CSMA-TAd, l’étude a montré que ces cellules dérivées de la graisse sont remarquablement résistantes. Leurs marqueurs d’identité de base, leur mode de croissance et leur profil de protéines sécrétées restaient en grande partie inchangés après chimiothérapie. L’activité génique liée à la croissance, l’auto-renouvellement et la réparation des plaies présentait seulement de petits changements non significatifs. En fait, les CSMA-TAd provenant de patients traités par chimiothérapie affichaient une activité mitochondriale légèrement plus élevée, laissant entrevoir un métabolisme plus robuste plutôt que des dommages. Dans des expériences en co‑culture — où CSMA-TAd et fibroblastes partageaient le même milieu sans contact direct — les CSMA-TAd stimulaient toujours certains comportements des fibroblastes, comme le mouvement dirigé vers des signaux de réparation, surtout dans les échantillons de patients n’ayant pas reçu de chimiothérapie.
Les bâtisseurs cutanés subissent les effets principaux de la chimiothérapie
Le tableau était très différent pour les fibroblastes. Les cellules prélevées sur la peau de patients traités par chimiothérapie présentaient des signes clairs de vigueur biologique réduite. Leur capacité à migrer dans une « plaie » simulée par une rayure sur une plaque de culture était significativement diminuée et leur production de collagène avait tendance à être plus faible. Le profil des molécules de signalisation qu’elles libéraient évoluait vers un état plus inflammatoire et moins régénératif, et de nombreux gènes associés aux signaux de croissance, à leurs récepteurs et au potentiel régénératif étaient réduits. Même lorsque ces fibroblastes étaient co‑cultivés avec leurs propres CSMA-TAd, la plupart de leurs fonctions — migration, production de collagène et expression génique favorable — restaient atténuées par rapport aux fibroblastes issus de patients n’ayant pas reçu de chimiothérapie.
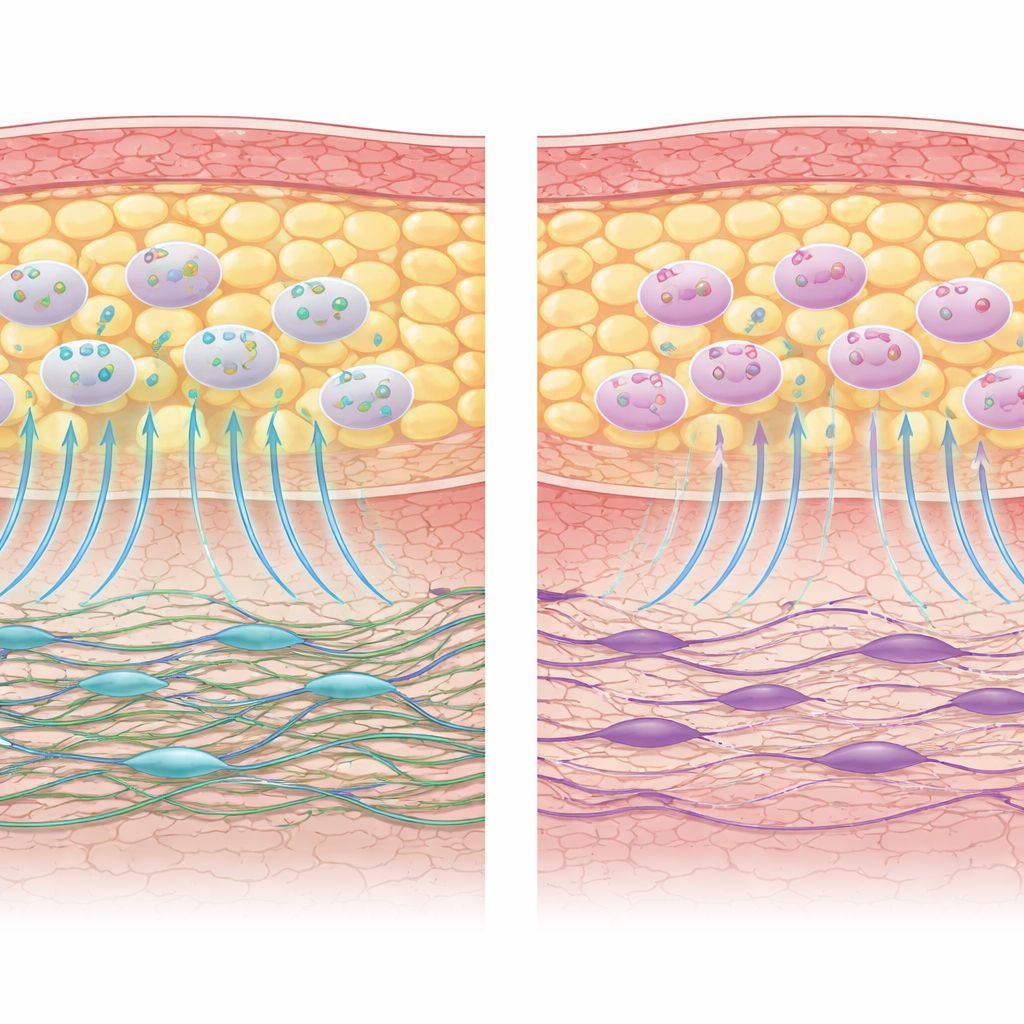
Ce que cela implique pour les thérapies de cicatrisation futures
Pour un non-spécialiste, le message de ce travail est que la chimiothérapie ne semble pas anéantir le réservoir de cellules réparatrices d’origine graisseuse de l’organisme, mais qu’elle laisse les constructeurs de première ligne de la peau — les fibroblastes — moins aptes à intervenir rapidement dans les plaies et à reconstruire un tissu solide. Parce que les CSMA-TAd restent fonctionnellement intactes, elles demeurent des candidates prometteuses pour des procédures reconstructrices, la prise en charge des plaies et les greffes de graisse après un traitement du cancer. Toutefois, l’état altéré des fibroblastes pourrait limiter l’efficacité que ces cellules de type souches peuvent apporter seules. Les auteurs suggèrent que les thérapies futures devront peut‑être soutenir les deux côtés du partenariat réparateur : préserver ou restaurer la santé des fibroblastes tout en exploitant des CSMA-TAd robustes, idéalement dans des modèles plus complexes et proches du corps qui capturent mieux l’environnement réel de cicatrisation chez les survivants du cancer.
Citation: Skoniecka, A., Słonimska, P., Tymińska, A. et al. Impact of neoadjuvant chemotherapy on the functionality of adipose-derived mesenchymal stromal cells and their modulatory effects on fibroblasts in oncology patients. Sci Rep 16, 8614 (2026). https://doi.org/10.1038/s41598-026-39457-9
Mots-clés: chimiothérapie, cicatrisation, cellules souches dérivées du tissu adipeux, fibroblastes, médecine régénérative