Clear Sky Science · fr
Analyse du génome entier du CVA4 chez des enfants atteints d’herpangine dans deux villes du Shandong, Chine
Pourquoi cette infection de la gorge chez l’enfant compte
Les parents connaissent peut‑être l’herpangine comme une angine brève mais pénible qui renvoie les enfants de la crèche à la maison. Pourtant, derrière ces petites vésicules se cache une famille de virus en évolution rapide. Cette étude suit l’un de ces virus, le Coxsackievirus A4 (CVA4), chez des enfants de deux villes de la province du Shandong, en Chine, afin de comprendre comment il se propage, comment sa composition génétique évolue dans le temps et ce que cela peut signifier pour de futures épidémies et pour les vaccins.
Un regard plus précis sur un virus fréquent chez les enfants
L’herpangine et la maladie main‑pied‑bouche, plus connue, sont toutes deux causées par des entérovirus qui infectent principalement les jeunes enfants. Les symptômes sont généralement bénins — fièvre, mal de gorge et petites ulcérations au fond de la bouche — mais certains virus apparentés peuvent parfois provoquer des complications graves comme des méningites. Ces dernières années, le CVA4 est apparu comme l’un des principaux responsables de l’herpangine en Asie de l’Est, bien qu’il ait attiré beaucoup moins d’attention que d’autres virus pédiatriques. Pour combler cette lacune, les chercheurs ont prélevé en 2024 des écouvillonnages de gorge sur 256 enfants atteints d’herpangine dans les villes de Linyi et Yantai, isolant 60 virus CVA4 et séquençant intégralement le génome de 50 d’entre eux.
Lire l’empreinte génétique du virus
Le CVA4 est un petit virus à ARN avec une longue séquence unique d’acide nucléique qui code à la fois pour les protéines formant sa coque externe et pour la machinerie lui permettant de se répliquer. En comparant les séquences d’un gène clé de la coque externe (appelé VP1) des échantillons du Shandong à des centaines de CVA4 collectés dans le monde depuis 1948, l’équipe a constaté que tous les nouveaux virus appartiennent à une branche connue sous le nom de sous‑génotype C2, devenue la forme dominante en circulation à l’échelle mondiale. Lorsque les génomes complets ont été analysés avec plus de 170 génomes CVA4 publiés antérieurement, toutes les souches du Shandong se sont regroupées au sein d’un grand groupe évolutif contenant la plupart des virus chinois récents, suggérant une circulation locale intense avec un certain regroupement régional.
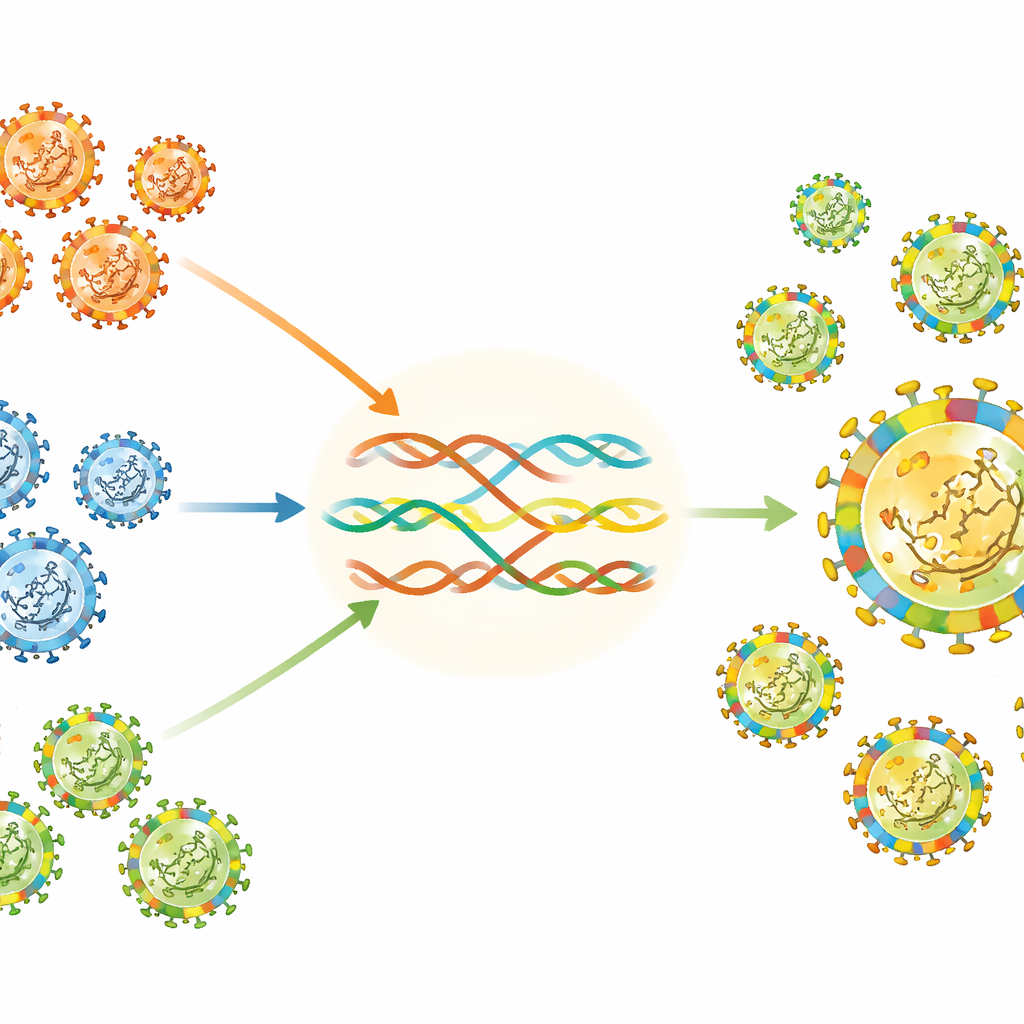
Comment les virus s’échangent des fragments de génome
Les virus à ARN comme le CVA4 n’accumulent pas seulement lentement des mutations aléatoires ; ils peuvent aussi recombiner — échanger des tronçons de matériel génétique lorsque deux virus apparentés infectent la même cellule. Pour rechercher ces événements de « mix‑and‑match », les auteurs ont comparé différentes régions génomiques de leurs échantillons de CVA4 avec celles de plusieurs entérovirus apparentés. Dans la portion codant la coque externe du virus, les souches du Shandong ressemblaient le plus au « prototype » historique du CVA4, ce qui renforce l’idée que cette région est relativement stable et reste une base fiable pour classer les souches. Mais dans les régions codant des enzymes internes, notamment une portion appelée 3D qui aide à copier le génome viral, certaines souches de CVA4 ressemblaient soudainement à d’autres entérovirus.
Preuves d’« hybrides » viraux
En utilisant des logiciels spécialisés pour détecter la recombinaison, l’équipe a identifié trois événements clairs où des parties du génome du CVA4 semblent avoir été acquises auprès de cousins appelés CVA2 et CVA8. Cinq virus du Shandong partageaient un court segment dans la région 3D identique à celui du CVA2, ce qui implique qu’un virus hybride précoce s’est propagé avec succès dans la population locale. Une souche, nommée LY17, était encore plus complexe : elle portait deux fragments importés distincts, l’un le plus similaire au CVA8 et l’autre au CVA2, tous deux localisés dans la région 3D. Ces réarrangements soulignent que l’évolution du CVA4 n’est pas linéaire mais implique des remaniements génétiques répétés dans un « point chaud » spécifique de sa machinerie de réplication.
Ce que cela signifie pour les familles et la santé publique
L’étude ne prétend pas que ces changements génétiques ont déjà rendu le CVA4 plus dangereux, mais elle met en évidence l’évolution active du virus pendant sa circulation chez les enfants. Étant donné que les vaccins actuellement utilisés en Chine ciblent un autre entérovirus, EV‑A71, d’autres virus comme le CVA4 jouent désormais un rôle plus important dans les épisodes quotidiens d’herpangine et d’affections apparentées. En cartographiant les relations entre les souches de CVA4 dans le monde et en identifiant les régions où elles recombinent avec d’autres virus, ce travail fournit une feuille de route génétique pour la surveillance future et la conception de vaccins. Pour les familles, le message principal est que même les infections infantiles habituelles sont animées par des virus dynamiques, et qu’une surveillance soutenue aide les autorités sanitaires à anticiper et atténuer l’impact de nouvelles vagues épidémiques.
Citation: Ma, W., Dong, Z., Mou, X. et al. Whole-genome analysis of CVA4 in children with herpangina in two cities of Shandong, China. Sci Rep 16, 7881 (2026). https://doi.org/10.1038/s41598-026-39455-x
Mots-clés: herpangine, Coxsackievirus A4, entérovirus, recombinaison virale, infection pédiatrique