Clear Sky Science · fr
Découverte de composés antiviraux potentiels et accélération de la recherche thérapeutique contre le virus de la variole du singe
Pourquoi cette recherche est importante maintenant
La variole du singe, désormais souvent appelée mpox, est passée d’une infection tropicale rare à une préoccupation mondiale, avec des foyers signalés sur plusieurs continents ces dernières années. Contrairement au COVID-19, il n’existe toujours pas de médicament spécifiquement conçu pour arrêter ce virus. Cette étude utilise des outils informatiques avancés pour rechercher de nouvelles petites molécules susceptibles de neutraliser le virus là où il est le plus dangereux : sa capacité à se cacher du système immunitaire. Si ces candidats sont confirmés en laboratoire, ils pourraient constituer le point de départ d’une nouvelle classe de médicaments antiviraux.
Comment le virus échappe à nos défenses
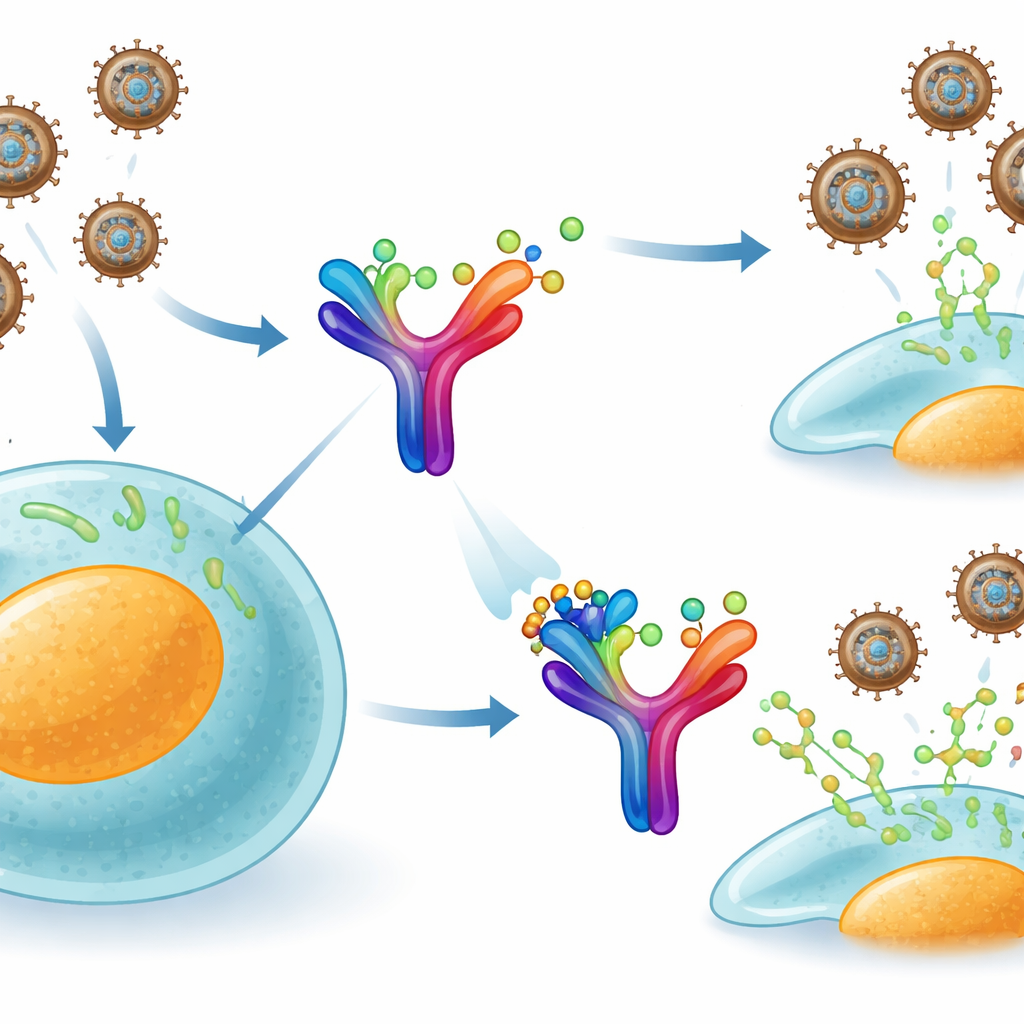
La variole du singe appartient à la même famille élargie que la variole et utilise une astuce ingénieuse pour éviter le système immunitaire. Nos cellules libèrent une protéine de signalisation appelée interféron-gamma, qui avertit normalement les cellules voisines et active des défenses antivirales. Le virus, en revanche, produit sa propre protéine sécrétée, appelée B8R, qui flotte à l’extérieur des cellules infectées. B8R mime étroitement notre récepteur de l’interféron-gamma et capture ces signaux immunitaires avant qu’ils n’atteignent leur véritable cible. En pratique, il agit comme une éponge, absorbant les messages d’alerte du corps et empêchant une réponse antivirale complète.
Utiliser l’informatique pour concevoir des traitements plus intelligents
La découverte de médicaments traditionnelle peut prendre de nombreuses années et mobiliser des ressources considérables. Ici, les chercheurs ont recours à la conception assistée par ordinateur pour accélérer le processus. Comme il n’existe pas de structure 3D expérimentale de la protéine B8R, ils ont d’abord utilisé des outils basés sur AlphaFold pour prédire sa forme atomique et ont soigneusement vérifié la qualité de ce modèle. Munis d’une structure 3D fiable, ils ont procédé à un criblage virtuel d’une bibliothèque chimique de 5 000 petites molécules. Des règles décrivant ce qui fait habituellement un médicament « pilule » (taille, forme et solubilité) ont servi à éliminer les mauvais candidats, laissant 2 890 composés prometteurs pour des tests détaillés contre le modèle de la protéine B8R.
Identifier une « clé » chimique prometteuse
L’étape suivante consistait à voir quelles molécules pouvaient s’insérer précisément dans une poche importante à la surface de B8R, là où elle interagit normalement avec l’interféron-gamma. L’équipe a utilisé le docking moléculaire, une technique qui teste des milliards de positions possibles pour une molécule dans la poche de la protéine et évalue la force de liaison. Trois candidats principaux ont émergé, chacun étant prévu pour former des interactions fortes avec des acides aminés clés du site. Un composé en particulier a montré la meilleure énergie de liaison et a établi plusieurs contacts stabilisants avec des résidus critiques qui contribuent à l’ancrer en place, ce qui suggère qu’il pourrait être particulièrement efficace pour bloquer l’activité de B8R.
Observer le mouvement des molécules dans le temps
Les protéines et les molécules médicamenteuses ne sont pas rigides ; elles bougent, fléchissent et « respirent » dans un environnement aqueux. Pour tenir compte de cela, les chercheurs ont réalisé de longues simulations de dynamique moléculaire — des films virtuels durant des centaines de nanosecondes — pour observer le comportement de chaque paire protéine–composé au fil du temps. Ces simulations ont montré que le composé le plus performant restait profondément enfoui dans la poche de B8R, la protéine s’ajustant légèrement autour de lui tout en restant structurellement stable. En revanche, les deux autres composés erraient davantage, migraient vers des poches alternatives ou montraient des fluctuations plus importantes, ce qui indique une liaison plus faible ou moins fiable. Des analyses supplémentaires de flexibilité, d’énergie et de mouvements à grande échelle ont toutes convergé vers le même gagnant : un composé qui produisait de manière cohérente le complexe le plus stable et le plus favorable énergétiquement.
Ce que cela pourrait signifier pour les traitements futurs
L’étude ne prétend pas avoir découvert un médicament fini, et aucune expérience sur des cellules ou des animaux n’a encore été réalisée. Elle fournit néanmoins un point de départ solide et fondé sur les données : une petite molécule spécifique qui semble idéalement façonnée pour se verrouiller dans la protéine B8R de la variole du singe et potentiellement rétablir le système d’alerte de l’interféron de l’organisme. En ciblant la stratégie d’évasion immunitaire du virus plutôt que sa machinerie de réplication, cette approche offre un angle nouveau pour la thérapie antivirale. Les auteurs soutiennent que leur composé principal devrait maintenant être testé en laboratoire, où sa capacité à bloquer B8R et à réduire l’infection par le mpox pourra être mesurée directement. Si ces essais sont concluants, cela pourrait ouvrir la voie à un traitement ciblé aidant le système immunitaire à détecter et stopper le virus plus efficacement.
Citation: Ahmad, F., Navid, A., Irfan, M. et al. Discovery of potential antiviral compounds and accelerating the therapeutic discovery against monkeypox virus. Sci Rep 16, 8306 (2026). https://doi.org/10.1038/s41598-026-39427-1
Mots-clés: antiviral variole du singe, évasion immunitaire, découverte de médicaments, modélisation informatique, signalisation de l’interféron