Clear Sky Science · fr
Optimisation des monocytes THP-1-CAR utilisant la phagocytose médiée par le signalement CD32a pour l’activation antigène-spécifique des lymphocytes T
Apprendre de nouvelles astuces au système immunitaire
Les thérapies cellulaires modernes reprogramment déjà les cellules immunitaires pour traquer le cancer, mais la plupart reposent sur les lymphocytes T, qui peinent parfois à opérer dans l’environnement hostile des tumeurs solides. Cette étude se tourne plutôt vers un autre défenseur puissant — les macrophages, les « mangeurs » professionnels de l’organisme — et s’interroge sur la manière de les reconfigurer pour qu’ils non seulement ingèrent plus efficacement les cellules nuisibles ou les virus, mais aussi recrutent les lymphocytes T pour une attaque ciblée et durable. Les travaux révèlent des règles de conception pour construire de meilleurs macrophages à récepteur antigénique chimérique (CAR) pouvant s’appliquer aussi bien aux infections comme la COVID-19 qu’aux tumeurs solides difficiles à traiter.
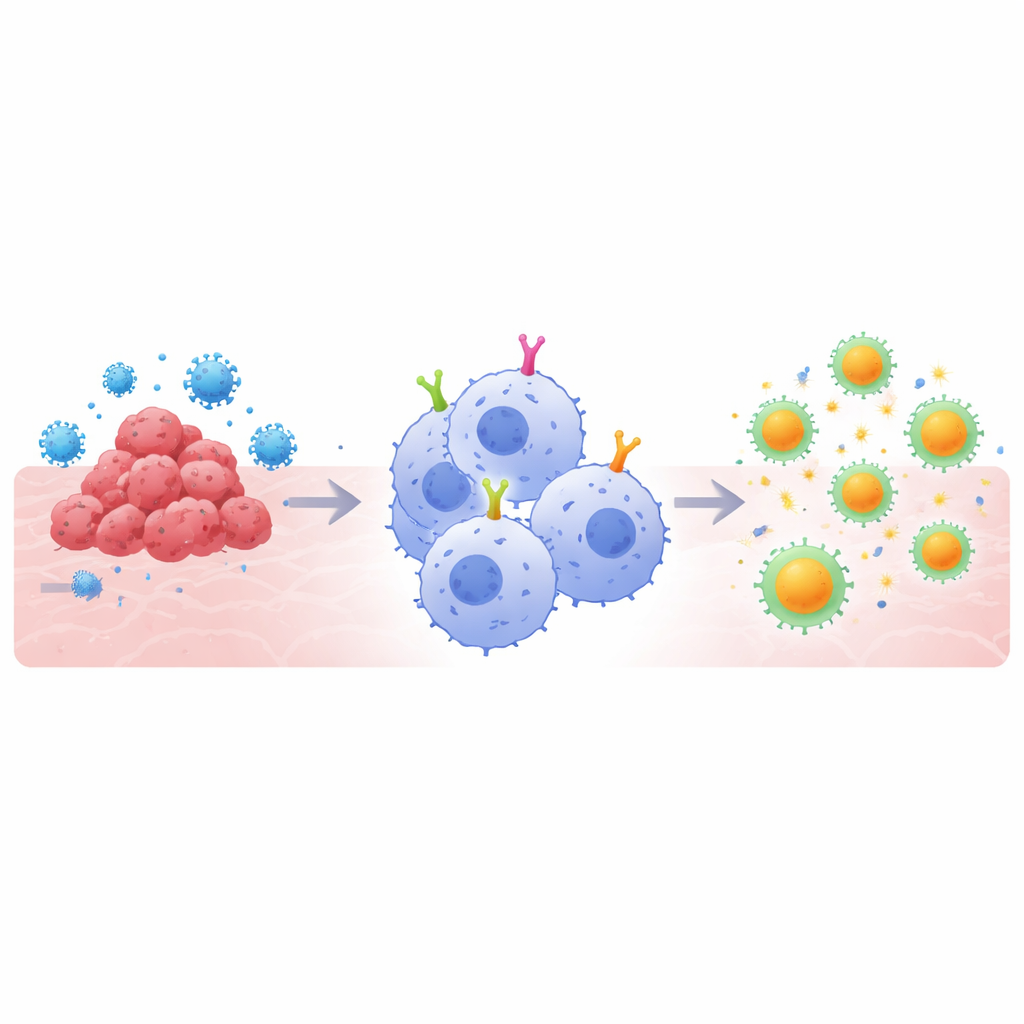
Pourquoi les super-mangeurs sont importants
Les thérapies basées sur les CAR fonctionnent en dotant les cellules immunitaires de récepteurs de surface sur mesure qui reconnaissent une cible choisie, comme une protéine tumorale ou la protéine de spicule d’un virus. Les versions basées sur les lymphocytes T ont transformé le traitement de certains cancers du sang, mais elles affrontent des obstacles contre les tumeurs solides et dans certaines infections. Les macrophages offrent un angle différent : ils engloutissent naturellement les menaces et les décomposent en fragments présentables aux lymphocytes T, faisant le lien entre les bras « inné » et « adaptatif » de l’immunité. Cependant, la plupart des conceptions de CAR ont été initialement développées pour les lymphocytes T, pas pour les macrophages. Les auteurs ont donc supposé que, pour exploiter pleinement les atouts des macrophages, les domaines de signalisation internes des CAR — les segments qui indiquent à la cellule quoi faire une fois la cible liée — devaient être adaptés spécifiquement à ces cellules mangeuses.
Trouver le meilleur câblage interne
L’équipe a comparé systématiquement plusieurs domaines de signalisation internes insérés dans des CAR introduits dans une lignée de monocytes humains (THP‑1) pouvant être différenciés en macrophages. Ils se sont concentrés sur des domaines issus de récepteurs qui pilotent normalement la phagocytose et l’inflammation : CD3ζ (le module classique des cellules T), CD32a (un récepteur qui se lie aux cibles recouvertes d’anticorps), les composants du CR3 CD11b et CD18 (récepteurs du complément clés), et TLR4 (un senseur du danger microbien). À l’aide de billes et de pseudovirus recouverts de la protéine de spicule du SARS‑CoV‑2, ils ont mesuré dans quelle mesure chaque conception de CAR permettait aux cellules d’ingérer des cibles, de produire des molécules inflammatoires, puis d’activer des lymphocytes T CD8 humains ayant déjà été exposés au virus. Ils ont ensuite transféré les conceptions les plus prometteuses dans des CAR ciblant la mésothéline, une protéine surexprimée dans de nombreuses tumeurs solides, pour vérifier si les mêmes règles s’appliquaient en contexte tumoral.
Construire de meilleurs mangeurs et amplificateurs de signal
Un schéma clair est apparu : les CAR basés sur CD32a déclenchaient systématiquement une phagocytose plus forte et plus rapide que ceux utilisant le domaine conventionnel CD3ζ, malgré le fait que CD3ζ comporte davantage des motifs d’activation habituels. Autrement dit, « l’adéquation » entre le signal et la machinerie du macrophage importait plus que la simple intensité du signal. L’ajout d’éléments dérivés du CR3 (CD11b ou CD18) en plus de CD32a n’augmentait pas davantage la capacité d’ingestion dans la plupart des conditions, mais élevait les niveaux de cytokines inflammatoires clés comme le TNF‑α et l’IL‑1β. Les combinaisons contenant TLR4 allaient encore plus loin pour renforcer les signaux inflammatoires et le marqueur de surface CD86, associé à la capacité de stimuler les lymphocytes T, quoique avec des compromis : des niveaux plus faibles de CAR à la surface cellulaire et une phagocytose quelque peu réduite.
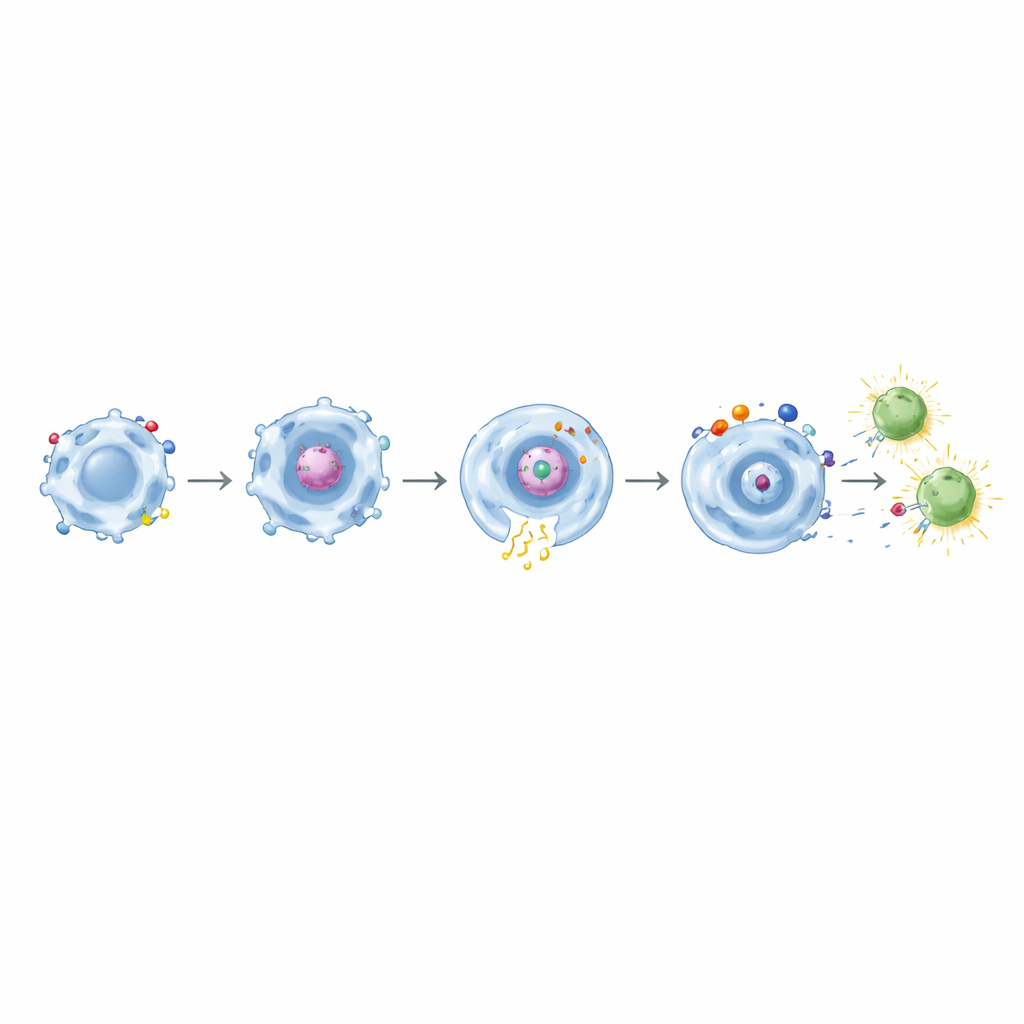
De la consommation à l’enseignement des lymphocytes T
De manière cruciale, après que des macrophages portant des CAR à base de CD32a eurent ingéré la protéine de spicule, ils furent capables d’activer des lymphocytes T CD8 mémoires de personnes précédemment vaccinées contre la COVID‑19. Ces lymphocytes T ont exprimé des marqueurs d’activation précoces et produit des molécules effectrices telles que l’interféron‑γ et le TNF‑α. L’effet devenait encore plus prononcé avec des CAR à domaines doubles associant CD32a à CD11b, CD18 ou TLR4. Lorsque des conceptions similaires ciblant la mésothéline furent testées contre des cellules tumorales modifiées, elles montrèrent à nouveau une phagocytose précise dépendante de la cible combinée à une signalisation inflammatoire accrue. Parmi celles-ci, la combinaison CD32a+TLR4 se distingua comme une puissante « alarme tissulaire », augmentant le mieux la sécrétion de cytokines et l’expression de CD86 tout en maintenant une ingestion tumorale spécifique.
Ce que cela pourrait signifier pour les traitements futurs
Pour un observateur non spécialiste, cette étude montre que l’ingénierie des macrophages n’est pas un problème universel. En échangeant et en combinant des modules de signalisation internes, les chercheurs peuvent façonner des cellules qui se concentrent soit sur le nettoyage efficace des cellules malades, soit sur le rôle d’amplificateurs immunitaires qui remodelent l’environnement suppressif d’une tumeur et recrutent des lymphocytes T. Les CAR à base de CD32a se sont révélés une solide base pour de telles conceptions, surpassant les modules traditionnels des cellules T dans les macrophages et fonctionnant à la fois contre des cibles virales et tumorales. Bien que ces résultats proviennent de modèles de laboratoire et devront être confirmés dans des cellules humaines primaires et chez l’animal, ils fournissent une feuille de route pour des thérapies CAR macrophages de nouvelle génération capables de mieux s’attaquer aux tumeurs solides et aux infections persistantes en unissant ingestion rapide et activation précise des lymphocytes T.
Citation: Hong, J., Lee, S., Kim, Y. et al. Optimization of THP-1-CAR monocytes utilizing CD32a signaling phagocytosis for antigen-specific T cell activation. Sci Rep 16, 8175 (2026). https://doi.org/10.1038/s41598-026-39406-6
Mots-clés: macrophages CAR, signalisation CD32a, phagocytose, immunothérapie des tumeurs solides, activation des lymphocytes T