Clear Sky Science · fr
FAM120A - une protéine intégrée au réseau moléculaire de la maladie ALS
Pourquoi cela compte pour les personnes et les familles
La sclérose latérale amyotrophique (SLA) est une maladie dévastatrice qui paralyse lentement les personnes en détruisant les cellules nerveuses qui contrôlent le mouvement. Aujourd'hui, nous ne comprenons toujours pas complètement pourquoi ces neurones moteurs meurent, et les traitements efficaces restent rares. Cette étude met en lumière une protéine peu connue, appelée FAM120A, et suggère qu'elle pourrait aider les cellules nerveuses à faire face au stress et à prévenir l'accumulation d'amas protéiques nocifs — une caractéristique de la SLA. En révélant le comportement de cette protéine pendant la maladie, ce travail ouvre une nouvelle voie pour comprendre, et peut‑être un jour traiter, la SLA.
Découvrir un acteur caché dans un réseau génique dense
Les chercheurs n'ont pas commencé au banc de laboratoire mais à l'ordinateur. Ils ont utilisé une approche d'« analyse convergente » pour combiner de nombreux jeux de données existants sur les gènes liés à la SLA et leurs interactions. Cette vision en réseau leur a permis d'identifier des grappes de protéines qui travaillent ensemble dans des processus cellulaires clés, en particulier ceux liés au traitement de l'ARN et au contrôle de la qualité des protéines — deux points sensibles connus dans la SLA. Au sein d'une de ces grappes, FAM120A est apparue comme une protéine jusqu'alors négligée mais fortement connectée, interagissant avec plusieurs protéines déjà impliquées dans la SLA. Ses rôles connus dans l'aide à la survie cellulaire face au stress oxydatif et dans la gestion de l'ARN en faisaient une candidate solide pour des études complémentaires.
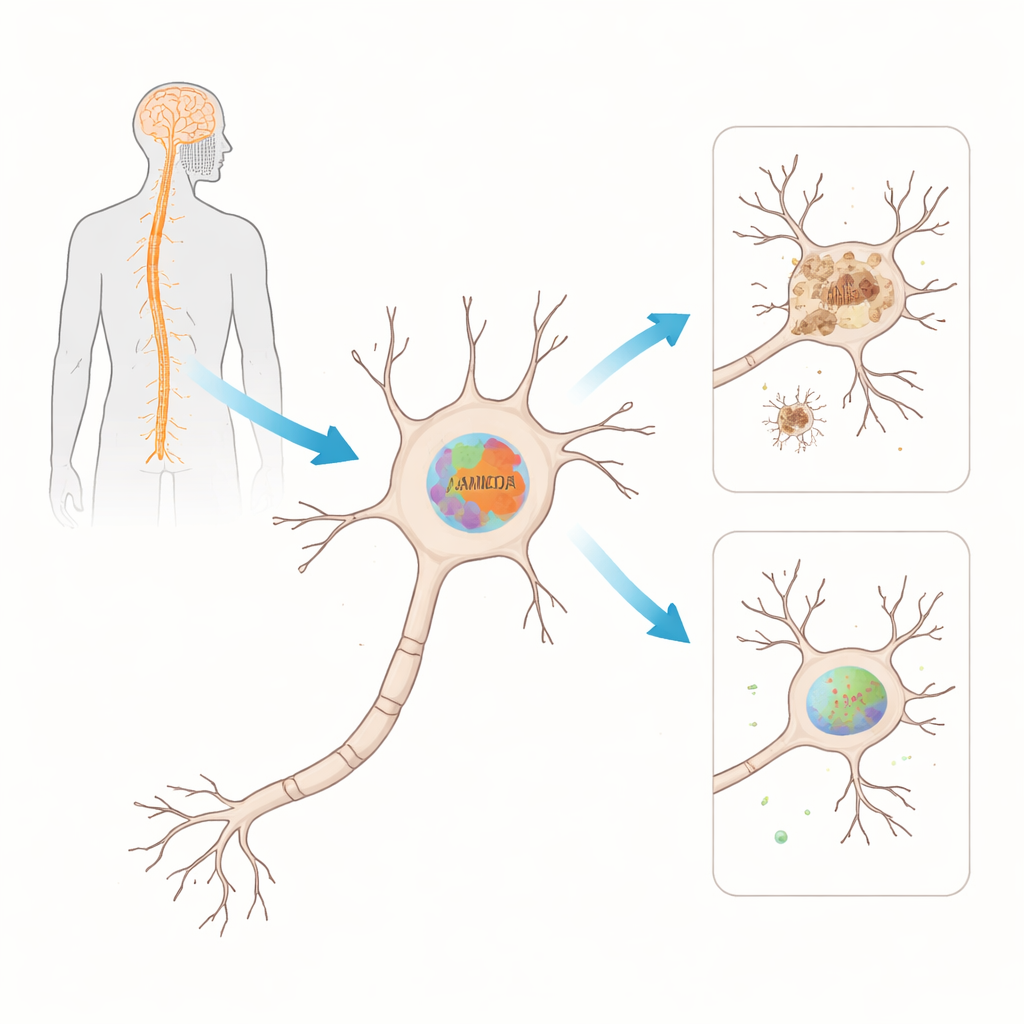
Suivre une protéine vulnérable au cours de la progression de la maladie
Pour tester si FAM120A joue effectivement un rôle dans la SLA, l'équipe s'est tournée vers un modèle murin largement utilisé portant une version mutante du gène SOD1, l'une des premières causes génétiques identifiées dans la SLA. Ils ont mesuré à la fois les messages ARN et les niveaux protéiques de la version murine, Fam120A, dans la moelle épinière au fil du temps, depuis la phase pré‑symptomatique jusqu'aux stades avancés de la maladie. Tôt dans la maladie, les niveaux d'ARN de Fam120A ont chuté dans la moelle épinière avant que les animaux ne montrent des signes clairs de maladie. Plus tard, au fur et à mesure que la paralysie se développait, la protéine Fam120A elle‑même était nettement réduite. Ce décalage — l'ARN qui change d'abord, la protéine ensuite — suggère que plusieurs niveaux de régulation se dérèglent à mesure que la maladie progresse.
Où se trouve cette protéine dans la moelle épinière
Les scientifiques ont ensuite cherché à savoir où exactement Fam120A est localisée dans la moelle épinière. En utilisant la microscopie à fluorescence sur des coupes de tissu, ils ont observé que Fam120A est principalement présente dans les neurones de la corne ventrale — la région riche en motoneurones qui dégénèrent dans la SLA. À un stade tardif de la maladie, ils ont noté un signal dans des cellules de soutien appelées astrocytes, mais le schéma dominant restait neuronal. Ces observations relient Fam120A directement aux cellules qui échouent dans la SLA et soutiennent l'idée que sa perte pourrait affaiblir leur capacité à gérer le stress cellulaire, contribuant possiblement au déclin de la fonction motrice.
Mettre un surplus de FAM120A au travail dans des cellules de type nerveux
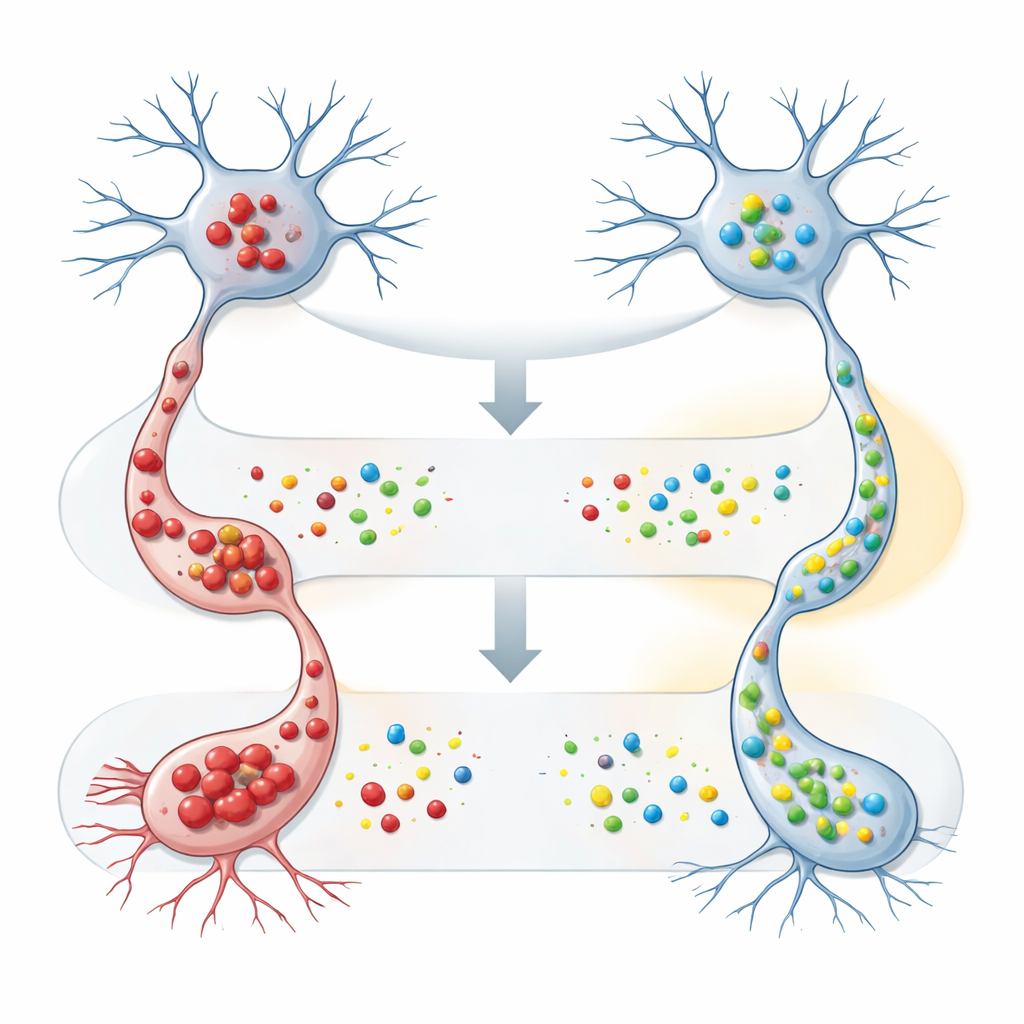
L'équipe est ensuite passée à des cellules cultivées de type nerveux pour explorer la fonction réelle de FAM120A. Ils ont modifié ces cellules pour produire soit la forme normale soit la forme mutante de SOD1, qui tend à former des agrégats toxiques, puis ont forcé les cellules à produire un excès de FAM120A humain. En présence de SOD1 mutant, l'augmentation de FAM120A a réduit de manière significative à la fois la quantité de SOD1 insoluble détectée par des tests biochimiques et le nombre d'agrégats visibles au microscope. De manière importante, FAM120A avait peu d'effet sur la forme normale de SOD1, ce qui suggère qu'elle pourrait aider spécifiquement les cellules à gérer les protéines mal repliées ou sujettes à l'agrégation, un problème central dans la SLA et d'autres maladies neurodégénératives.
Construire une carte plus large d'alliés et d'ennemis moléculaires
Au‑delà de ces expériences, les chercheurs ont exploré le réseau d'interactions plus vaste de FAM120A. Ils ont confirmé qu'elle s'associe physiquement à PURA, une protéine liant l'ARN déjà liée au développement cérébral et à la neurodégénérescence, et ont constaté que les niveaux de PURA chutent également dans la moelle épinière du modèle murin de la SLA, bien qu'à un stade plus tardif de la maladie. Ils mettent en avant d'autres liens entre FAM120A, son gène partenaire antisens FAM120Aos, et une autre protéine liant l'ARN, ELAVL1, qui régule des gènes impliqués dans l'inflammation et les réponses au stress dans le cerveau. Cette toile de connexions place FAM120A au carrefour de la régulation de l'ARN, des réponses au stress et du contrôle de la qualité protéique — précisément les systèmes qui défaillent dans la SLA.
Ce que cela pourrait signifier pour les traitements futurs de la SLA
Pris ensemble, ces résultats suggèrent que FAM120A n'est pas un simple spectateur mais une composante importante du réseau moléculaire de la SLA. Son déclin précoce dans les motoneurones vulnérables, ses liens physiques avec d'autres protéines régulant l'ARN et sa capacité à réduire les amas toxiques de SOD1 dans les cellules indiquent tous un rôle protecteur dans le maintien de l'équilibre protéique. Beaucoup de travail reste à faire — notamment pour vérifier si des changements similaires surviennent chez les personnes atteintes de SLA et dans d'autres modèles de la maladie — mais FAM120A apparaît désormais comme une cible prometteuse pour des études futures et, potentiellement, pour des thérapies visant à préserver la santé des motoneurones.
Citation: Vicencio, E., Gomez, L., Beltran, S. et al. FAM120A - a protein inserted in the ALS disease network. Sci Rep 16, 8200 (2026). https://doi.org/10.1038/s41598-026-39329-2
Mots-clés: sclérose latérale amyotrophique, neurones moteurs, agrégation protéique, protéines liant l'ARN, neurodégénérescence