Clear Sky Science · fr
La toxicologie intégrative en réseau et les preuves expérimentales révèlent les mécanismes sous-jacents à l’initiation et à la progression du cancer de l’endomètre induites par le phtalate diéthyl
Des produits chimiques quotidiens et le risque de cancer chez les femmes
Les assouplissants plastiques sont omniprésents dans la vie moderne, présents dans les emballages, les cosmétiques et les dispositifs médicaux. L’un d’eux, le phtalate diéthyl (DEP), est si répandu que son produit de dégradation peut être détecté dans l’urine de la plupart des personnes. Parallèlement, l’incidence du cancer de l’endomètre — un cancer de la muqueuse utérine — augmente dans le monde. Cette étude pose une question urgente pour toute personne préoccupée par la santé environnementale : une exposition prolongée au DEP pourrait-elle discrètement pousser les cellules de l’utérus vers la cancérogenèse, et si oui, de quelle manière ?
Comment l’étude a relié exposition et maladie
Les chercheurs ont commencé par exploiter de larges bases de données publiques contenant des profils d’expression génique provenant de tissus de cancer de l’endomètre et de muqueuse utérine saine. En comparant des milliers de gènes simultanément, ils ont identifié lesquels étaient systématiquement plus ou moins actifs dans le cancer. Ils ont ensuite superposé cette carte avec une seconde : la liste des gènes humains que des bases de données chimiques et des outils de prédiction antérieurs suggèrent comme susceptibles d’interagir avec le DEP. Là où ces deux cartes se recoupaient, ils ont mis au jour 19 gènes se situant au carrefour de l’exposition au DEP et du cancer de l’endomètre, suggérant un lien mécanistique entre un produit chimique courant et le développement tumoral.
Algorithmes intelligents pour trouver les gènes les plus cruciaux
Parcourir 19 gènes candidats reste un défi, aussi l’équipe a-t-elle eu recours à l’apprentissage automatique. Ils ont entraîné et testé plus de 100 modèles prédictifs différents sur des jeux de données patients combinés pour voir quels ensembles de gènes distinguaient le mieux les tissus cancéreux des tissus normaux. En utilisant une méthode d’interprétabilité appelée SHAP, qui révèle dans quelle mesure chaque gène « pousse » une prédiction vers l’état cancéreux ou sain, ils ont établi un classement des candidats. Cinq gènes — FOS, JUN, NR4A1, ADRA2C et SLC6A2 — ont émergé comme acteurs centraux, chacun montrant individuellement une forte capacité à séparer les échantillons cancéreux des non-cancéreux, et formant ensemble une empreinte des changements liés au DEP dans la muqueuse utérine.
Zoom sur les rencontres chimie–protéine
Pour vérifier si le DEP pouvait se lier physiquement aux protéines codées par ces gènes, les chercheurs ont utilisé le docking moléculaire et de longues simulations informatiques du mouvement atomique. Ces analyses suggèrent que le DEP s’insère dans des poches de plusieurs de ces protéines, en particulier ADRA2C, NR4A1 et SLC6A2, formant des complexes stables au fil du temps. De telles expériences virtuelles ne prouvent pas à elles seules la causalité, mais elles renforcent l’idée que le DEP peut se fixer directement sur des protéines de contrôle clés à l’intérieur ou à la surface des cellules utérines, pouvant ainsi influer sur leur comportement d’une manière favorable à la croissance tumorale.
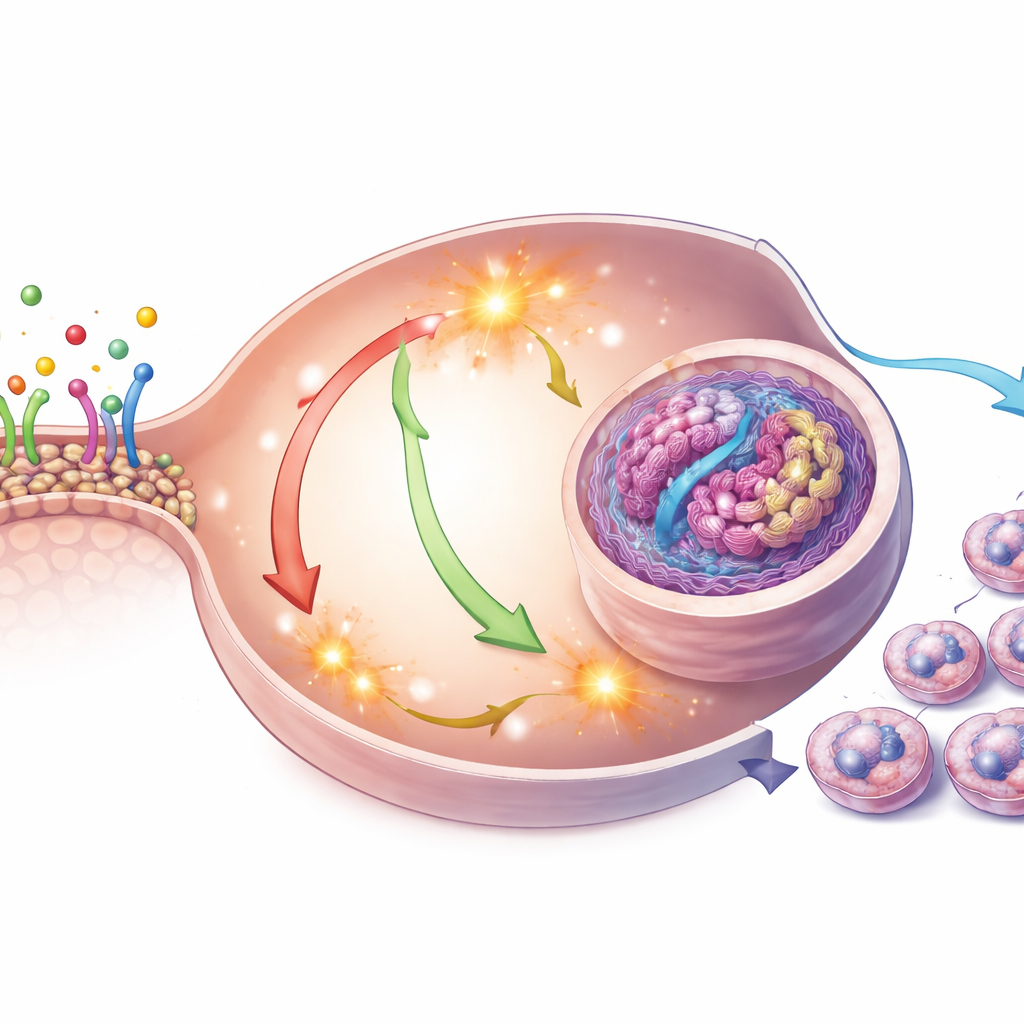
Ce qui se passe à l’intérieur des cellules utérines
L’équipe est ensuite passée des modèles informatiques aux cellules vivantes, en exposant deux lignées cellulaires humaines de cancer de l’endomètre au DEP à des doses choisies pour être biologiquement actives mais pas immédiatement toxiques. Ils ont observé que les cellules traitées au DEP se multipliaient plus rapidement et entraient plus facilement dans la phase de copie de l’ADN du cycle cellulaire. À l’intérieur de ces cellules, les niveaux d’espèces réactives de l’oxygène — des formes chimiquement agressives de l’oxygène — ont augmenté, tandis qu’une enzyme antioxydante naturelle a diminué. Parallèlement, des voies majeures de contrôle de la croissance intracellulaire, souvent désignées MAPK/ERK et PI3K/AKT, sont devenues plus actives. Cette activation a coïncidé avec une augmentation de la Cycline D1 et de CDK4, deux protéines qui jouent un rôle de vigie en poussant les cellules d’un état de repos vers la division active.
Qu’est-ce que cela signifie pour la vie quotidienne
Pris ensemble, les résultats dressent un tableau à plusieurs niveaux : le DEP peut se lier à des protéines cellulaires spécifiques, déclencher un stress oxydatif, activer des circuits de signalisation favorisant la croissance et accélérer le cycle cellulaire dans des cellules de cancer de l’endomètre. Pour un non-spécialiste, le message est qu’un additif plastique courant a le potentiel de créer un terrain plus « fertile » pour le cancer dans la muqueuse utérine, en particulier dans un organisme déjà influencé par des hormones et d’autres facteurs de risque. Bien que ces travaux aient été réalisés sur des modèles cellulaires et nécessitent encore des confirmations chez l’animal et chez l’humain, ils soulignent l’importance d’examiner de près les expositions chimiques de routine et soutiennent les efforts visant à réduire les contacts avec des composés perturbateurs endocriniens inutiles.
Citation: Chen, X., Wang, Z., Wang, F. et al. Integrative network toxicology and experimental evidence reveal mechanisms underlying diethyl phthalate-induced initiation and progression of endometrial cancer. Sci Rep 16, 8066 (2026). https://doi.org/10.1038/s41598-026-39325-6
Mots-clés: cancer de l’endomètre, phtalate diéthyl, perturbateurs endocriniens, toxicologie environnementale, signalisation cellulaire