Clear Sky Science · fr
Dynamiques microbiologiques et rhéologiques des biofilms mixtes formés par des bactéries et un virus eucaryote
Communautés cachées sur les dispositifs hospitaliers
De nombreuses infections hospitalières ne commencent pas par un seul germe, mais par des communautés visqueuses et invisibles appelées biofilms qui couvrent les cathéters et d'autres dispositifs médicaux. Cette étude examine une question négligée mais aux grandes répercussions pour la sécurité des patients : que se passe-t-il lorsque non seulement des bactéries, mais aussi des virus infectant l'homme, s'installent ensemble dans ces biofilms ? En observant le comportement d'un virus mammifère courant au sein des biofilms bactériens, les chercheurs révèlent comment ces villes microbiennes collantes peuvent abriter silencieusement des virus et modifier leur comportement.
Villes collantes de microbes
Les biofilms ressemblent à des villes microscopiques construites par des microbes sur des surfaces humides—canalisations, rochers, dents ou tubes en plastique placés chez des patients. Les bactéries s'installent, se multiplient et sécrètent une matrice semblable à une colle qui les protège du dessèchement, des produits chimiques et du système immunitaire. À l'hôpital, ces biofilms se forment couramment sur les cathéters urinaires et veineux, où ils peuvent ensemencer des infections sanguines et des infections urinaires difficiles à traiter. Ces biofilms contiennent généralement de nombreuses espèces et même différents règnes du vivant, mais la plupart des recherches se sont concentrées uniquement sur les bactéries, laissant le rôle des virus largement inexploré.
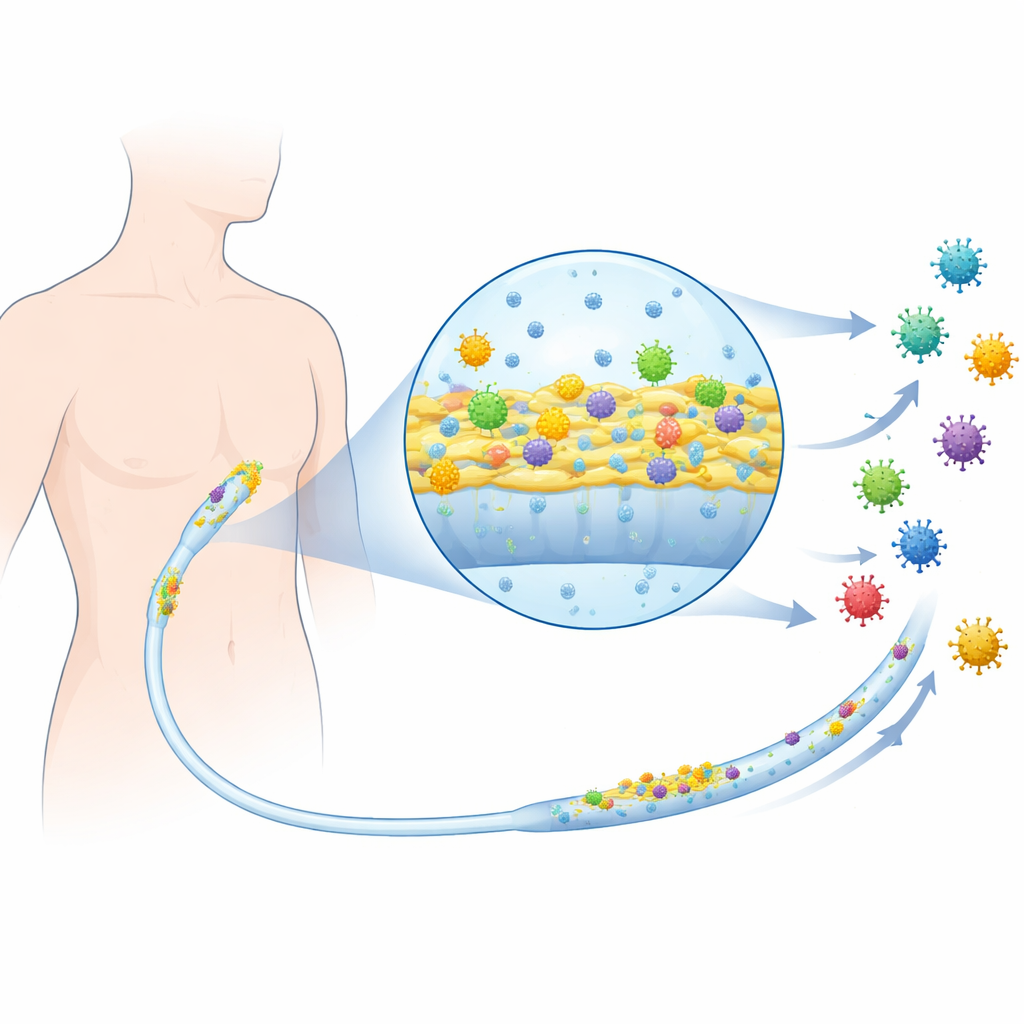
Introduire un virus de mammifère dans le mélange
L'équipe a travaillé avec des souches bactériennes cliniques connues pour coloniser les cathéters, notamment des Escherichia coli uropathogènes responsables d'infections urinaires et d'autres bactéries fréquemment retrouvées dans les infections de voies centrales. Ils ont ensuite introduit le reovirus mammifère, un virus non enveloppé bien étudié qui infecte les cellules animales, comme substitut de virus infectant l'humain de manière plus générale. Ils ont d'abord vérifié si l'ajout de matériel contenant des virus affectait la croissance bactérienne libre normale. Pour de nombreuses souches, les bactéries ont poussé et survécu tout aussi bien avec ou sans virus, montrant que le virus ne tuait pas directement les bactéries et n'agissait pas comme un antibiotique.
Les biofilms modifient la texture, pas la taille
Lorsque les bactéries se déposent en biofilms, le tableau devient plus nuancé. Pour la plupart des souches, la quantité totale de biofilm—mesurée par une coloration standard qui quantifie la matière couchant une surface—changeait peu en présence du virus. Certaines souches, toutefois, produisaient légèrement plus ou moins de biofilm selon la présence ou non de préparations virales, suggérant des effets spécifiques à la souche. Pour aller au-delà de la simple quantité, les chercheurs ont emprunté des outils à la science des matériaux et ont mesuré à quel point chaque biofilm était « mou » ou « rigide », un peu comme on sonde la texture d'un gel. Ils ont montré que chaque souche bactérienne formait sa propre signature mécanique. Fait important, l'ajout du virus pouvait soit raidir soit assouplir ces biofilms selon la souche : dans une souche d'E. coli, le virus rendait la matrice plus rigide, tandis que dans une souche de Staphylococcus epidermidis, le virus entraînait une structure plus faible et plus conforme.
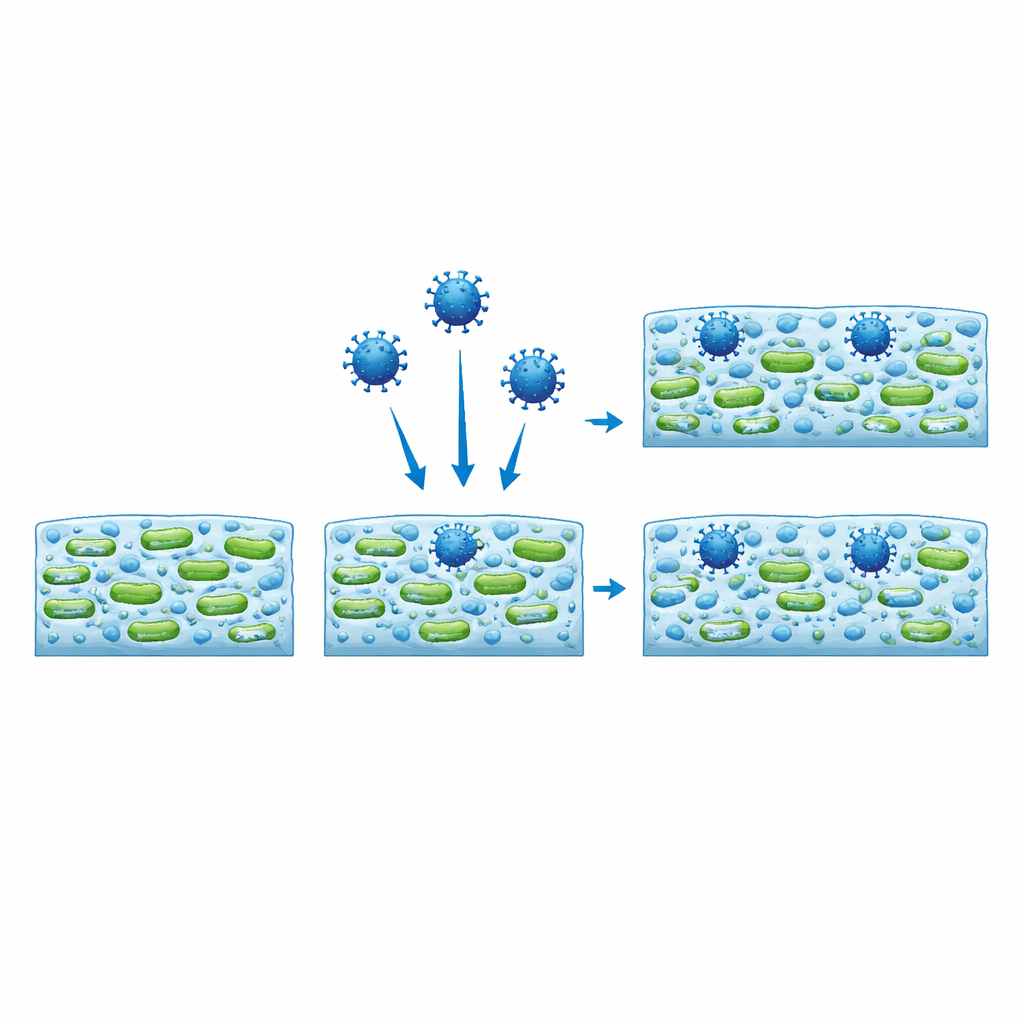
Les virus trouvent un abri et conservent leur pouvoir infectieux
Grâce à la microscopie à fluorescence, les scientifiques ont marqué les particules virales pour qu'elles brillent et ont suivi leur localisation au sein du biofilm. Contrairement à des billes plastiques inertes de taille similaire, qui restaient surtout dans des zones clairsemées et étaient emportées au lavage, les virus pénétraient profondément dans la matrice et avaient tendance à se regrouper là où les cellules bactériennes étaient les plus denses. Dans certains cas, la présence du virus modifiait même la forme globale du biofilm, transformant des amas compacts en réseaux plus filamenteux ou inversement, selon la souche bactérienne. Pour tester si ces virus emprisonnés restaient dangereux, les auteurs les ont retrouvés dans les biofilms puis les ont exposés à des cellules de mammifères. Les virus récupérés sont demeurés infectieux, malgré leur séjour dans la matière bactérienne pendant deux jours.
Pourquoi cela compte pour les patients et au-delà
Pour le grand public, le message principal est que les biofilms sur les dispositifs médicaux peuvent non seulement protéger les bactéries contre les traitements—ils peuvent aussi cacher et préserver des virus qui infectent les cellules humaines ou animales. L'étude montre que les virus peuvent s'installer dans la matrice bactérienne, modifier subtilement la structure du biofilm tout en restant pleinement capables d'infecter de nouvelles cellules une fois libérés. Cela suggère que les cathéters et autres surfaces recouverts de biofilms pourraient servir de réservoirs silencieux où les virus persistent, à l'abri du dessèchement, des désinfectants et des attaques du système immunitaire. Comprendre ces communautés microbiennes mixtes pourrait être crucial pour concevoir de meilleurs matériaux, stratégies de nettoyage et thérapies ciblant à la fois les partenaires bactériens et viraux afin de réduire les infections tenaces associées aux dispositifs.
Citation: Gao, J., Abriat, C., Laekas-Hameder, M. et al. Microbiological and rheological dynamics of mixed biofilms formed by bacteria and eukaryotic virus. Sci Rep 16, 8315 (2026). https://doi.org/10.1038/s41598-026-39314-9
Mots-clés: biofilms, infections liées aux cathéters, interactions virus–bactéries, reovirus, communautés microbiennes