Clear Sky Science · fr
Un modèle de physique des polymères du noyau cellulaire en interphase pour des simulations radiobiologiques
Pourquoi la forme de notre « maison » d’ADN compte
Les rayonnements sont une arme à double tranchant en médecine : ils peuvent tuer les cellules cancéreuses, mais aussi endommager les tissus sains. Au cœur de ces risques et bénéfices se trouve notre ADN, compacté à l’intérieur du noyau cellulaire. Cet article montre comment un modèle 3D détaillé, inspiré de la physique, de cette « ville » nucléaire d’ADN peut aider les chercheurs à prévoir comment les rayonnements brisent et réparent mal les chromosomes, améliorant potentiellement le traitement du cancer et les estimations des risques liés aux radiations spatiales.
Voir le génome comme une structure vivante
Dans chaque cellule humaine, deux mètres d’ADN sont repliés dans un noyau minuscule de seulement quelques micromètres. Ce repliement n’est pas aléatoire : chaque chromosome tend à occuper son propre territoire, lui-même divisé en quartiers et en domaines en boucles. De nouveaux outils expérimentaux, comme la microscopie à super-résolution et les cartes de contacts Hi-C, ont révélé cette organisation 3D avec un détail remarquable. Pourtant, la plupart des modèles de radiation traitent encore l’ADN comme un enchevêtrement simplifié de lignes ou des boucles idéalisées, en négligeant cette organisation de niveau supérieur. Les auteurs se sont donné pour objectif de construire un modèle de noyau entier qui respecte ce que les biologistes savent de l’architecture réelle de la chromatine, tout en restant suffisamment rapide pour tourner sur des ordinateurs de laboratoire ordinaires.
Construire un noyau virtuel avec la physique des polymères
L’équipe a modélisé les chromosomes comme des chaînes flexibles, empruntant des concepts à la physique des polymères, le même domaine utilisé pour comprendre les plastiques et les matériaux mous. Ils ont découpé le problème en trois étapes de relaxation pour maîtriser le coût informatique énorme. D’abord, ils ont placé de grands blocs appelés domaines de chromatine dans tout le noyau, en leur permettant de se repousser mutuellement, de s’étirer le long de leur longueur et de se regrouper en sous-compartiments plus larges. Ensuite, ils ont zoomé à l’intérieur de chaque domaine pour déployer des fibres de chromatine plus fines, y compris des régions en boucle maintenues par des protéines de liaison. Troisièmement, ils ont laissé toutes les fibres interagir librement à l’intérieur de la limite nucléaire pour atteindre une configuration finale réaliste. En divisant ainsi le processus et en ajoutant une recherche hiérarchique et des astuces de calcul parallèle, ils ont réduit le temps d’exécution d’un délai impraticable de quatre mois à environ trois heures par noyau virtuel sur une station de travail 64 cœurs.
Des traces de radiation aux cassures et réparations de l’ADN
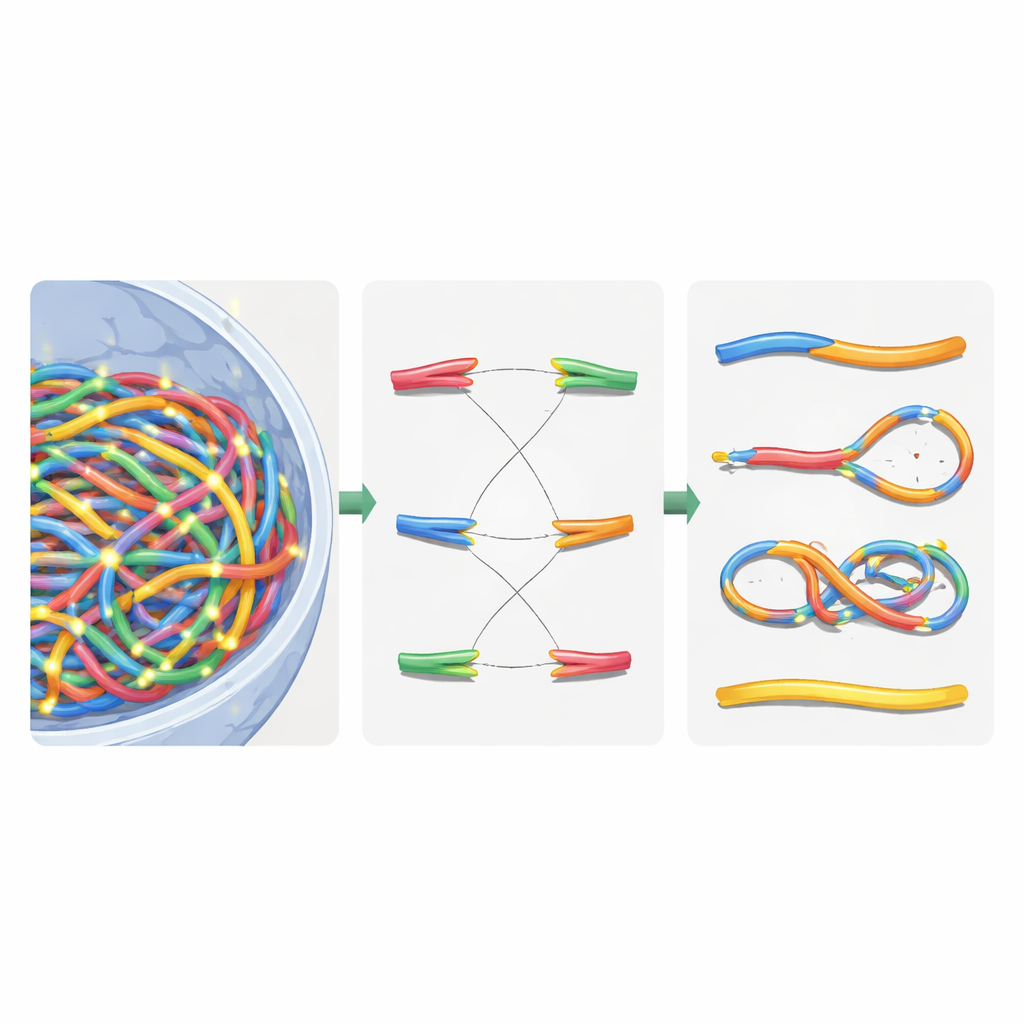
Une fois le noyau virtuel construit, les auteurs ont superposé des traces de radiation détaillées générées par des simulations Geant4‑DNA. Ils ont utilisé une recherche hiérarchique pour trouver, pour chaque événement d’ionisation, quel domaine de chromatine, quel segment de fibre et enfin quel nucléotide était le plus proche, sans jamais stocker les dix milliards de positions de nucléotides en mémoire. À la place, ils ont conservé un modèle réutilisable de chromatine et appliqué des transformations de coordonnées astucieuses à la volée. Les ionisations dans l’épine dorsale de l’ADN ont été traitées comme des cassures simples, et des cassures proches sur des brins opposés sont devenues des cassures double brin. Pour reproduire la machinerie de réparation cellulaire, les auteurs ont introduit une règle de recollage basée sur la distance : les extrémités d’ADN libres situées à proximité ont plus de chances de se recoller. Les décisions de recollage étaient prises étape par étape jusqu’à ce que toutes les extrémités soient appariées ou laissées non réparées, recréant à la fois des réparations correctes et des fragments mal joints.
Trier les chromosomes brisés avec une logique de réseau
Après cette réparation virtuelle, le noyau contenait un mélange de chromosomes réassemblés et de fragments résiduels. Pour classer ce qui s’était produit, les auteurs ont traduit le génome réparé en un graphe non orienté : les segments de chromosome sont devenus des arêtes, et leurs extrémités et points de rupture sont devenus des nœuds. En utilisant un algorithme standard de composantes connexes, ils ont pu récupérer automatiquement chaque nouvel objet de type chromosome et compter des caractéristiques clés telles que le nombre de centromères (points d’attache pour la division cellulaire) et de télomères (extrémités naturelles). À partir de là, ils ont identifié des dicentriques (chromosomes avec deux centromères), des anneaux et des délétions. Ils ont ensuite comparé leurs simulations à des expériences classiques sur des cellules de la peau humaine exposées à des rayons gamma et des particules alpha, constatant que les aberrations chromosomiques totales étaient reproduites à environ 20 % des valeurs mesurées, une amélioration significative par rapport aux modèles antérieurs.
Ce que cela signifie pour les patients et les astronautes
En termes simples, ce travail montre que « où » l’ADN se situe dans le noyau et « comment » il se replie influencent fortement la manière dont les dommages par radiation se cumulent en modifications chromosomiques dangereuses. En combinant une architecture 3D réaliste du génome, une simulation efficace fondée sur la physique et un comptage des chromosomes brisés basé sur les graphes, les auteurs créent un pont puissant entre la biologie structurale et la radiobiologie. Ils soutiennent que des améliorations futures — comme l’ajout d’un calendrier détaillé des réparations et l’utilisation de données de séquençage du génome entier — pourraient rendre cette approche encore meilleure pour prédire l’impact biologique des particules énergétiques utilisées en thérapie anticancéreuse ou rencontrées en mission spatiale lointaine. En fin de compte, de meilleurs modèles de la « maison » d’ADN à l’intérieur de nos cellules pourraient aider à adapter des traitements par radiation plus sûrs et plus efficaces et à affiner notre compréhension des risques radiologiques à long terme.
Citation: Zhao, M., Huang, G., Xu, Z. et al. A polymer physics model of the interphase cell nucleus for radiobiological simulations. Sci Rep 16, 7913 (2026). https://doi.org/10.1038/s41598-026-39234-8
Mots-clés: lésions d’ADN induites par les rayonnements, architecture 3D de la chromatine, anomalies chromosomiques, modélisation par physique des polymères, thérapie par particules