Clear Sky Science · fr
Évolution de la fonction mitochondriale des cellules mononucléées du sang périphérique pendant la phase aiguë du sepsis chez des patients en réanimation
Pourquoi les centrales énergétiques de nos cellules comptent dans les infections mortelles
Le sepsis, une réaction potentiellement mortelle à une infection, conduit chaque année des centaines de milliers de personnes en unités de soins intensifs (USI) et tue des millions de personnes dans le monde. Les médecins savent que de nombreux organes défaillent pendant le sepsis, mais le rôle discret de petites « centrales » à l’intérieur de nos cellules immunitaires — les mitochondries — a été plus difficile à préciser. Cette étude a suivi des patients en USI atteints de sepsis pendant leur première semaine de soins intensifs pour observer comment la production d’énergie des principales cellules immunitaires sanguines évoluait dans le temps et si ces changements étaient associés à la survie.
Observer le sang pendant le sepsis
Les chercheurs se sont concentrés sur les cellules mononucléées du sang périphérique, un groupe majeur de globules blancs qui contribuent à l’inflammation et à la lutte contre les agents infectieux. Parce qu’elles circulent dans tout le corps et sont faciles à prélever, ces cellules offrent une fenêtre utile sur la manière dont le système immunitaire réagit. L’équipe a comparé 40 adultes atteints de sepsis ou de choc septique dans une USI néerlandaise à 30 témoins hospitaliers appariés par âge et sexe, sans sepsis et métaboliquement sains. Le sang des patients septicémiques a été prélevé trois fois — dans les deux premiers jours suivant l’admission en USI puis autour des jours 3–4 et 5–6 — tandis que le sang des témoins a été prélevé une fois. À partir de chaque échantillon, les investigateurs ont isolé les cellules immunitaires, les ont placées dans une solution nutritive standardisée et ont mesuré la vitesse à laquelle leurs mitochondries consommaient de l’oxygène dans différentes conditions, une mesure directe de l’activité des « centrales » cellulaires. 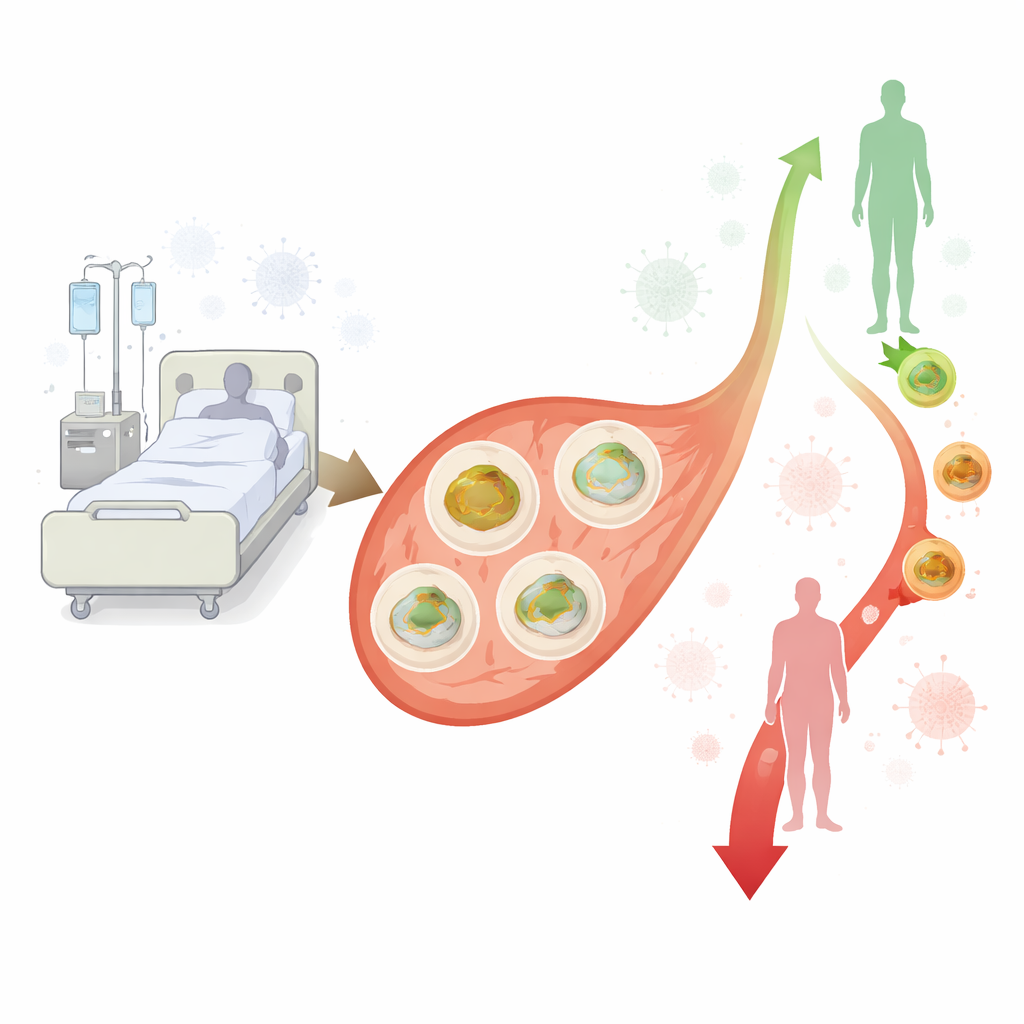
Des moteurs des cellules immunitaires en surrégime
Contrairement à l’idée selon laquelle le sepsis « éteint » simplement la production d’énergie cellulaire, l’équipe a trouvé que l’activité mitochondriale dans les cellules immunitaires était systématiquement plus élevée chez les patients septicémiques que chez les témoins. À tous les moments mesurés, la respiration basale (l’utilisation d’oxygène au repos) était augmentée. Les composantes liées à la production utile d’énergie — la respiration liée à l’ATP — ainsi que la capacité maximale respiratoire des mitochondries avaient également tendance à être plus élevées, en particulier plus tard durant la première semaine. Même la fuite de protons, une forme de « respiration » gaspillée où le carburant est brûlé sans produire d’énergie, était augmentée. Ensemble, ces résultats suggèrent que, du moins dans les cellules immunitaires circulantes, la machinerie énergétique est accélérée plutôt que défaillante pendant le sepsis précoce, reflétant peut‑être les fortes exigences d’une réponse immunitaire activée.
Signaux géniques compatibles avec une activité accrue
Pour vérifier si cette respiration plus intense était soutenue au niveau moléculaire, les chercheurs ont examiné l’activité de plusieurs gènes codant des éléments critiques de la machinerie mitochondriale. Dans un sous‑groupe de 10 patients septicémiques et 10 témoins appariés, ils ont mesuré l’expression génique de composants des complexes de phosphorylation oxydative — les assemblages protéiques qui convertissent le carburant en ATP. Deux gènes en particulier, SDHB (partie du complexe II) et ATP5F1A (partie du complexe V, l’ATP synthase), étaient significativement plus actifs chez les patients septicémiques à plusieurs moments, avec des augmentations d’environ 40–50 % par rapport aux témoins. Cette « montée en régime » moléculaire des composants centraux concorde avec les données fonctionnelles, renforçant l’idée que les mitochondries des cellules immunitaires sont poussées à travailler davantage pendant le sepsis plutôt qu’à se dégrader purement et simplement. 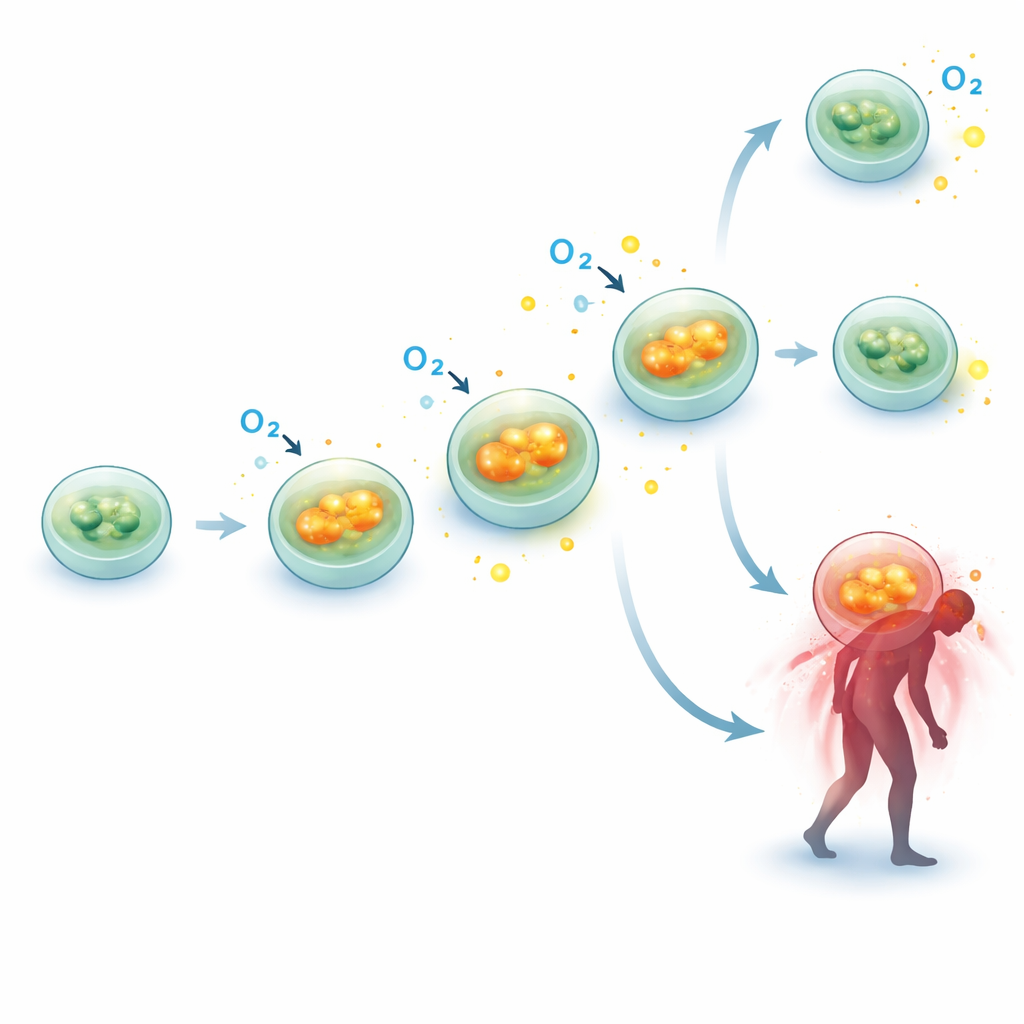
Des modifications énergétiques liées au devenir des patients
La constatation la plus frappante concernait la manière dont ces changements mitochondriaux se rapportaient au pronostic. Lorsque l’équipe a comparé les survivants aux non‑survivants sur trois mois, elle n’a pas observé de différences majeures de fonction mitochondriale au tout premier prélèvement. Cependant, la direction de l’évolution au cours de la première semaine racontait une autre histoire. Chez les survivants, la respiration mitochondriale des cellules immunitaires avait tendance à diminuer légèrement ou à rester stable. Chez les patients décédés par la suite, ces mêmes mesures — respiration basale, liée à l’ATP, respiration maximale et réserve respiratoire — augmentaient encore au fil de la semaine. L’analyse statistique a suggéré qu’une augmentation plus marquée de la respiration basale entre le premier et le dernier prélèvement était associée à un risque plus élevé de décès dans les trois mois, même après ajustement sur les scores de sévérité de la maladie. Comme le nombre de décès était limité, les auteurs soulignent que ce lien est exploratoire et nécessite confirmation, mais il laisse entendre qu’une poussée métabolique persistante dans les cellules immunitaires pourrait être un signal d’alerte.
Ce que cela signifie pour les patients atteints de sepsis
Pour un non‑spécialiste, le message central est que, au cours du sepsis précoce, les « centrales » à l’intérieur des cellules immunitaires circulantes ne tombent pas simplement en panne ; elles semblent au contraire passer en surrégime. Cet effort supplémentaire peut aider à alimenter la lutte précoce du corps contre l’infection, mais chez certains patients il continue d’augmenter au lieu de se stabiliser, et cette suractivité persistante dans les cellules immunitaires sanguines était associée à une survie plus mauvaise. L’étude ne montre pas encore si cette poussée mitochondriale est bénéfique, nuisible, ou les deux selon les stades, mais elle souligne que le sepsis est autant une maladie de l’économie énergétique de l’organisme qu’une maladie d’infection et d’inflammation. À l’avenir, suivre attentivement et peut‑être moduler délicatement cette utilisation énergétique cellulaire pourrait faire partie des moyens par lesquels les médecins évaluent le risque et adaptent les traitements des personnes en lutte contre le sepsis en USI.
Citation: Moonen, H.P.F.X., Slingerland-Boot, R., de Jong, J.C.B.C. et al. Progression of peripheral blood mononuclear cell mitochondrial function during the early phase of sepsis in intensive care unit patients. Sci Rep 16, 8828 (2026). https://doi.org/10.1038/s41598-026-39202-2
Mots-clés: sepsis, mitochondries, cellules immunitaires, maladie critique, métabolisme cellulaire