Clear Sky Science · fr
Augmentation de l’athérosclérose et expression des inflammarafts dans les cellules spumeuses macrophagiques chez des souris déficientes en AIBP.
Pourquoi les artères bouchées sont plus que du simple excès de graisses
L’athérosclérose — l’obstruction et le raidissement progressifs de nos artères — est une cause majeure d’infarctus et d’accidents vasculaires cérébraux. On l’imagine souvent comme un simple dépôt de graisses dans les vaisseaux, mais l’histoire est plus complexe : les cellules immunitaires dans la paroi vasculaire peuvent soit apaiser la situation, soit attiser l’inflammation. Cette étude examine pourquoi, dans certaines circonstances, ces cellules passent de « brigades de nettoyage » qui stockent les graisses à des instigatrices dangereuses qui poussent les plaques vers un stade plus létal.
Cellules immunitaires accumulant les graisses
Au sein des plaques en formation, un type de globule blanc appelé macrophage absorbe de grandes quantités de cholestérol et se transforme en cellule dite spumeuse — une cellule gonflée remplie de gouttelettes huileuses. Des travaux antérieurs chez la souris suggéraient que ces cellules spumeuses, malgré leur aspect malsain, sont étonnamment calmes sur le plan inflammatoire, tandis que des macrophages plus maigres à proximité ont tendance à produire davantage de signaux inflammatoires. La nouvelle recherche s’interroge sur ce qui se passe si l’organisme manque d’une protéine appelée AIBP, qui aide normalement à éliminer le cholestérol de la surface cellulaire et à maintenir sous contrôle certaines « zones chaudes » de la membrane.
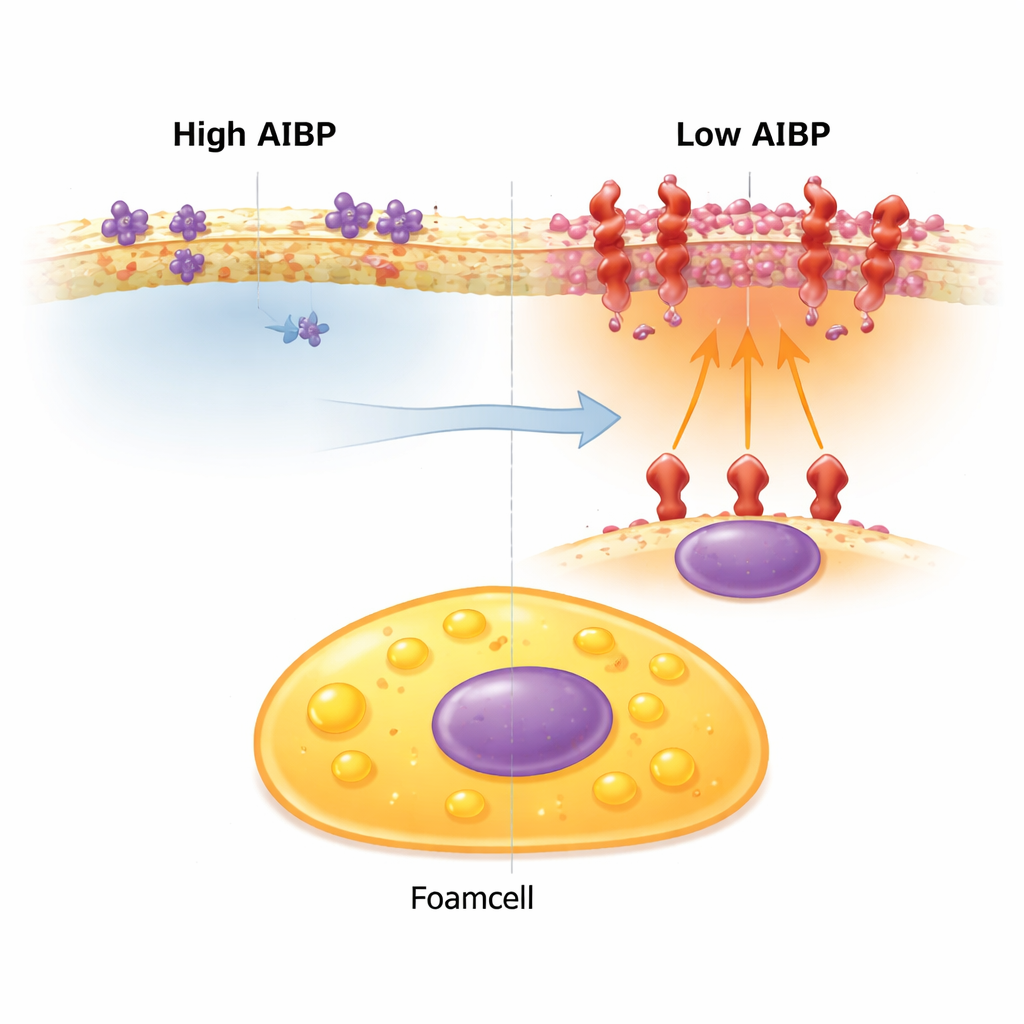
Zones chaudes de la membrane qui amplifient les signaux d’alarme
La surface cellulaire n’est pas uniforme. Le cholestérol et certaines graisses se regroupent en minuscules plateformes où des récepteurs détecteurs de danger peuvent se rassembler. Lorsque ces plateformes s’agrandissent et concentrent des récepteurs inflammatoires, les auteurs les désignent sous le nom d’« inflammarafts ». Un de ces récepteurs, TLR4, aide les cellules à détecter les menaces mais peut provoquer une inflammation chronique en cas de suractivation. Chez des souris normalement prédisposées à l’hypercholestérolémie, les macrophages non spumeux portent généralement davantage d’inflammarafts, tandis que les cellules spumeuses en ont relativement peu — une des raisons pour lesquelles on considérait que les cellules spumeuses étaient moins inflammatoires.
Quand les cellules chargées de graisses deviennent enflammées
L’équipe a comparé des souris dépourvues à la fois d’AIBP et d’un récepteur clé de l’élimination du cholestérol (les rendant fortement susceptibles aux maladies artérielles) avec des souris témoins ne présentant que l’absence de ce récepteur. Après 16 semaines d’un régime riche en graisses, les souris déficientes en AIBP présentaient des plaques contenant davantage de cellules spumeuses, chacune remplie de plus de graisses neutres. De manière cruciale, ces cellules spumeuses montraient désormais des niveaux élevés de dimères de TLR4 et de zones membranaires riches en cholestérol — caractéristiques des inflammarafts — faisant d’elles le principal type cellulaire inflammatoire dans la plaque, plutôt que les cellules plus calmes orientées vers le stockage observées auparavant. En culture, des macrophages provenant de souris déficientes en AIBP et transformés en cellules spumeuses par du cholestérol oxydé activaient des gènes associés à l’inflammation, à la dégradation tissulaire et au remodelage vasculaire, et présentaient davantage de stress oxydatif ainsi que des mitochondries en souffrance.
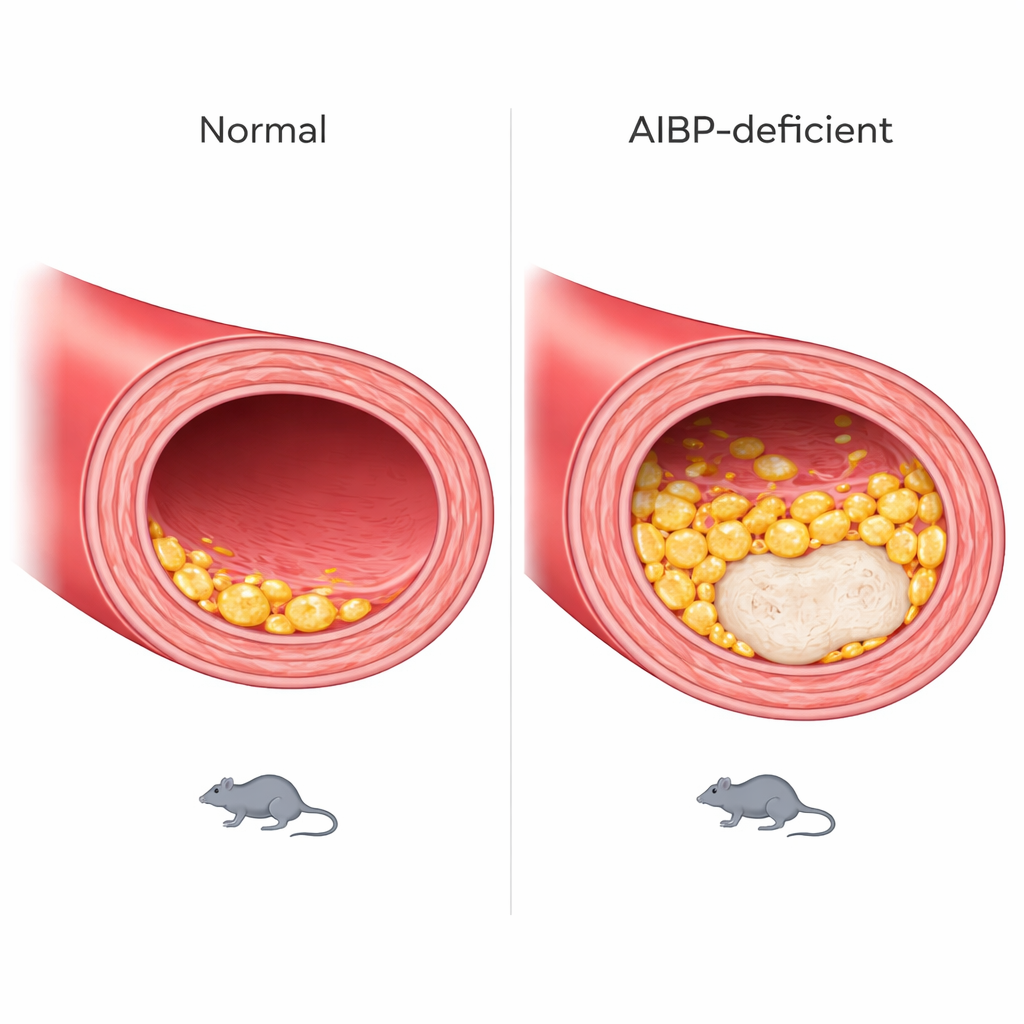
Des plaques plus volumineuses et instables dans la paroi vasculaire
Ces changements cellulaires se reflétaient par une maladie artérielle plus sévère. Des coupes transversales du principal vaisseau de sortie du cœur ont révélé que les souris déficientes en AIBP développaient des plaques plus grandes et, surtout, des cœurs nécrotiques plus étendus — des zones mortes au sein de la plaque associées à des lésions « vulnérables » sujettes à la rupture. Les mâles et les femelles étaient touchés, bien que la localisation le long du vaisseau du dommage le plus marqué diffère selon le sexe. Les animaux prenaient également du poids plus rapidement et présentaient des taux de triglycérides sanguins plus élevés, suggérant des perturbations plus larges du métabolisme lipidique.
Ce que cela pourrait signifier pour de futurs traitements
Pour un non-spécialiste, le message clé est que toutes les cellules chargées de cholestérol dans une plaque ne se valent pas. Lorsque AIBP est présent, les cellules spumeuses ont tendance à jouer un rôle de réservoir, stockant silencieusement l’excès de graisses. En l’absence d’AIBP, ces mêmes cellules reconfigurent leur surface, forment des inflammarafts et commencent à émettre des signaux inflammatoires puissants qui contribuent à faire progresser les plaques vers des stades avancés et dangereux. Bien que les travaux aient été réalisés chez la souris, ils mettent en lumière AIBP et le contrôle de ces zones membranaires comme des leviers potentiels pour des thérapies futures visant à empêcher les plaques artérielles de devenir instables et mortelles.
Citation: Li, S., Nazarenkov, N., Alekseeva, E. et al. Increased atherosclerosis and expression of inflammarafts in macrophage foam cells in AIBP-deficient mice.. Sci Rep 16, 7645 (2026). https://doi.org/10.1038/s41598-026-39113-2
Mots-clés: athérosclérose, cellules spumeuses macrophagiques, inflammation, métabolisme du cholestérol, AIBP