Clear Sky Science · fr
Préducteurs EEG de la récupération motrice pendant une rééducation immersive VR-BCI
Reconfigurer le mouvement après un AVC
Pour de nombreuses personnes survivantes d’un AVC, une faiblesse au bras ou à la main perdure pendant des années, limitant discrètement les gestes du quotidien comme s’habiller, cuisiner ou taper au clavier. Cette étude explore une forme de rééducation de haute technologie qui combine interfaces cerveau–ordinateur et réalité virtuelle immersive pour aider le cerveau à réapprendre à mobiliser un membre affaibli. En examinant de près les ondes cérébrales, les chercheurs posent une question pratique : l’activité cérébrale précoce pendant cet entraînement peut‑elle indiquer qui a le plus de chances de retrouver des capacités motrices ?
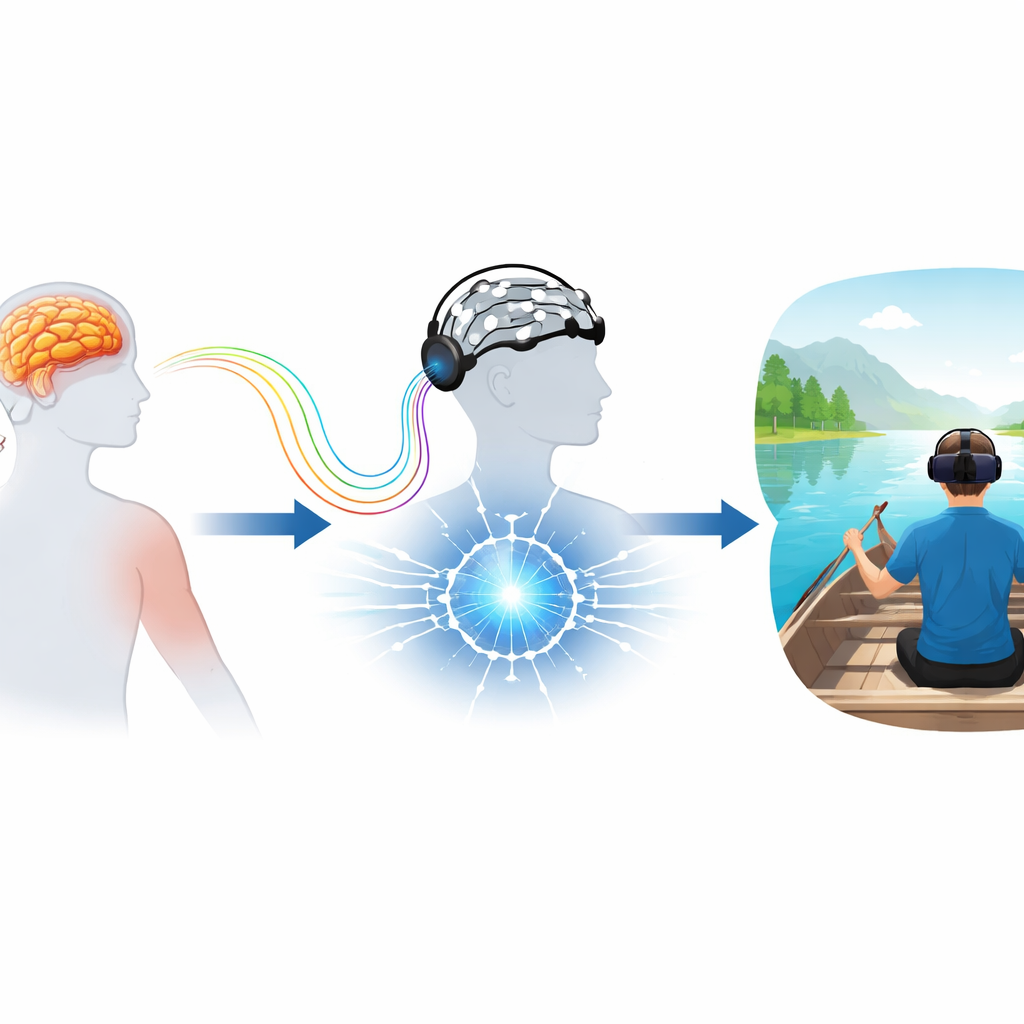
Entraîner le cerveau dans un bateau virtuel
L’équipe a travaillé avec des adultes présentant une faiblesse chronique du bras après un premier AVC. Sur quatre semaines, les participants du groupe expérimental ont effectué jusqu’à douze séances d’un jeu en réalité virtuelle immersive appelé NeuRow. Munis d’un casque de réalité virtuelle et d’une coiffe enregistrant les signaux cérébraux, ils étaient assis dans un bateau virtuel et devaient imaginer ramer du bras gauche ou droit tout en regardant un avatar virtuel effectuer le mouvement. Lorsque l’activité cérébrale correspondait au mouvement imaginé, le bateau avançait et de petites vibrations dans les contrôleurs manuels renforçaient l’action, créant une boucle étroite entre l’effort mental et le retour sensoriel. Un groupe témoin a reçu des séances supplémentaires de thérapie conventionnelle au lieu de cet entraînement basé sur la RV.
Écouter le rythme du cerveau
Les chercheurs se sont concentrés sur un motif particulier de l’activité électrique cérébrale appelé désynchronisation liée à l’événement, ou ERD. Lorsque nous planifions ou imaginons un mouvement, certaines oscillations rythmiques, en particulier au niveau des aires motrices, s’affaiblissent temporairement. Cette chute d’intensité rythmique serait le reflet de l’engagement des réseaux moteurs. À l’aide d’électroencéphalographie (EEG), l’équipe a mesuré l’ampleur de cette baisse lorsque les participants imaginaient ramer, et la répartition de ce motif entre les deux hémisphères. Ils ont aussi construit des bandes de fréquence individualisées pour chaque personne afin de tenir compte du fait que l’AVC peut déplacer ces rythmes de manière subtile.
Comparer les survivants d’un AVC et des cerveaux non lésés
Pour obtenir une référence de ce à quoi ressemblent des rythmes moteurs « sains » dans la même tâche RV, les auteurs ont comparé le groupe AVC à un groupe de référence de 35 personnes sans AVC ayant précédemment complété le protocole NeuRow identique. Sur les localisations clés liées à la motricité au niveau du scalp, les survivants d’un AVC présentaient une ERD sensiblement plus faible que le groupe de référence, et l’équilibre entre les deux hémisphères était moins stable. Autrement dit, leurs cerveaux mobilisaient les réseaux moteurs de façon moins forte et moins cohérente lors du mouvement imaginé. Cependant, au sein du groupe AVC, ces profils d’ERD n’ont guère évolué au cours des 12 séances d’entraînement, et la latéralité, ou l’équilibre gauche–droite, est restée relativement plate dans le temps.
Les signaux cérébraux de base comme boule de cristal
Même si l’intensité globale de l’ERD n’augmentait pas régulièrement avec l’entraînement, le niveau d’ERD au départ s’est avéré très informatif. À l’aide de modèles statistiques prenant en compte les différences individuelles, les chercheurs ont constaté que l’ERD de base dans les zones motrices affectées prédisait l’ampleur de l’amélioration de la fonction du bras, mesurée par le test standard de Fugl–Meyer, après l’intervention. Les participants dont le cerveau montrait une baisse rythmique motrice plus marquée au départ avaient tendance à gagner davantage en mouvement sur le mois. En revanche, les variations d’ERD d’une séance à l’autre étaient un prédicteur beaucoup plus faible de la récupération. L’étude a aussi laissé entrevoir que, particulièrement après un AVC ischémique, une activité accrue du côté non lésé du cerveau pourrait jouer un rôle compensatoire, une ERD ipsilatérale plus importante étant associée à de meilleurs résultats.
Qu’est‑ce que cela signifie pour la prise en charge future des AVC ?
Pour les patients et les cliniciens, ces résultats suggèrent qu’une simple mesure EEG réalisée en début d’entraînement VR–BCI pourrait fournir un indice puissant sur qui est le plus susceptible de bénéficier. Plutôt que d’attendre des semaines pour voir si la fonction s’améliore, les thérapeutes pourraient à terme utiliser les rythmes cérébraux de base pour personnaliser les plans de traitement, ajuster l’intensité ou combiner des thérapies pour les personnes dont le cerveau montre un engagement plus faible. L’étude souligne également que la récupération après un AVC chronique est complexe : les patients se sont améliorés cliniquement, mais les signaux cérébraux n’ont pas suivi une trajectoire ascendante simple. Néanmoins, en montrant que les rythmes cérébraux pré‑entraînement sont liés aux gains ultérieurs, ce travail rapproche le domaine d’une neurorééducation prédictive et sur mesure qui exploite la plasticité résiduelle du cerveau.
Citation: Valente, M., Branco, D., Bermúdez i Badia, S. et al. EEG-based predictors of motor recovery during immersive VR-BCI rehabilitation. Sci Rep 16, 7870 (2026). https://doi.org/10.1038/s41598-026-39106-1
Mots-clés: rééducation après AVC, entraînement en réalité virtuelle, interface cerveau-ordinateur, biomarqueurs EEG, récupération motrice