Clear Sky Science · fr
La déficience en Dlgap2 perturbe l’homéostasie synaptique en favorisant la dégradation ubiquitine‑dépendante d’Itsn1 dans un modèle d’autisme induit par l’acide valproïque
Pourquoi un médicament courant et le câblage cérébral comptent
L’acide valproïque est un médicament utilisé depuis longtemps pour l’épilepsie et les troubles de l’humeur, mais son utilisation pendant la grossesse a été associée à un risque accru d’autisme chez les enfants. Cette étude pose une question urgente pour les familles et les cliniciens : que fait exactement ce médicament au câblage du cerveau en développement ? En retraçant les changements jusqu’à des molécules spécifiques aux synapses — les points de communication entre les neurones — les chercheurs dévoilent une nouvelle chaîne d’événements qui peut aider à expliquer des comportements de type autistique et orienter de futures stratégies thérapeutiques. 
Comparer les espèces pour repérer des points sensibles partagés
Pour trouver des indices fiables, l’équipe ne s’est pas appuyée sur un seul modèle animal. Ils ont comparé des cerveaux ou des tissus cérébraux simulés provenant d’organoïdes corticaux humains, de singes, de rats et de souris exposés à l’acide valproïque avant la naissance. À l’aide d’études à grande échelle des gènes et des protéines, ils ont identifié un petit ensemble de gènes modifiés dans tous ces systèmes, liés aux synapses et à la gaine des fibres nerveuses. Parmi eux, un a particulièrement retenu l’attention : Dlgap2, une protéine d’échafaudage qui aide à organiser la face postsynaptique des synapses excitatrices. Chez les souris exposées prénatalement à l’acide valproïque, les niveaux de Dlgap2 chutaient dans le cortex et, plus précisément, à l’intérieur de minuscules compartiments synaptiques, ce qui suggère que cette molécule de maintien de la structure est une victime clé de l’exposition au médicament.
Des changements moléculaires aux altérations comportementales
Les auteurs se sont ensuite demandé si la perte de Dlgap2, à elle seule, suffit à perturber la fonction cérébrale. Ils ont utilisé des virus porteurs d’ARN en épingle à cheveux pour réduire l’expression de Dlgap2 dans des neurones de souris en culture et chez des souriceaux nouveaux‑nés. En culture, les neurones avec moins de Dlgap2 développaient des ramifications plus courtes et présentaient moins de poncta postsynaptiques, signes de connexions affaiblies. Chez les animaux vivants, l’inhibition ciblée de Dlgap2 dans le cerveau a provoqué des comportements de type autistique : les jeunes mâles avaient des difficultés à apprendre l’emplacement d’une plateforme cachée dans un labyrinthe aquatique et montraient un manque d’intérêt pour des partenaires sociaux et pour la nouveauté sociale dans un test à trois compartiments. Ces altérations reproduisent les déficits d’apprentissage et sociaux observés chez les animaux exposés à l’acide valproïque, renforçant l’idée que la perte de Dlgap2 n’est pas un simple effet secondaire mais un moteur des modifications comportementales.
Trouver un partenaire vulnérable à la synapse
Pour comprendre comment la perte de Dlgap2 se répercute au sein de la synapse, les chercheurs ont examiné de plus près les protéines ancrées dans la densité postsynaptique, le coussinet moléculaire dense qui reçoit les signaux chimiques. Grâce à la protéomique, ils ont constaté que la réduction de Dlgap2 modifiait l’abondance de centaines de protéines synaptiques, en particulier celles impliquées dans l’organisation des synapses et le recyclage des vésicules par endocytose. Une protéine, Intersectin‑1 (Itsn1), a chuté de façon particulièrement marquée. Des analyses biochimiques supplémentaires ont montré que Dlgap2 et Itsn1 coexistent physiquement dans les mêmes complexes protéiques dans les fractions enrichies en synapses et que les deux figurent parmi les gènes associés à l’autisme. Cela indique un partenariat régulateur ciblé entre ces deux molécules au sein d’un paysage synaptique très dense. 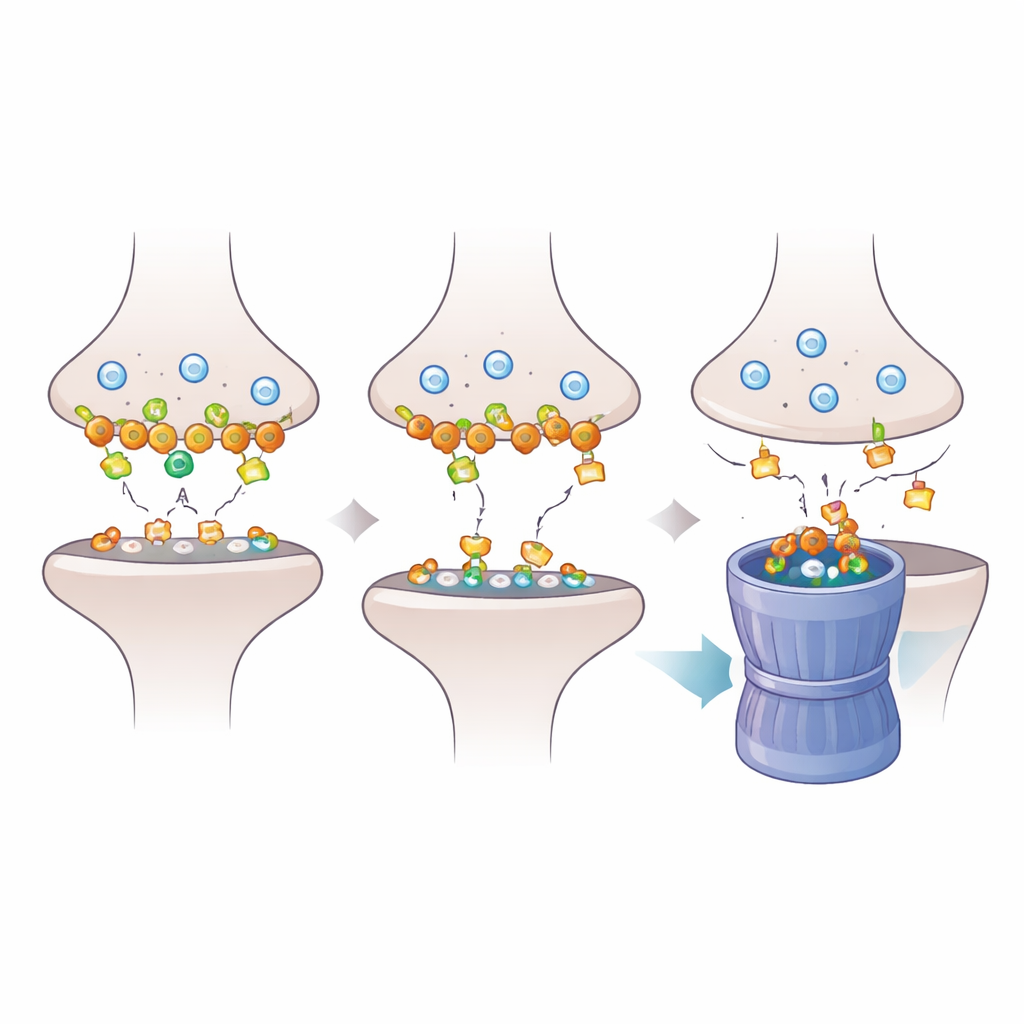
Une voie d’élimination cachée mise en lumière
L’équipe s’est ensuite demandé pourquoi les niveaux d’Itsn1 diminuent quand Dlgap2 fait défaut. Ils ont observé que, dans les compartiments synaptiques, l’inhibition de Dlgap2 déclenchait une forme d’étiquetage protéique connue sous le nom d’ubiquitination liée à K48, qui marque les protéines pour leur dégradation par le protéasome cellulaire, sorte de « broyeur ». Le blocage de ce système d’élimination avec le médicament MG132 a empêché la perte d’Itsn1, indiquant que Dlgap2 protège normalement Itsn1 contre ce marquage et cette destruction. Sans Dlgap2, Itsn1 est de plus en plus ciblée, dirigée vers le protéasome et appauvrie au niveau des synapses, compromettant le recyclage endocytique et l’équilibre de l’activité synaptique. Ce travail suggère que des variations subtiles de la vitesse de renouvellement des protéines clés peuvent déstabiliser les synapses pendant le développement cérébral.
Ce que cela signifie pour l’autisme et les traitements futurs
Dans l’ensemble, l’étude propose une idée simple mais puissante pour un public non spécialiste : l’exposition prénatale à l’acide valproïque peut affaiblir une protéine structurelle « d’étayage » (Dlgap2) aux synapses. Lorsque cet étai disparaît, sa protéine partenaire (Itsn1) devient excessivement ciblée par le système d’élimination cellulaire, entraînant un mauvais recyclage des composants synaptiques et, en fin de compte, des circuits mal câblés et des comportements de type autistique chez la souris. Bien que de nombreux gènes et facteurs environnementaux contribuent à l’autisme, cet axe Dlgap2–Itsn1 offre une chaîne moléculaire concrète reliant l’exposition prénatale à un médicament à l’altération de la fonction cérébrale. À long terme, des stratégies visant à préserver ce partenariat ou à ajuster le système d’élimination des protéines aux synapses pourraient aider à protéger les cerveaux en développement contre des formes similaires de perturbation.
Citation: Guo, X., Zhang, L. & Zhuang, K. Dlgap2 deficiency disrupts synaptic homeostasis by promoting ubiquitin-mediated Itsn1 degradation in a valproic acid-induced autism-like model. Sci Rep 16, 8305 (2026). https://doi.org/10.1038/s41598-026-39099-x
Mots-clés: acide valproïque et grossesse, protéines d’échafaudage synaptique, mécanismes du spectre autistique, voie protéasome‑ubiquitine, modèles murins d’autisme