Clear Sky Science · fr
Dépistage virtuel intégré, profilage ADMET et simulations de dynamique moléculaire de nouveaux inhibiteurs naturels de HDAC6 susceptibles d'atténuer la dégénérescence du muscle squelettique
Pourquoi il est important de protéger nos muscles
Le muscle squelettique ne sert pas seulement à soulever des poids ou à courir ; c’est le plus grand réservoir de protéines du corps, un moteur majeur du métabolisme et un élément essentiel des mouvements du quotidien. Lorsque les muscles s’atrophient en raison du vieillissement, de maladies ou d’inactivité, les personnes perdent en force, en autonomie et en qualité de vie. Cette étude explore une approche guidée par ordinateur pour découvrir de nouveaux candidats-médicaments issus de substances naturelles susceptibles de ralentir ou de prévenir ce type de perte musculaire en ciblant un commutateur moléculaire clé à l’intérieur des cellules musculaires.
Une protéine problématique dans l’affaiblissement des muscles
À l’intérieur des fibres musculaires, une protéine appelée HDAC6 contribue à organiser l’échafaudage interne et à la dégradation d’autres protéines. Dans des conditions normales, elle participe au maintien sain du muscle. Mais lorsque l’activité de HDAC6 devient excessive, elle déstabilise le réseau de microtubules qui soutient la forme du muscle et les connexions entre les nerfs et les fibres musculaires. Cette perturbation favorise l’endommagement des protéines et le rétrécissement du muscle. Des études animales ont montré qu’inhiber HDAC6 peut préserver la taille musculaire et améliorer la fonction, ce qui en fait une cible thérapeutique intéressante pour lutter contre l’atrophie musculaire.
À la recherche d’idées médicamenteuses dans la nature
Beaucoup d’inhibiteurs existants de HDAC6 ont été conçus synthétiquement et peuvent provoquer des effets indésirables ou manquer de précision pour cette cible spécifique. Les auteurs se sont donc tournés vers la diversité chimique naturelle, en partant du principe que les produits naturels possèdent souvent des structures qui interagissent de manière subtile mais efficace avec les protéines humaines. Ils ont exploité la collection SuperNatural 3.0, qui contient près d’un demi-million de composés naturels distincts, et posé une question simple : lesquels de ces molécules pourraient s’insérer dans la cavité active de HDAC6 de manière à l’inactiver tout en présentant des propriétés compatibles avec un médicament potentiel ? 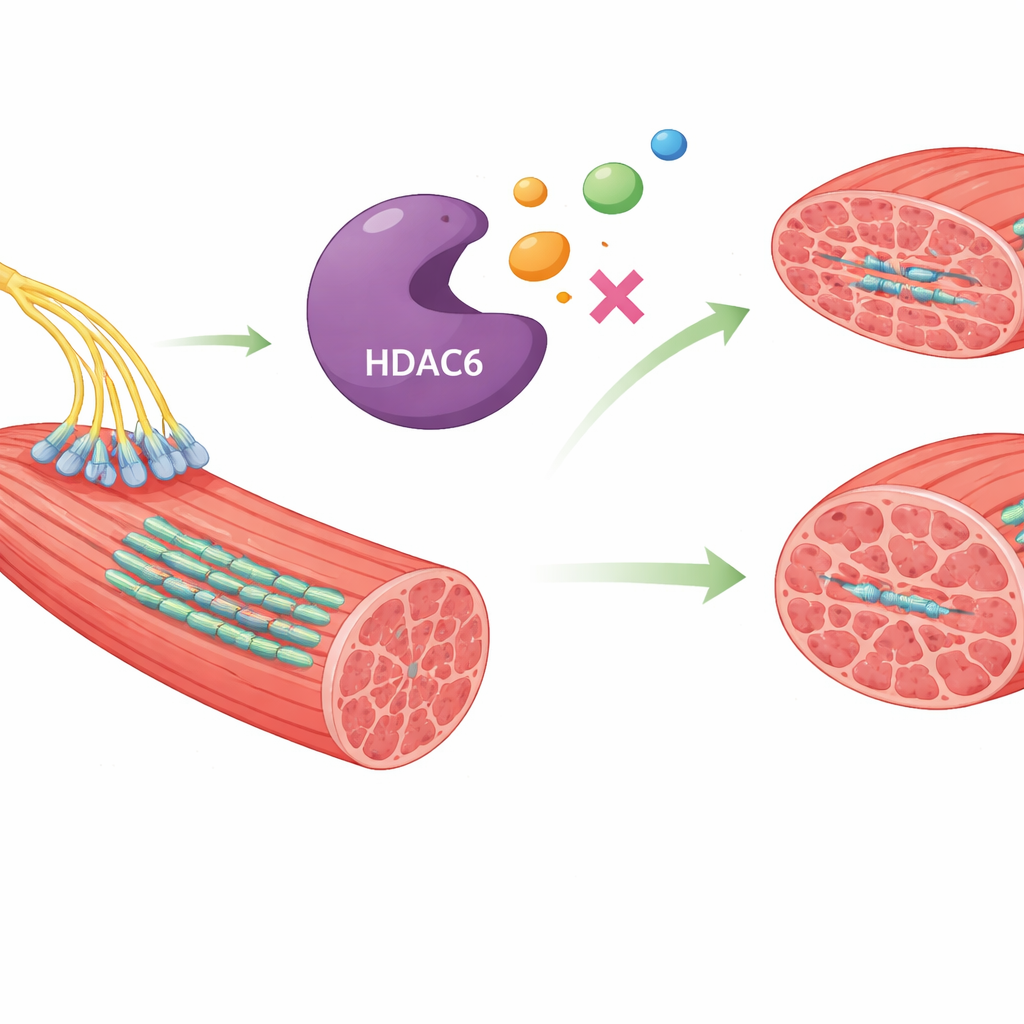
Criblage informatique à grande vitesse de centaines de milliers de molécules
Pour répondre à cette question, l’équipe a utilisé une chaîne de « criblage virtuel » intégrée. D’abord, ils ont préparé un modèle tridimensionnel détaillé du tunnel catalytique de HDAC6, fondé sur une structure expérimentale de l’enzyme liée à un inhibiteur connu. Puis, à l’aide de logiciels spécialisés, ils ont docké 449 058 composés naturels dans ce tunnel, en évaluant la qualité et la faveur de chaque ajustement. À partir de cet énorme pool initial, 146 molécules ont obtenu de meilleurs résultats que le médicament de référence trichostatine A. Les chercheurs ont ensuite appliqué une série de filtres simulant les critères des développeurs de médicaments : taille et polarité appropriées, capacité d’absorption intestinale, solubilité acceptable, toxicité prédite limitée et faisabilité réaliste de synthèse chimique. Après ces étapes, deux candidats se sont distingués, étiquetés SN0000021 et SN0000043.
Tester la stabilité et le comportement dans une cellule virtuelle
Trouver une bonne pose de docking ne suffit pas ; les candidats-médicaments doivent rester liés malgré le mouvement constant des systèmes biologiques réels. Pour étudier cela, l’équipe a exécuté de longues simulations de dynamique moléculaire, essentiellement des films haute résolution des complexes HDAC6–composé sur 200 milliardsièmes de seconde. Ils ont surveillé l’amplitude des mouvements du squelette protéique, la profondeur d’enfouissement de chaque composé dans le tunnel, son exposition à l’eau environnante et la compaction du complexe. Les deux composés naturels ont formé des interactions stables et durables avec des acides aminés clés connus pour contrôler l’activité de HDAC6. Ils ont présenté des fluctuations moindres et une compaction plus serrée que l’inhibiteur de référence, suggérant un ajustement plus robuste. Des calculs d’énergie avancés, estimant la faveur thermodynamique de la liaison, ont en outre confirmé que ces deux molécules sont susceptibles de se lier plus fortement que le médicament témoin. 
Des coups de cœur informatiques aux futurs médicaments préservant le muscle
Pour un non-spécialiste, la conclusion est simple : en n’utilisant que des outils informatiques, les chercheurs ont trié un catalogue immense de substances naturelles et identifié deux composés particulièrement prometteurs pour se lier et neutraliser HDAC6, une protéine liée à la fonte musculaire. Ces candidats non seulement se lient fortement dans les simulations, mais présentent aussi des profils prédits d’absorption, de distribution et de sécurité favorables, en faisant des points de départ prometteurs pour de nouveaux médicaments. Le travail ne prouve pas encore que ces molécules aideront les muscles réels ; cela nécessitera des tests en laboratoire sur l’enzyme purifiée, sur des cellules et sur des modèles animaux. Mais l’étude fournit une feuille de route puissante montrant comment le criblage numérique de produits naturels peut découvrir des thérapies potentielles pour protéger le muscle squelettique de la dégénérescence.
Citation: Ahmad, K., Ahmad, S.S. & Choi, I. Integrated virtual screening, ADMET profiling, and molecular dynamics simulations of novel natural HDAC6 inhibitors with the potential to ameliorate skeletal muscle degeneration. Sci Rep 16, 7840 (2026). https://doi.org/10.1038/s41598-026-39066-6
Mots-clés: atrophie du muscle squelettique, inhibition de HDAC6, découverte de médicaments à partir de produits naturels, criblage virtuel, régénération musculaire