Clear Sky Science · fr
Le casr des poissons-zèbres module la structure et la fonction cardiaques
Pourquoi le cœur des poissons est important pour la santé humaine
Nos cœurs dépendent du calcium, un minéral simple, pour battre correctement. Lorsque les signaux calciques déraillent, cela peut conduire à une insuffisance cardiaque ou à d’autres maladies graves. Cette étude utilise de minuscules poissons-zèbres—des poissons d’eau douce transparents couramment utilisés en laboratoire—pour explorer comment un détecteur de calcium dans les cellules influence la force et la survie du cœur. En désactivant un seul gène qui aide les cellules à détecter le calcium, les chercheurs ont mis au jour une chaîne de problèmes affectant la contraction cardiaque, la morphologie corporelle et même la vessie natatoire remplie d’air du poisson. Leurs travaux montrent également que le contexte génétique global d’un animal peut fortement atténuer ou aggraver l’impact d’une mutation délétère, une leçon qui résonne clairement en médecine humaine.
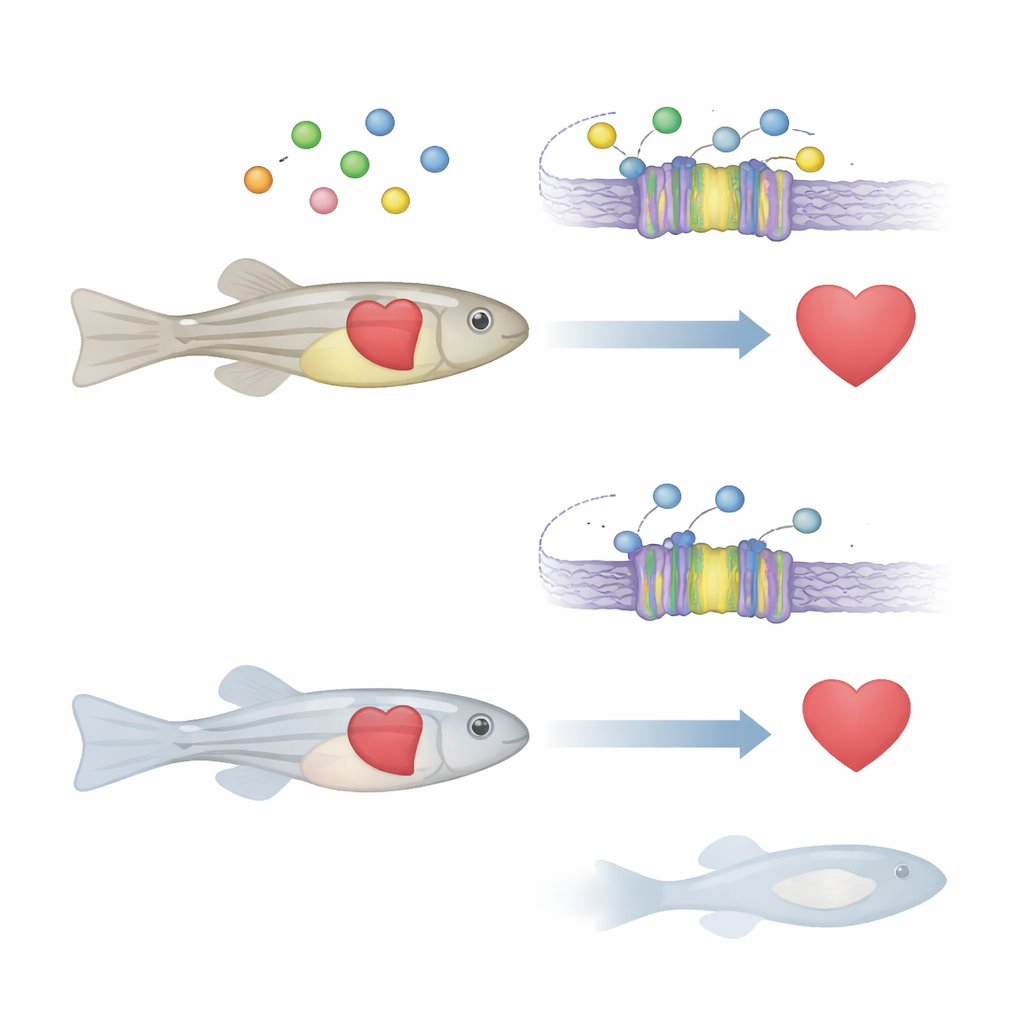
Un « thermostat » cellulaire pour le calcium
Le calcium à l’intérieur et à l’extérieur des cellules agit comme un signal universel qui commande le mouvement musculaire, la libération d’hormones et même l’activation de certains gènes. De nombreux organes dépendent d’une protéine appelée récepteur sensible au calcium, qui fonctionne comme un thermostat des niveaux de calcium. Lorsque le calcium extracellulaire varie, ce récepteur ajuste la sécrétion hormonale et d’autres processus pour rétablir l’équilibre. Chez l’humain, des défauts de ce récepteur sont déjà associés à des troubles osseux et minéraux, et il est suspecté de participer aux maladies cardiaques et à certains cancers. Cependant, la façon dont ce senseur calcique influence le développement et la fonction cardiaque au niveau d’un organisme entier restait incertaine.
Que se passe-t-il lorsque le senseur calcique est désactivé
L’équipe s’est concentrée sur la version poisson-zèbre de ce gène, appelée casr, fortement conservée avec son homologue humain. En utilisant des outils d’édition génétique modernes, ils ont créé des poissons-zèbres dont les deux copies de casr étaient inactivées. Au début, les jeunes poissons semblaient presque normaux. Mais à partir de cinq jours après la fécondation, de nombreux mutants n’ont pas réussi à gonfler leur vessie natatoire, un petit organe rempli de gaz qui contrôle la flottabilité. Ces poissons coulaient au fond, nageaient mal, développaient rapidement une courbure de la colonne vertébrale et mouraient tous avant deux semaines. Ces signes externes indiquaient de graves problèmes internes affectant plusieurs systèmes d’organes.
Un cœur plus faible, plus petit et plus lent
Des vidéos à haute vitesse et l’analyse d’images des battements cardiaques ont révélé à quel point l’absence du senseur calcique affectait la performance cardiaque. Chez les larves de poisson-zèbre normales, le ventricule cardiaque se remplit et se vide selon un rythme fort et régulier. Chez les mutants, le ventricule était nettement plus petit lors du remplissage, le cœur battait plus lentement et chaque battement éjectait moins de sang. Les mesures de la diminution de la longueur du muscle cardiaque et des variations de surface de la cavité de pompage à chaque battement étaient toutes deux réduites, témoignant d’une contraction affaiblie. Le débit cardiaque global — le volume de sang déplacé par minute — chutait fortement. Au niveau des gènes, des centaines de transcrits variaient, et des réseaux clés contrôlant la gestion du calcium et la machinerie de la contraction musculaire étaient réprimés, reliant l’édition génique tant à une défaillance moléculaire qu’à une défaillance mécanique du cœur.
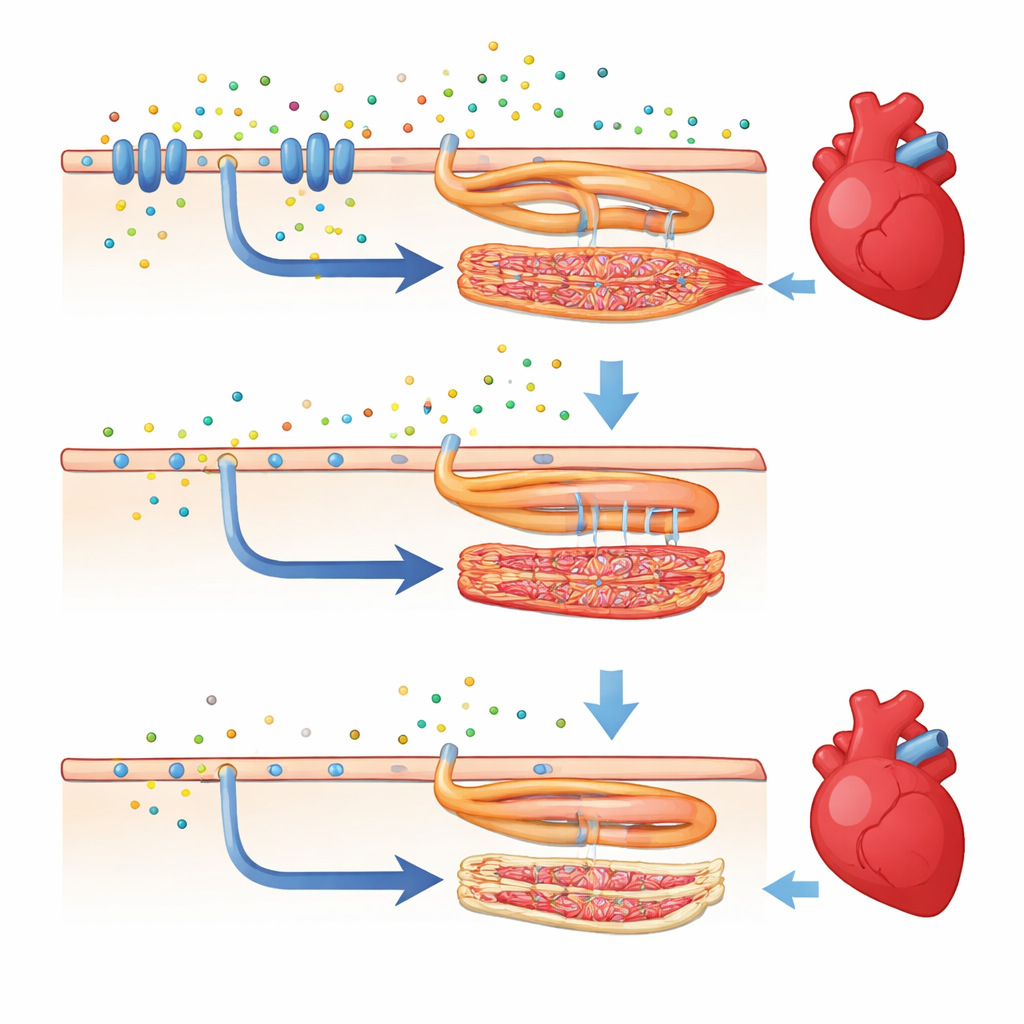
Comment les gènes de fond peuvent sauver un cœur malade
De façon surprenante, la même mutation de casr se comportait très différemment dans une autre souche courante de poisson-zèbre, connue sous le nom de TL (Tupfel long-fin). Lorsque l’extinction du gène a été introduite dans ce nouveau contexte génétique, les poissons ont pu gonfler leur vessie natatoire, survivre à l’âge adulte et présentaient une fonction de pompage bien meilleure. Leurs cœurs restaient quelque peu compromis — la fréquence cardiaque demeurait plus basse que la normale — mais les mesures de la force de contraction ventriculaire et du volume de sang pompé par minute approchaient presque celles des poissons sains. Chez ces animaux « sauvés », de nombreux gènes liés à la signalisation calcique et à la contraction du muscle cardiaque retrouvaient des niveaux intermédiaires, supérieurs à ceux de la lignée initiale malade. Cela révèle que d’autres gènes dispersés dans le génome peuvent tamponner ou intensifier l’impact d’une variation délétère.
Signaux qui façonnent le cœur et la flottabilité
Au‑delà du cœur, la perte du senseur calcique perturbait aussi d’importants systèmes de contrôle de la croissance de l’embryon. Les gènes des voies de signalisation Wnt et Hedgehog — de célèbres architectes de la formation des organes — étaient abaissés chez les mutants. Ces changements contribuent probablement à l’échec d’inflation de la vessie natatoire, qui peut à son tour aggraver la survie en compliquant l’alimentation et la mobilité du poisson. Les marqueurs de différenciation des cellules du muscle cardiaque étaient également réduits et les ventricules étaient plus petits, suggérant que le senseur calcique participe à l’orientation de la croissance et de la maturation des cellules cardiaques.
Ce que cela signifie pour comprendre le risque de maladie
Pris ensemble, ces travaux montrent que le récepteur sensible au calcium est un gardien crucial de la fonction cardiaque et du développement organique adéquat chez le poisson-zèbre. Lorsque ce senseur est perdu, les signaux calciques défaillent, le muscle cardiaque se contracte faiblement, la vessie natatoire ne se gonfle pas et les animaux meurent jeunes. Pourtant, le sauvetage spectaculaire observé dans une autre souche génétique souligne un message clé : le reste du génome peut fortement modifier la dangerosité réelle d’une mutation donnée. Pour la santé humaine, cela explique pourquoi des personnes porteuses de variants génétiques similaires à risque peuvent avoir des résultats très différents, et pourquoi comprendre à la fois les gènes centraux de la maladie et leur contexte génétique est essentiel pour prédire et traiter les affections cardiaques.
Citation: Liu, L., Hu, Y., Xie, B. et al. Zebrafish casr modulates cardiac structure and function. Sci Rep 16, 8543 (2026). https://doi.org/10.1038/s41598-026-39063-9
Mots-clés: signalisation calcique, développement cardiaque, modèle poisson-zèbre, contexte génétique, fonction cardiaque