Clear Sky Science · fr
La transmission des forces de traction via un hydrogel matriciel bioactif favorise la migration collective des épithéliums médiée par l’intégrine
Comment les cellules tirent ensemble pour réparer
Lorsque vous vous coupez la peau ou endommagez un organe, des feuillets cellulaires doivent se déplacer de façon coordonnée pour refermer la blessure. Cette étude pose une question apparemment simple : quand les cellules rampent ensemble, se contentent-elles de se tirer les unes sur les autres, ou « parlent‑elles » aussi à travers le matériau mou qui les soutient ? En recréant en laboratoire un environnement gélifié réaliste, les auteurs montrent que les cellules peuvent transmettre des forces mécaniques à travers cette matrice souple pour orienter le mouvement du groupe, révélant un niveau de communication caché qui pourrait être crucial pour la cicatrisation, la réparation tissulaire et même la dissémination du cancer.
Un sol souple qui transmet la force
Dans notre corps, de nombreuses cellules reposent sur un échafaudage protéique souple plutôt que sur une surface rigide comme du verre ou du plastique. Pour imiter cela, les chercheurs ont cultivé des cellules épithéliales rénales en feuillet continu sur un hydrogel bioactif composé de Matrigel et de collagène, deux composants courants des tissus naturels. Ils ont ensuite créé une petite zone vide au centre du gel, comme une minuscule blessure, et ont observé le feuillet cellulaire avancer pour combler l’écart. Pour suivre l’activité d’une voie de signalisation clé à l’intérieur des cellules, ils ont utilisé un biosenseur fluorescent qui rend compte de l’activité d’ERK, une protéine souvent responsive aux indices mécaniques. Ce dispositif leur a permis de voir, en temps réel, comment les forces mécaniques dans le gel souple se relient à la fois au mouvement cellulaire et à la signalisation interne. 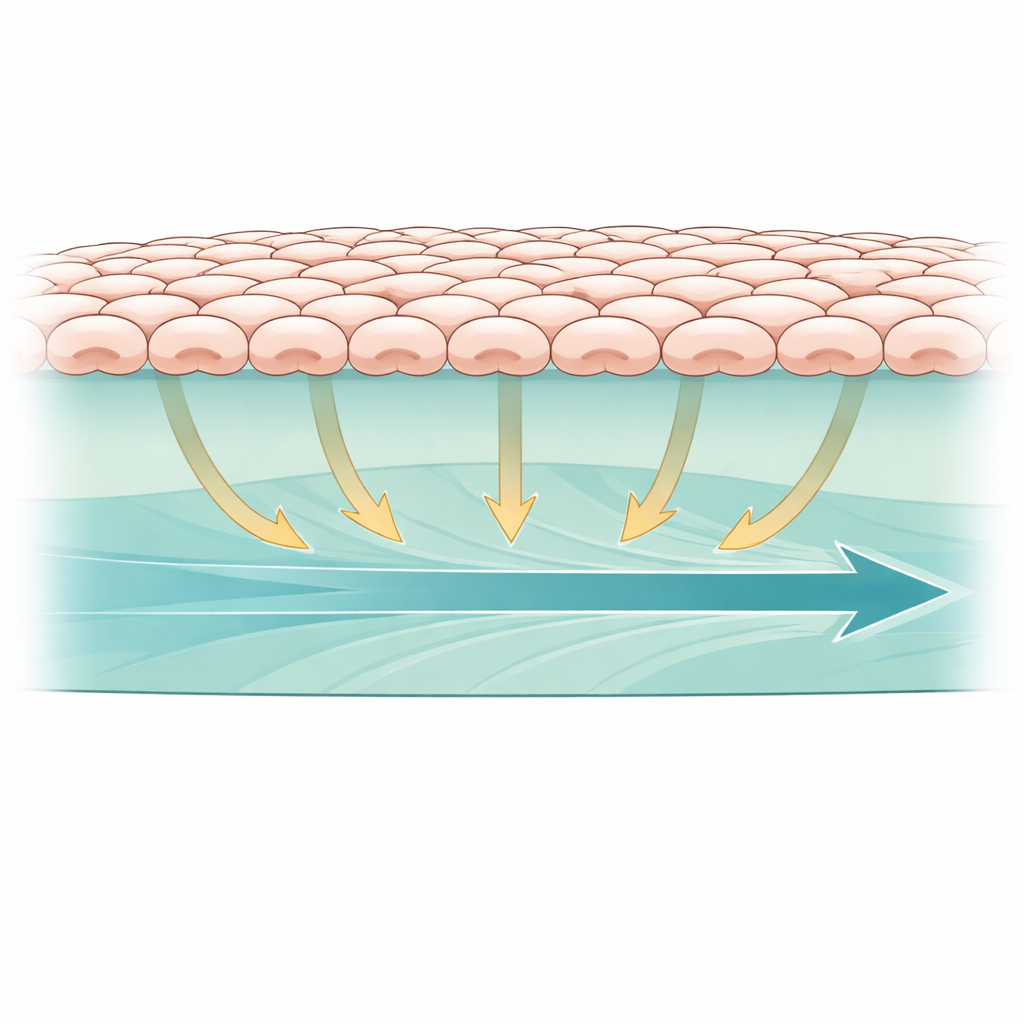
Observer le sol bouger sous les cellules
Pour savoir si le gel supportait et transmettait effectivement la force, l’équipe a mélangé de minuscules billes magnétiques dans la matrice et a suivi leur mouvement pendant la migration cellulaire. Sur le gel normal contenant à la fois Matrigel et collagène, les billes glissaient lentement vers l’avant dans la même direction que le feuillet cellulaire avancé, indiquant que les cellules agrippaient et tiraient la matrice sous elles. Sur des gels composés uniquement de Matrigel, les billes se déplaçaient plus lentement, suggérant une transmission de force plus faible. Lorsque le gel était chimiquement réticulé au glutaraldéhyde pour rigidifier et « verrouiller » le réseau, les billes bougeaient à peine. Dans ces conditions verrouillées, les cellules restaient attachées mais leur progression collective ralentissait considérablement, et le signal ERK devenait plus faible et moins concentré en bordure avancée, liant une forte traction sur la matrice à un mouvement de groupe plus rapide et mieux dirigé.
Moteurs internes et portails ioniques qui alimentent le mouvement
Les auteurs ont ensuite sondé ce qui, à l’intérieur des cellules, génère ces forces de traction et comment cette activité est perçue. Ils ont utilisé des médicaments pour bloquer la contraction basée sur la myosine, le même type de machinerie moléculaire qui alimente les muscles. Lorsque la contraction était inhibée, l’activité d’ERK chutait et le feuillet cellulaire avançait plus lentement, ce qui est cohérent avec l’idée que la traction interne est nécessaire pour transmettre la tension à la matrice. Ils ont également perturbé plusieurs types de canaux calciques dans la membrane cellulaire et les réserves calciques internes. Le blocage de ces voies ioniques atténuait l’activité d’ERK et ralentissait la migration collective, indiquant une chaîne d’événements dans laquelle le tiraillement mécanique sur la matrice est converti en signaux calciques et ERK qui contribuent à maintenir le groupe en mouvement coordonné.
Orienter la direction via des ancrages de surface
Une découverte particulièrement marquante provient du ciblage des intégrines, ces molécules de surface qui agissent comme de minuscules ancres reliant les cellules à leur environnement. Lorsque les chercheurs ont bloqué un sous‑type majeur d’intégrine, le feuillet n’avançait plus comme un front cohérent, même si des cellules individuelles pouvaient encore se remuer localement à une vitesse proche de la normale. Parallèlement, le mouvement des billes dans le gel s’est presque arrêté, montrant que les intégrines sont essentielles pour transmettre la force des cellules contractiles à la matrice. En revanche, le blocage des canaux mécanosensibles liés à Piezo1, qui aident les cellules à ressentir la pression physique, réduisait à la fois le rythme de migration et la traction observée dans le gel. Ensemble, ces résultats dessinent un schéma dans lequel la contraction génère la force, les intégrines la transmettent à la matrice, et les canaux mécanosensibles ainsi que la signalisation ERK interprètent cette force pour coordonner la direction et l’efficacité du mouvement collectif. 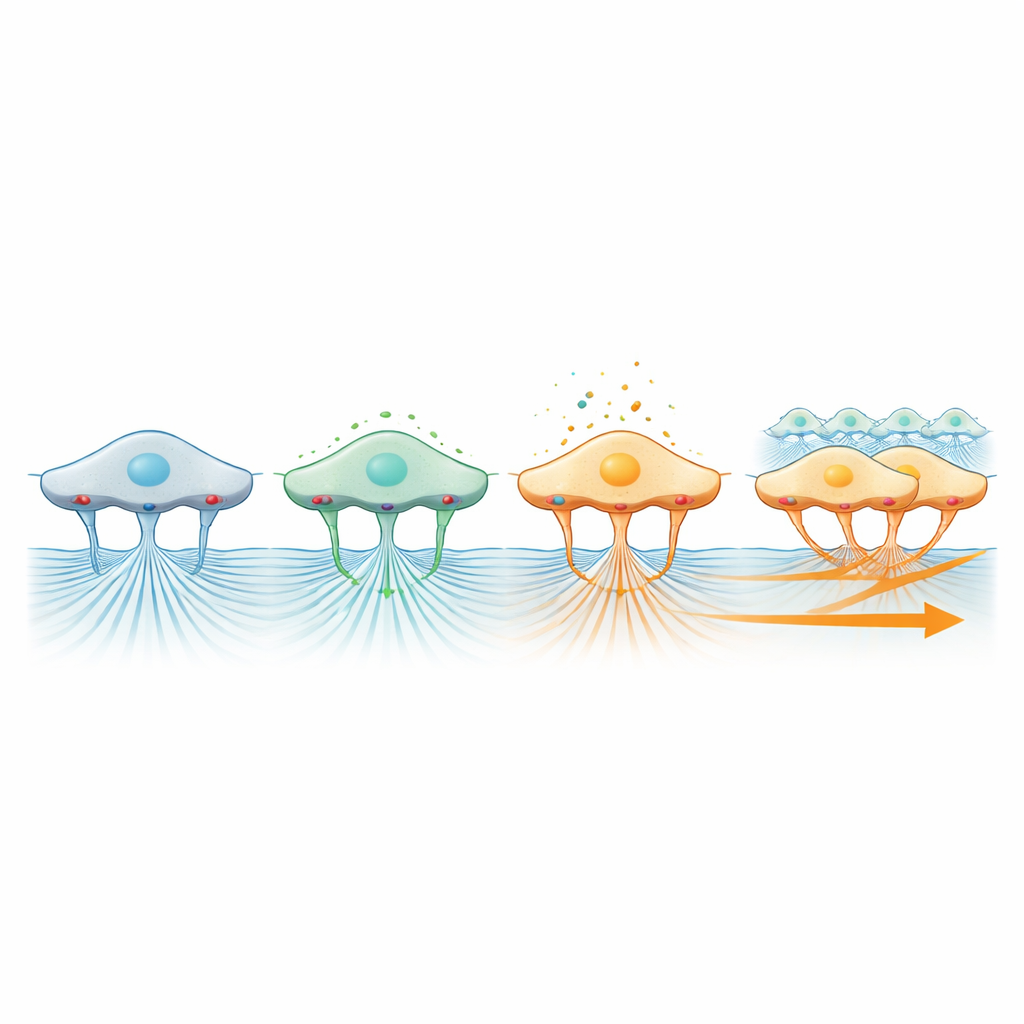
Pourquoi cela compte pour la réparation et la maladie
En termes simples, ce travail montre que les feuillets cellulaires ne se contentent pas de se tirer les uns sur les autres ; ils tirent aussi sur le matériau mou qui les soutient, et à travers lui, en l’utilisant comme une sorte de ligne téléphonique mécanique. Les contractions de la couche cellulaire transmettent de la tension à travers la matrice, et cette tension, détectée via les intégrines et les canaux ioniques et retranscrite par l’activité d’ERK, aide le groupe à se déplacer rapidement et dans une direction unifiée. Lorsque la matrice est chimiquement verrouillée de sorte que les forces ne peuvent pas se propager, ou lorsque les ancrages et capteurs de surface clés sont bloqués, la marche collective s’essouffle. Ces connaissances approfondissent notre compréhension de la fermeture des plaies, de la maintenance de la structure tissulaire et de la manière dont des groupes cellulaires invasifs, comme ceux impliqués dans le cancer et la fibrose, pourraient exploiter des voies mécaniques de leur environnement pour se propager.
Citation: Ouyang, M., Cao, Y., Sheng, H. et al. Traction force transmission via bioactive matrix hydrogel promotes epithelial collective migration mediated by integrin. Sci Rep 16, 8923 (2026). https://doi.org/10.1038/s41598-026-39048-8
Mots-clés: migration cellulaire collective, signalisation mécanique, matrice extracellulaire, intégrine, cicatrisation