Clear Sky Science · fr
Identification in silico d’antagonistes inhalables de petite taille ciblant IL-33/ST2 pour les endotypes d’asthme sévère de type 2 élevé
Pourquoi cela compte pour la respiration
Pour des millions de personnes atteintes d’asthme sévère, même les inhalateurs modernes et les injections avancées laissent souvent un essoufflement persistant et un risque d’attaques dangereuses. Cette étude examine si des médicaments familiers, de type comprimé, pourraient être repensés pour être administrés par inhalation afin de bloquer un des signaux « d’alarme » en amont de l’asthme dans les poumons. En n’utilisant que des simulations informatiques, les chercheurs ont recherché de petites molécules susceptibles de se loger sur un récepteur clé impliqué dans l’asthme sévère d’origine allergique, jetant les bases d’essais en laboratoire futurs plutôt que de proposer un médicament prêt à l’emploi.
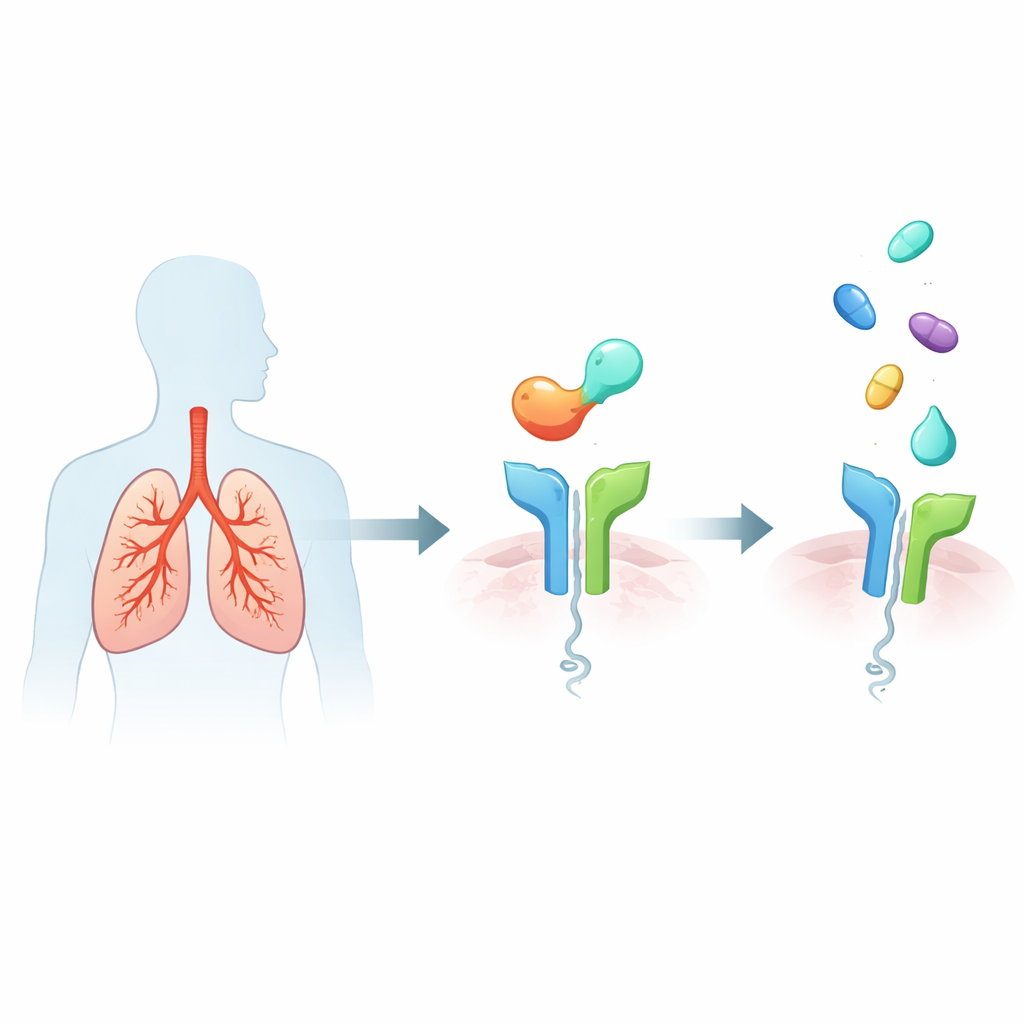
Le système d’alarme à l’intérieur des poumons asthmatiques
L’asthme sévère de type 2 élevé se caractérise par une réponse immunitaire hyperactive qui remplit les voies respiratoires de mucus et de cellules inflammatoires, rétrécit les conduits respiratoires et endommage la structure pulmonaire au fil du temps. Un déclencheur majeur est une protéine appelée IL-33, libérée par les cellules de la muqueuse respiratoire stressées. IL-33 se fixe sur un récepteur nommé ST2 présent sur diverses cellules immunitaires, qui libèrent alors de puissants messagers conduisant aux manifestations caractéristiques de l’asthme, comme la respiration sifflante, les exacerbations et le remodelage chronique des voies aériennes. Comme une activité IL-33/ST2 accrue est associée à des symptômes plus graves et à des attaques plus fréquentes, ST2 est apparu comme une cible en amont attrayante : bloquer ST2 pourrait apaiser simultanément de nombreux signaux inflammatoires en aval.
Des anticorps aux médicaments de tous les jours
Plusieurs thérapies actuelles contre l’asthme sévère utilisent des anticorps injectables qui neutralisent des protéines inflammatoires dans le sang ou bloquent leurs récepteurs. Bien qu’efficaces chez certains patients, ces médicaments biologiques sont coûteux, doivent être administrés par injection et ciblent principalement des signaux plus en aval de la cascade. En revanche, des petites molécules — plus proches des comprimés ou des formes inhalées traditionnelles — pourraient être produites à grande échelle, stockées facilement et potentiellement délivrées directement dans les poumons. Le défi vient du fait que ST2 lie IL-33 via une large interface protéine–protéine, laquelle est plus difficile à perturber par de petites molécules que ne le serait une poche profonde sur une enzyme. Les auteurs se sont donc appuyés sur des données structurales haute résolution du complexe ST2–IL-33 et sur des outils in silico modernes pour vérifier si certains médicaments anti-inflammatoires connus pourraient, de façon inattendue, se fixer sur une partie de cette interface.
Explorer la surface du récepteur par ordinateur
En utilisant la structure cristalline humaine de ST2 liée à IL-33, l’équipe a d’abord retiré IL-33 pour exposer la surface de liaison du récepteur, puis a utilisé un programme de détection de poches pour repérer la région la plus prometteuse où une petite molécule pourrait se loger. Ils ont ensuite sélectionné dix petites molécules cliniquement pertinentes déjà utilisées dans l’asthme ou des maladies immunitaires apparentées — comme les bloqueurs des leucotriènes Montélukast et Zafirlukast, des dérivés immunomodulateurs de la thalidomide, et des inhibiteurs de JAK — ainsi qu’une molécule axée sur ST2 déjà rapportée comme référence. Avec un logiciel de docking virtuel, chaque composé a été positionné des milliers de fois sur la surface de ST2, et les poses les mieux ajustées ont été notées selon la force de liaison prédite. La Zafirlukast est ressortie comme l’ossature la mieux classée, devançant légèrement le Montélukast et le comparateur connu dirigé vers ST2.
Ajuster une molécule candidate à l’écran
Parce que la Zafirlukast présentait le meilleur compromis entre affinité prédite et propriétés pharmaceutiques générales, les auteurs ont utilisé un outil de conception assistée par IA pour créer une version modifiée de cette molécule. L’objectif était de conserver son ancrage sur ST2 tout en améliorant son profil de sécurité prédit. L’analogue redessiné avait un score de docking très similaire et était prédit comme moins toxique in silico. Les cartes de contacts détaillées suggéraient que le composé parent et le composé modifié touchaient plusieurs des mêmes acides aminés de ST2 qui contactent normalement IL-33, laissant entendre qu’ils occupent des régions fonctionnellement importantes de l’interface. Des simulations étendues de dynamique moléculaire — une demi-microseconde de mouvement virtuel en milieu aqueux et salin — ont montré que le récepteur et le ligand restaient tous deux flexibles, la petite molécule explorant différentes positions le long de la surface plutôt que de se verrouiller rigidement. Les calculs des énergies d’interaction au cours du temps ont indiqué une association significative mais dynamique, compatible avec une molécule sondant une surface protéine–protéine relativement plate.
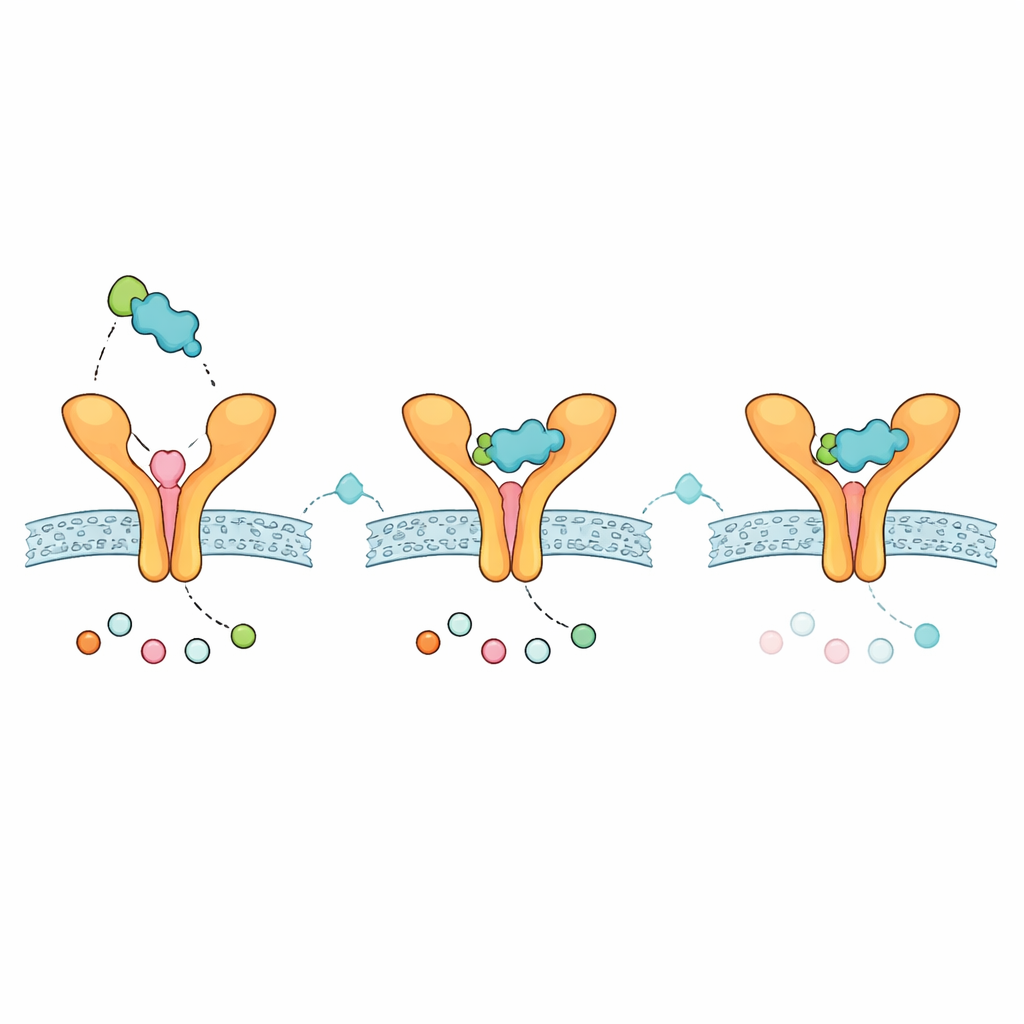
Indices sur le comportement possible d’un futur inhalateur
Pour évaluer si la Zafirlukast modifiée pourrait plausiblement fonctionner comme médicament, l’équipe a effectué des contrôles computationnels standard d’absorption, distribution, métabolisme, excrétion et toxicité. L’analogue respectait les règles courantes de drug-likeness pour l’administration orale, présentait une taille et une liposolubilité modérées, et était prédit pour ne pas pénétrer dans le cerveau — des caractéristiques potentiellement favorables pour un traitement ciblé sur les poumons avec des effets systémiques réduits. Les estimations de solubilité variaient selon le modèle, impliquant qu’une formulation soignée serait nécessaire, en particulier pour des voies non orales comme l’inhalation. Le composé était également prédit comme interagissant avec certaines enzymes hépatiques, ce qui suggère que des interactions médicamenteuses potentielles devraient être prises en compte s’il devait un jour être utilisé en association avec d’autres médicaments.
Ce que montre réellement ce travail
Plutôt que de fournir un nouveau médicament contre l’asthme, cette étude démontre une stratégie computationnelle étape par étape pour identifier et affiner de petites molécules susceptibles d’interférer avec le système d’alarme IL-33/ST2 à la surface des cellules des voies aériennes. Elle met en évidence la Zafirlukast et un parent optimisé par IA comme points de départ plausibles pour des expériences en laboratoire, montrant qu’elles peuvent occuper des parties clés de l’interface ST2 et présenter des propriétés prédites de sécurité et de drug-likeness globalement acceptables. Cependant, toutes les preuves sont virtuelles : le travail ne prouve pas que ces molécules empêchent IL-33 de se lier à ST2, n’atténuent la signalisation inflammatoire ni n’améliorent la respiration des patients. Ces réponses nécessiteront des tests biochimiques, des études cellulaires, des modèles animaux, puis des essais cliniques. Pour l’heure, l’étude offre une feuille de route computationnelle et une courte liste d’ossatures candidates pour les chercheurs souhaitant transformer le propre commutateur d’alarme de l’asthme en une cible médicamenteuse inhalable et pratique.
Citation: Sun, G., Liu, Q., Yu, M. et al. In Silico identification of inhalable small-molecule IL-33/ST2 antagonists for severe type-2-high asthma endotypes. Sci Rep 16, 7996 (2026). https://doi.org/10.1038/s41598-026-39027-z
Mots-clés: asthme sévère, voie IL-33 ST2, antagonistes de petite taille, conception de médicaments in silico, traitements inhalés