Clear Sky Science · fr
Analyse du mécanisme et de la valeur pronostique de PRKCQ-AS1 dans l’inhibition de la progression de l’adénocarcinome pulmonaire via la régulation de la voie PD-1/PD-L1
Pourquoi cette molécule cachée compte
L’adénocarcinome pulmonaire est la forme la plus fréquente de cancer du poumon et, malgré les progrès de l’immunothérapie moderne, trop de patients voient leur maladie récidiver ou résister au traitement. Cette étude se concentre sur une molécule d’ARN peu connue, PRKCQ-AS1, qui ne code pas de protéines mais pourrait influer discrètement sur la capacité du système immunitaire à contrôler ou non la croissance tumorale. Comprendre cet acteur invisible pourrait ouvrir de nouvelles voies pour un pronostic plus précoce et une meilleure utilisation de l’immunothérapie.
Un signal discret dans les tumeurs pulmonaires
Les chercheurs ont commencé par exploiter une vaste base de données publique sur le cancer pour mesurer la présence de PRKCQ-AS1 dans des échantillons tumoraux de centaines de personnes atteintes d’adénocarcinome pulmonaire. Ils ont constaté que cet ARN est systématiquement plus faible dans les tissus tumoraux que dans le poumon normal, et que son niveau diminue encore à mesure que les tumeurs progressent vers des stades plus avancés. Les patients dont les tumeurs présentaient moins de cet ARN avaient tendance à avoir un pronostic plus défavorable, ce qui suggère que PRKCQ-AS1 agit davantage comme un frein naturel au cancer que comme un moteur. L’équipe a ensuite confirmé ce schéma sur des échantillons de patients prélevés en clinique, renforçant l’idée que PRKCQ-AS1 pourrait servir d’indicateur utile d’une maladie agressive.
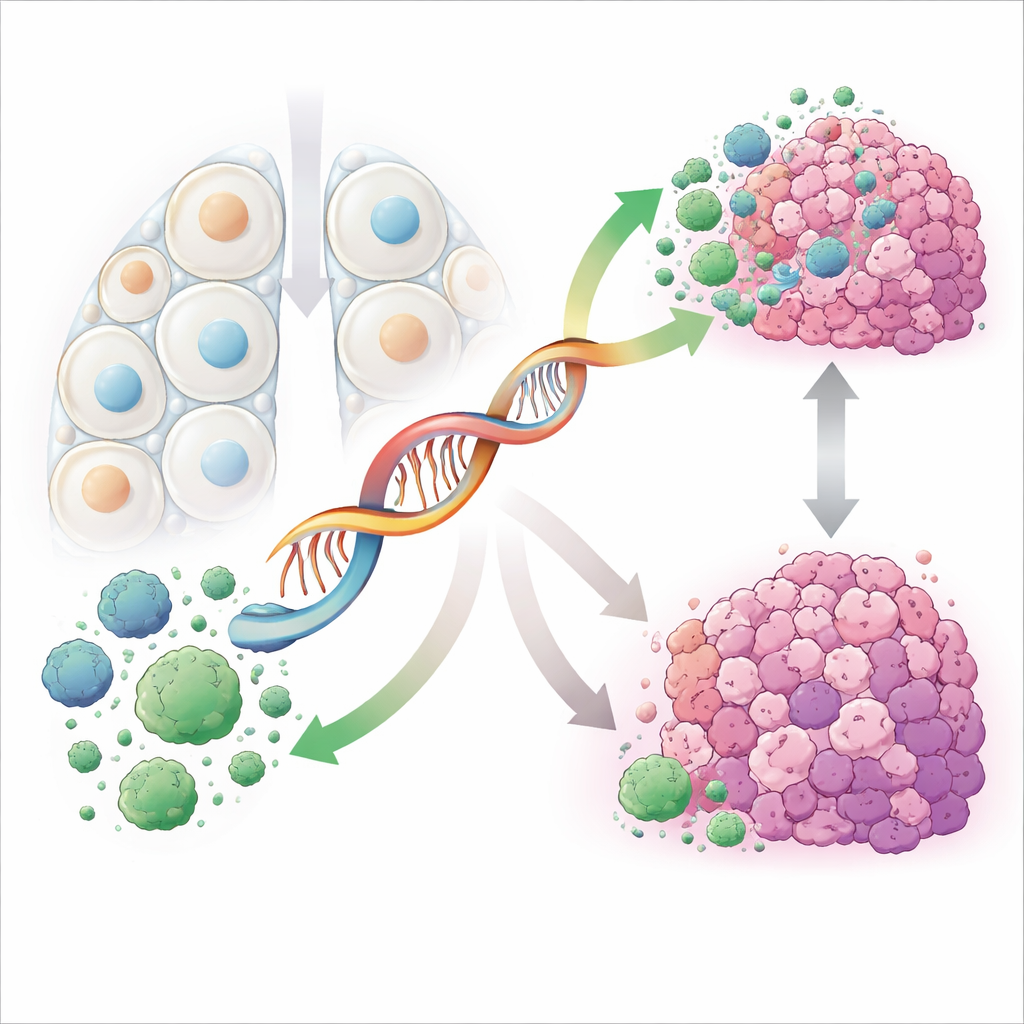
Explorer comment la molécule influence le comportement des cellules cancéreuses
Pour passer des tendances de la base de données à la biologie, les scientifiques ont utilisé des cellules d’adénocarcinome pulmonaire cultivées en laboratoire. Ils ont artificiellement augmenté ou diminué les niveaux de PRKCQ-AS1 et observé la réponse des cellules. Lorsque cet ARN était réduit, les cellules cancéreuses proliféraient plus rapidement, migraient plus aisément à travers des barrières artificielles et envahissaient davantage les membranes. Parallèlement, moins de cellules subissaient la mort cellulaire programmée, le processus d’autodestruction qui aide normalement à éliminer les cellules endommagées. L’augmentation de PRKCQ-AS1 produisait l’effet inverse : la croissance ralentissait, la migration et l’invasion diminuaient, et davantage de cellules mouraient. Ensemble, ces expériences montrent que PRKCQ-AS1 freine directement plusieurs comportements caractéristiques qui rendent les tumeurs pulmonaires dangereuses.
Liens avec les défenses de l’organisme
L’étude s’est également intéressée à la façon dont cet ARN pourrait influencer l’environnement plus large autour de la tumeur, en particulier les cellules immunitaires qui surveillent la croissance anormale. À l’aide d’outils computationnels, les auteurs ont construit une carte régulatrice reliant PRKCQ-AS1 à d’autres molécules d’ARN et gènes impliqués dans le cancer et l’immunité. Ils ont constaté que les gènes associés à cet ARN se regroupent dans des voies liées aux réponses immunitaires et à la signalisation cellulaire. Dans les données patientes, les tumeurs présentant davantage de PRKCQ-AS1 avaient tendance à contenir des niveaux plus élevés de certaines cellules immunitaires bénéfiques, notamment des lymphocytes T cytotoxiques capables de détruire directement les cellules cancéreuses. Les tumeurs avec peu de PRKCQ-AS1 présentaient une composition immunitaire différente, potentiellement moins efficace ou même épuisée, laissant entendre que cet ARN contribue à façonner un microenvironnement tumoral plus ou moins favorable aux défenses de l’organisme.
Contrôler un point de contrôle immunitaire clé
Un des mécanismes de défense les plus puissants utilisés par les tumeurs pour survivre est le système de point de contrôle PD-1/PD-L1, qui agit comme un déguisement moléculaire indiquant aux cellules immunitaires de cesser l’attaque. Les médicaments d’immunothérapie modernes bloquent ce signal. Les auteurs ont découvert une forte corrélation entre PRKCQ-AS1 et ce point de contrôle. Dans les tissus de patients et dans des cultures cellulaires, de faibles niveaux de PRKCQ-AS1 s’associaient à des niveaux plus élevés de PD-1 et PD-L1, tandis que l’augmentation de cet ARN réduisait ces signaux de point de contrôle. Cela suggère que lorsque PRKCQ-AS1 est abondant, les cellules tumorales affichent moins de signaux « ne pas attaquer » à leur surface, les rendant plus visibles pour les cellules immunitaires. À l’inverse, la carence en PRKCQ-AS1 rend le point de contrôle plus actif, facilitant la dissimulation des tumeurs face à l’attaque immunitaire et leur croissance continue.
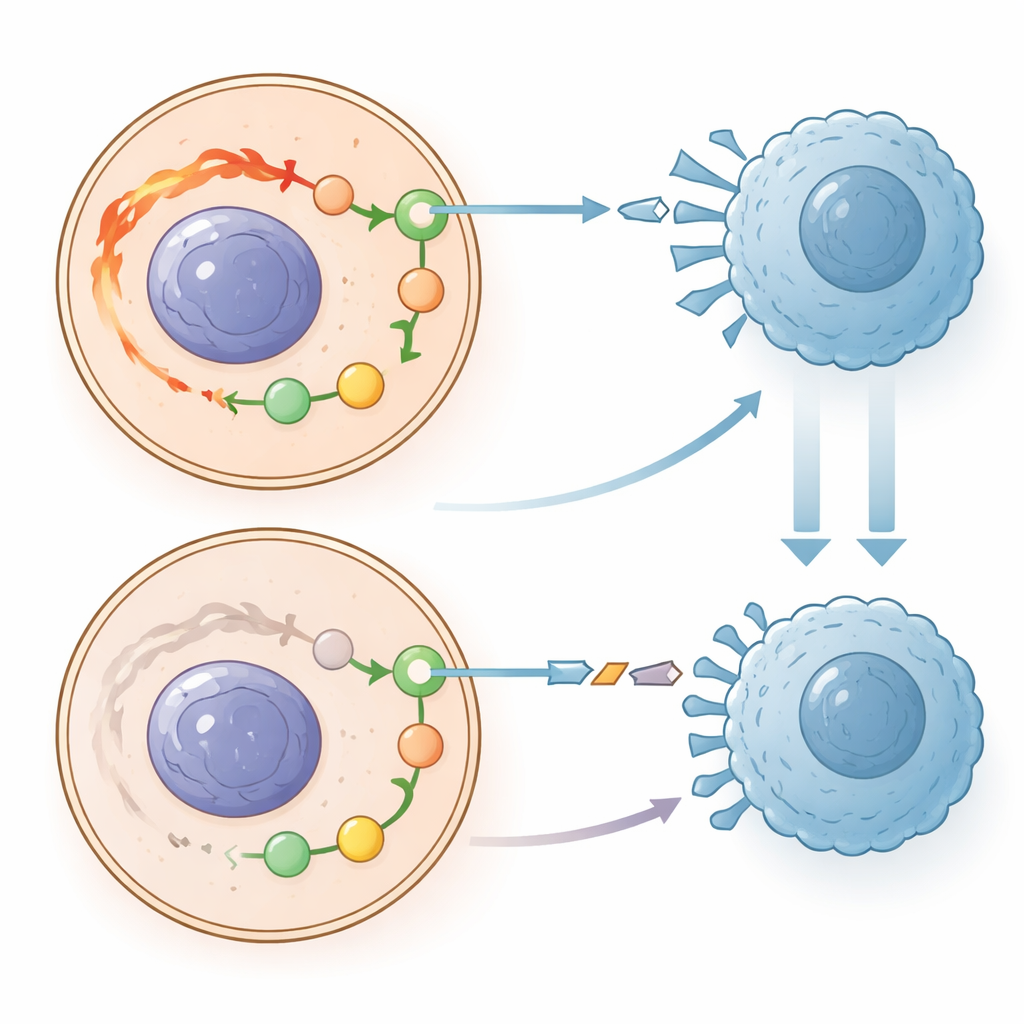
Ce que cela pourrait signifier pour la prise en charge future
Bien que ce travail repose encore sur des modèles cellulaires et un groupe clinique relativement restreint, il désigne PRKCQ-AS1 comme un suppresseur tumoral naturel dans l’adénocarcinome pulmonaire. En limitant la croissance des cellules cancéreuses et en atténuant une voie clé d’échappement immunitaire, cet ARN non codant pourrait influencer à la fois la vitesse de progression tumorale et la réponse à l’immunothérapie. À l’avenir, la mesure de PRKCQ-AS1 pourrait aider les médecins à estimer le pronostic d’un patient, et des traitements visant à restaurer ou à mimer son activité pourraient renforcer l’efficacité des thérapies immunitaires. Pour l’instant, cette étude apporte un élément important pour comprendre pourquoi certains cancers du poumon résistent aux défenses de l’organisme—et offre une nouvelle cible moléculaire pour les combattre.
Citation: Wu, M., Wang, Y., He, G. et al. Analysis of the mechanism and prognostic value of PRKCQ-AS1 in inhibiting the progression of lung adenocarcinoma via regulating the PD-1/PD-L1 pathway. Sci Rep 16, 9782 (2026). https://doi.org/10.1038/s41598-026-39024-2
Mots-clés: adénocarcinome pulmonaire, point de contrôle immunitaire, ARN long non codant, microenvironnement tumoral, PD-1 PD-L1