Clear Sky Science · fr
MUC14 supprime l’adénocarcinome pulmonaire via l’intégrine α8β6/PI3K/AKT/MAPK modulant la réponse au cisplatine et l’immunité
Pourquoi cette étude sur le cancer du poumon est importante
L’adénocarcinome pulmonaire est la forme de cancer du poumon la plus fréquente et est souvent traité par le chimiothérapeutique cisplatine. Malheureusement, de nombreuses tumeurs développent une résistance à ce médicament, et la survie à long terme reste faible. Cette étude met en lumière une protéine de surface cellulaire peu connue, MUC14, qui semble agir comme un frein naturel sur les tumeurs pulmonaires. Comprendre le fonctionnement de MUC14 pourrait ouvrir de nouvelles voies pour rendre la chimiothérapie plus efficace et aider le système immunitaire à mieux reconnaître et attaquer les cellules cancéreuses.
Une protéine protectrice en pleine vue
MUC14, aussi appelée endomucine, se situe à la surface des cellules et appartient à une famille de protéines glycosylées connues sous le nom de mucines. En exploitant de larges bases de données publiques sur le cancer et en examinant des échantillons de patients, les chercheurs ont constaté que les tumeurs d’adénocarcinome pulmonaire produisent généralement beaucoup moins de MUC14 que les tissus normaux adjacents. Les patients dont les tumeurs conservaient des niveaux plus élevés de MUC14 vivaient plus longtemps et présentaient une progression de la maladie plus lente que ceux ayant de faibles niveaux. Dans de nombreux types de cancers, MUC14 tendait à être supprimée, ce qui suggère qu’elle joue souvent un rôle d’inhibiteur tumoral plutôt que de promoteur. 
Ralentir les cellules cancéreuses et réduire les tumeurs
Pour déterminer ce que fait réellement MUC14, l’équipe a modulé son expression dans des lignées cellulaires de cancer du poumon. Lorsqu’ils ont forcé les cellules à produire davantage de MUC14, celles-ci se divisaient plus lentement, migraient moins et avaient une capacité d’invasion réduite à travers un gel mimant le tissu corporel. Elles adhéraient aussi plus difficilement aux molécules de matrice essentielles et formaient moins de colonies, et de plus petite taille. Chez la souris, des cellules cancéreuses programmées pour surexprimer MUC14 formaient des tumeurs sous-cutanées plus petites et provoquaient moins de métastases pulmonaires après injection intraveineuse. Lorsque MUC14 était au contraire inhibée par des petits ARN interférents, l’effet inverse était observé : les cellules croissaient plus vite, se déplaçaient davantage, adhéraient mieux et formaient plus de colonies, autant de signes d’un comportement tumoral plus agressif.
Couper les signaux de croissance à la surface cellulaire
Les auteurs ont ensuite cherché à comprendre comment MUC14 exerce ces effets puissants. Ils se sont intéressés aux intégrines, une famille de récepteurs qui ancrent les cellules à leur environnement et transmettent des signaux de croissance et de survie à l’intérieur de la cellule. Les données de centaines de tumeurs pulmonaires révélaient un lien fort entre MUC14 et deux sous-unités d’intégrine, appelées α8 et β6, qui s’associent à la surface cellulaire. En utilisant une technique optique capable de détecter des protéines séparées par des distances de l’ordre du milliardième de mètre, les chercheurs ont confirmé que MUC14 et le complexe intégrine α8β6 cohabitent côte à côte dans la membrane. Un excès de MUC14 perturbait le regroupement de ces intégrines et affaiblissait deux voies de croissance majeures qu’elles activent normalement : PI3K/AKT et MAPK/ERK. Lorsque MUC14 était réduite, ces voies devenaient plus actives, ce qui explique en partie pourquoi les cellules cancéreuses se multipliaient et se disséminaient plus facilement. 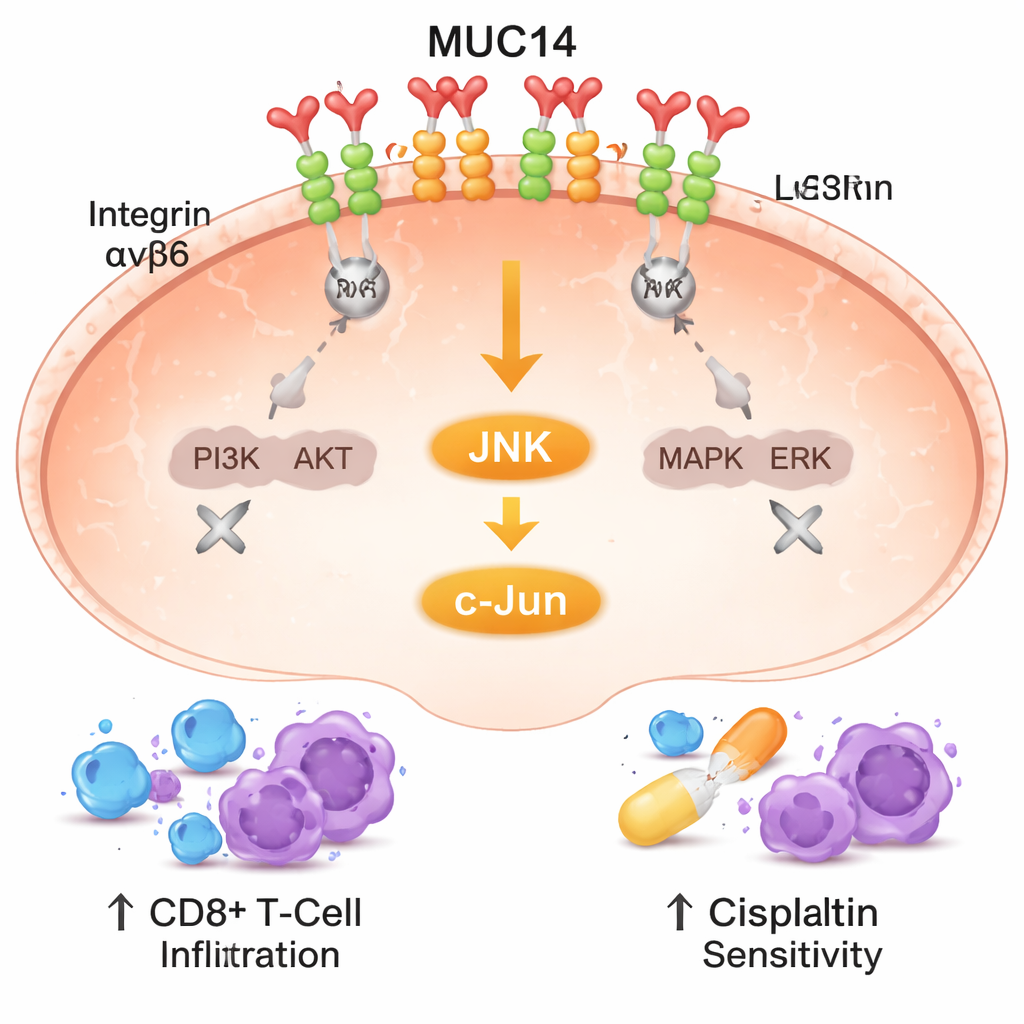
Favoriser la coopération entre le système immunitaire et la chimiothérapie
Le pronostic d’un cancer dépend non seulement des cellules tumorales elles-mêmes, mais aussi des cellules immunitaires environnantes. En analysant des bases de données de profilage immunitaire et en colorant des coupes de tumeurs humaines, l’équipe a observé que les tumeurs présentant des niveaux plus élevés de MUC14 contenaient davantage de lymphocytes T CD3+ et CD8+ — des cellules immunitaires capables de tuer directement les cellules tumorales — situés à proximité des régions tumorales positives pour MUC14. Cela suggère que MUC14 contribue à créer un environnement plus favorable à l’attaque immunitaire. Les chercheurs ont également étudié le cisplatine, un traitement de référence pour l’adénocarcinome pulmonaire. En culture cellulaire, les tumeurs surexprimant MUC14 nécessitaient des doses beaucoup plus faibles de cisplatine pour être inhibées, tandis que les cellules dépourvues de MUC14 devenaient plus résistantes au médicament. Il est important de noter que MUC14 ne rend pas simplement les cellules plus susceptibles de mourir de façon intrinsèque ; elle amplifie l’effet létal du cisplatine, en partie en activant une voie de stress connue sous le nom de JNK/c-Jun, déclenchée par les dommages à l’ADN.
Vers des combinaisons thérapeutiques plus intelligentes pour le traitement du poumon
En termes simples, ce travail présente MUC14 comme un système de défense intégré contre l’adénocarcinome pulmonaire. Lorsqu’elle est présente, elle bloque des commutateurs de croissance clés à la surface cellulaire, freine la dissémination tumorale, attire des lymphocytes T anti-tumoraux et renforce l’efficacité du cisplatine sans ajouter de toxicité d’organe dans les tests réalisés chez l’animal. Lorsqu’elle est perdue, les tumeurs deviennent plus résistantes, plus mobiles et moins réceptives aux traitements standards. Ces résultats suggèrent que la mesure de MUC14 pourrait aider à prédire le pronostic et la réponse au traitement, et que des thérapies futures visant à augmenter l’activité de MUC14 — ou à imiter ses effets sur la signalisation des intégrines — pourraient permettre de mieux combiner chimiothérapie et immunothérapie pour les patients atteints de cancer du poumon avancé.
Citation: Li, X., Li, M., Huang, S. et al. MUC14 suppresses lung adenocarcinoma via integrin α8β6/PI3K/AKT/MAPK modulating cisplatin response and immunity. Sci Rep 16, 7784 (2026). https://doi.org/10.1038/s41598-026-39019-z
Mots-clés: adénocarcinome pulmonaire, MUC14, résistance au cisplatine, signalisation des intégrines, immunité tumorale