Clear Sky Science · fr
La modélisation structurale révèle la base moléculaire de la nouvelle activité de CYP153A6 envers des dérivés du toluène
Confier des tâches chimiques difficiles à la nature
Les chimistes et l’industrie comptent sur des réactions qui introduisent de l’oxygène sur des liaisons carbone–hydrogène récalcitrantes, par exemple pour dépolluer ou pour synthétiser des ingrédients pour médicaments et parfums. Réaliser cela proprement, sans produits chimiques agressifs ni déchets métalliques lourds, est difficile. Cette étude examine un catalyseur naturel, une enzyme appelée CYP153A6 issue d’une bactérie du sol, et pose une question simple aux implications importantes : peut-on orienter cette enzyme pour qu’elle « améliore » sélectivement des molécules proches du toluène — composés courants des carburants et solvants — en produits plus utiles et plus respectueux de l’environnement ?
Une enzyme qui choisit un seul endroit
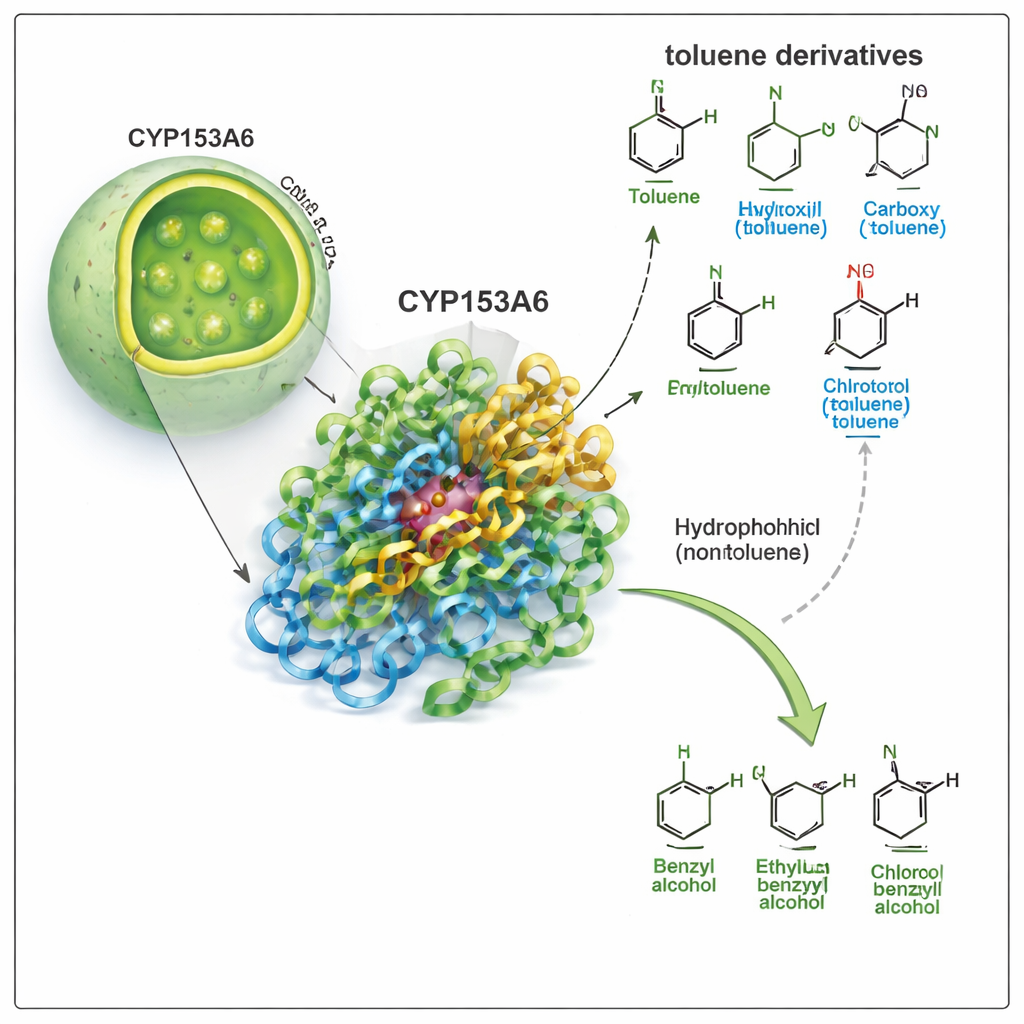
CYP153A6 appartient à la vaste famille des cytochromes P450, les spécialistes naturels de l’oxydation. À la différence de nombreux catalyseurs industriels, cette enzyme fonctionne en milieu aqueux, à température modérée, et cible des positions très spécifiques sur une molécule. Des travaux antérieurs avaient montré que CYP153A6 ajoute de l’oxygène sur les extrémités d’alcools gras et sur certains composés odorants d’origine végétale. Ici, les auteurs s’interrogent : peut‑elle aussi attaquer la position « benzylique » — la petite chaîne latérale attachée à un noyau benzénique — dans le toluène et des composés apparentés ? Cette transformation convertit les dérivés du toluène en alcools benzylés, des blocs de construction précieux pour la pharmacie, les arômes et les produits chimiques fins.
Tester quelles molécules l’enzyme préfère
L’équipe a d’abord réalisé des expériences de biotransformation en utilisant des cellules d’E. coli génétiquement modifiées pour produire CYP153A6, soit en cellules entières soit en extraits cellulaires. Elles ont exposé l’enzyme à un panel de dérivés du toluène, en variant le groupe fixé sur l’anneau aromatique (méthyle, chlore, méthoxy, hydroxy ou nitro) et sa position (para, méta ou ortho). L’enzyme a très bien fonctionné sur des composés apolaires ou faiblement polaires, comme le p‑cymène, le p‑xylène, le p‑méthylanisole et le p‑chlorotoluène, convertissant systématiquement le groupe méthyle benzylique en alcool benzylé. De manière frappante, elle a complètement ignoré des molécules plus fortement polaires comme le p‑crésol, le p‑méthylbenzylalcool et le p‑nitrotoluène, bien qu’elles soient structurellement similaires. Ce profil suggère que la poche de l’enzyme est fortement hydrophobe et défavorise les groupes polaires.
Construire une carte 3D de la machine moléculaire
Comme la structure tridimensionnelle de CYP153A6 n’avait pas été résolue expérimentalement, les chercheurs ont construit un modèle informatique de haute qualité en s’appuyant sur un P450 étroitement apparenté dont la structure est connue. Ils ont validé ce modèle en vérifiant sa géométrie et en exécutant de longues simulations de dynamique moléculaire pour s’assurer que la protéine restait stable dans le temps, ce qui fut le cas. Les simulations ont révélé un site actif enfoui relié à l’extérieur par des tunnels étroits par lesquels les substrats entrent et les produits sortent. Ces tunnels sont façonnés et régulés par des boucles flexibles en surface, ce qui aide à expliquer comment l’enzyme peut guider des molécules hydrophobes jusqu’au centre réactif contenant le groupe hème tout en permettant à l’eau et aux produits oxydés d’évacuer.
Observer la liaison, le mouvement et la réaction des molécules
Avec le modèle en main, les auteurs ont simulé la façon dont différents dérivés du toluène se lient à l’intérieur de CYP153A6. Ils ont utilisé une approche dite d’ensemble de docking, testant de nombreuses conformations proteinques légèrement différentes et plusieurs états électroniques du fer de l’hème, pour identifier quelles configurations distinguaient le mieux les substrats réels des non‑substrats. Le scénario gagnant utilisait le fer à l’état ferrique de repos et sans molécules d’eau supplémentaires dans la poche, et favorisait correctement les substrats connus. Des simulations de suivi ont suivi, image par image, la position de chaque molécule par rapport à l’hème. Les bons substrats comme le p‑cymène et le p‑xylène restaient proches du fer avec leur groupe méthyle benzylique orienté vers lui, et leurs énergies de liaison prédites étaient fortement favorables. Les mauvais substrats avaient tendance à dériver, à adopter des orientations gênantes ou à interagir défavorablement avec les chaînes latérales majoritairement lipophiles qui tapissent la poche.
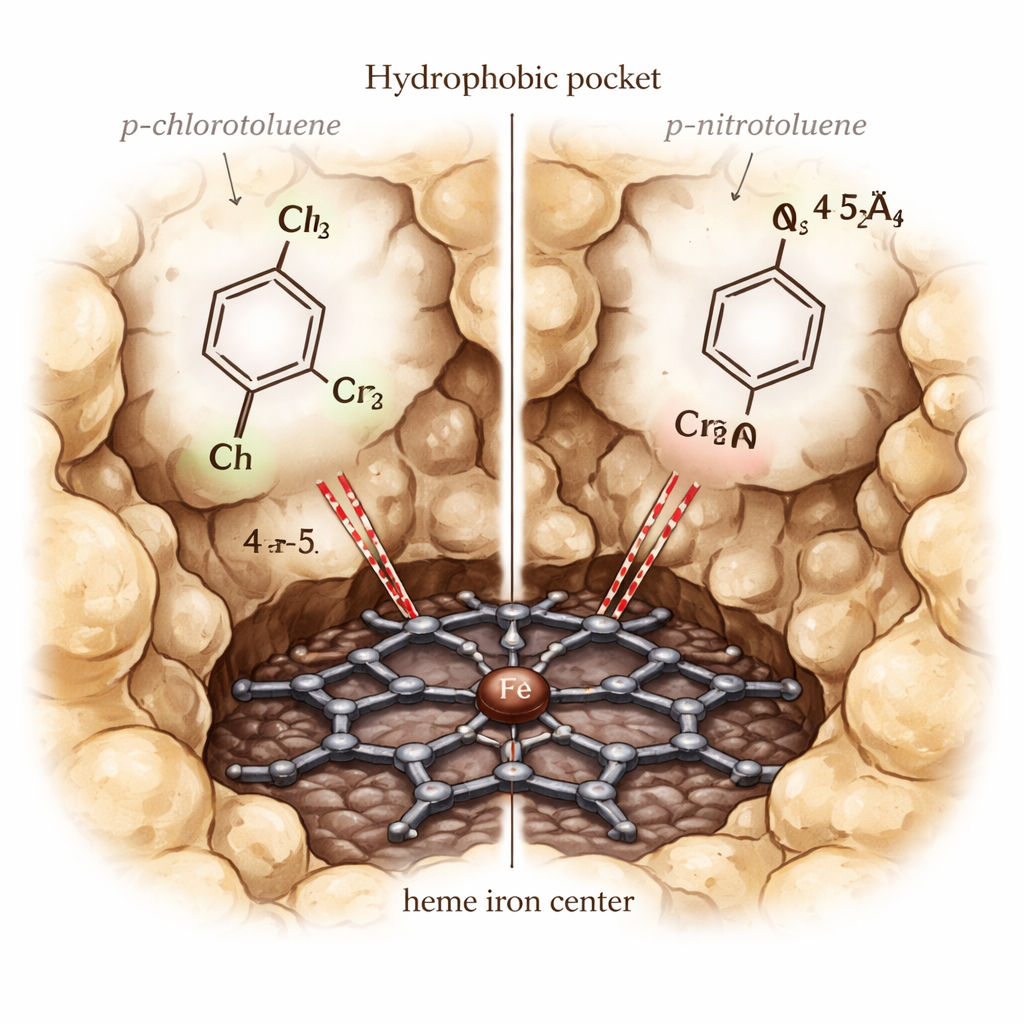
Pourquoi un sosie réagit et un autre non
Un puzzle a retenu l’attention : le p‑chlorotoluène est efficacement oxydé par CYP153A6, alors que le p‑nitrotoluène ne l’est pas, bien que les deux s’insèrent dans la poche et lient avec une force similaire dans les simulations. Pour résoudre cela, les auteurs ont réalisé des calculs plus détaillés en mécanique quantique/mécanique moléculaire (QM/MM) sur l’état hautement réactif « Compound I » de l’enzyme. Ces calculs ont montré que le groupe nitro attire tellement la densité électronique loin du carbone benzylique qu’il devient très difficile à oxyder, malgré une proximité géométrique suffisante. En revanche, le groupe chlore permet une meilleure communication électronique entre l’hème et le substrat, ce qui se traduit par une plus grande densité de spin sur l’anneau aromatique et le groupe méthyle et un alignement plus réactif pour l’étape critique d’abstraction d’hydrogène.
Ce que cela signifie pour une chimie plus propre
En termes simples, CYP153A6 se comporte comme un petit gant huileux qui maintient certaines molécules de type carburant de manière à ce que l’oxygène soit ajouté en un point précis — les transformant en produits plus solubles dans l’eau, plus utiles et finalement plus facilement dégradables. L’étude montre que l’enzyme préfère des substituants non polaires et que la forme et le flux électronique déterminent si un dérivé du toluène sera transformé. En clarifiant comment CYP153A6 reconnaît et active ces molécules, ce travail fournit une feuille de route pour concevoir des versions améliorées qui pourraient aider à dépolluer des aromatiques ou à fabriquer des produits chimiques complexes de façon plus durable.
Citation: Wei, Y., Donzella, S., Foiadelli, S. et al. Structure-based modeling reveals molecular basis for CYP153A6’s novel activity toward toluene derivatives. Sci Rep 16, 7570 (2026). https://doi.org/10.1038/s41598-026-38986-7
Mots-clés: biocatalyse, cytochrome P450, hydroxylation du toluène, ingénierie enzymatique, chimie verte