Clear Sky Science · fr
Bio-usine transplastomique pour la production d’α‑lactalbumine humaine fonctionnelle à des fins nutritionnelles et thérapeutiques
Transformer les plantes en usines à protéines du lait
Les régimes modernes dépendent fortement des protéines du lait, mais l’élevage bovin à grande échelle comporte des coûts environnementaux et des enjeux éthiques. Cette étude explore une manière radicalement différente de produire une protéine clé du lait humain — en apprenant aux feuilles de plantes à la synthétiser. Les travaux montrent que le tabac peut être reprogrammé pour fabriquer l’α‑lactalbumine humaine, une protéine importante pour la nutrition infantile et dotée de potentielles propriétés anticancéreuses, ouvrant la voie à des ingrédients pour formules infantiles sans animaux et à de nouveaux composants alimentaires anti‑cancer.
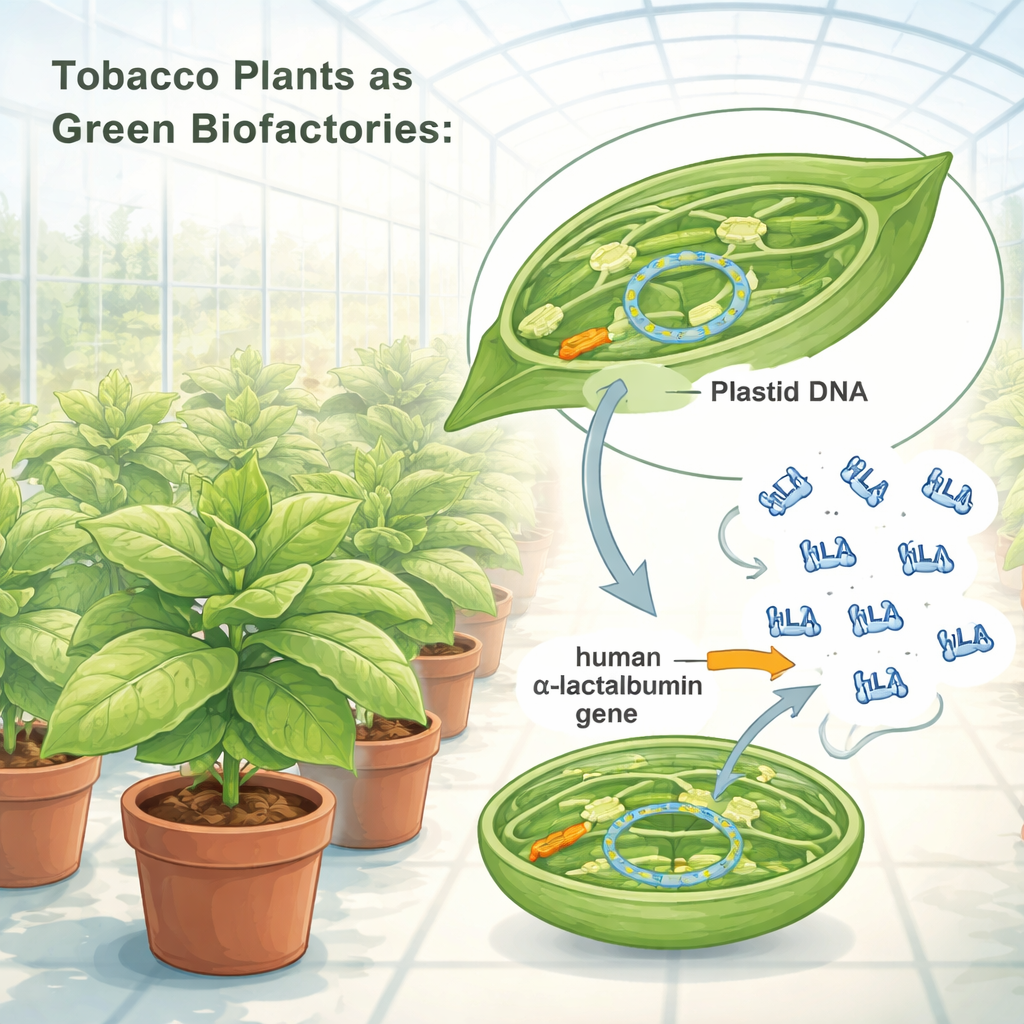
Pourquoi cette protéine du lait est importante
Le lait maternel est plus que de la nourriture ; c’est un cocktail finement réglé de protéines, de lipides et de sucres qui évolue avec les besoins du nourrisson. L’une de ses protéines les plus importantes est l’α‑lactalbumine, qui contribue à la synthèse du lactose, le sucre principal du lait et une source d’énergie critique pour les bébés. L’α‑lactalbumine est riche en acides aminés essentiels, dont le tryptophane, précurseur de la sérotonine, le neurotransmetteur associé au bien‑être, et a été liée à une meilleure résistance au stress et à une protection potentielle contre certains cancers. Facile à digérer, au goût neutre et stable sur une large plage d’acidité, elle est largement utilisée dans les préparations pour nourrissons et les boissons nutritionnelles — et la demande augmente.
Le problème du lait traditionnel
Dépendre des vaches pour fournir les protéines du lait présente des inconvénients. Le bétail génère une part importante des émissions mondiales de gaz à effet de serre, et les grandes exploitations laitières nécessitent d’immenses surfaces, quantités d’eau et d’aliments. De plus, la gestion des fermes peut soulever des inquiétudes liées aux hormones, aux antibiotiques et aux agents pathogènes qui peuvent se retrouver dans le lait. Ces pressions ont stimulé l’intérêt pour l’agriculture cellulaire, où des microbes ou des cellules en culture produisent les protéines du lait à la place des animaux. Pourtant, beaucoup de ces systèmes restent coûteux, difficiles à industrialiser ou produisent des protéines qui ne sont pas parfaitement identiques aux versions humaines. Les plantes, et en particulier leurs chloroplastes — ces petites usines vertes responsables de la photosynthèse — offrent une plateforme alternative prometteuse.
Reprogrammer les chloroplastes en bio-usines
Les chercheurs ont réécrit les instructions génétiques de l’α‑lactalbumine humaine pour que les chloroplastes du tabac puissent les lire efficacement. Ils ont inséré ce gène optimisé dans l’ADN chloroplastique à l’aide d’une « cassette génique » composée d’éléments régulateurs végétaux puissants faisant office d’interrupteurs. Par bombardement de particules, ils ont délivré cette cassette dans les cellules foliaires du tabac, puis sélectionné des plantules dont les chloroplastes avaient entièrement intégré le nouveau gène. Des tests génétiques ont confirmé que toutes les copies de l’ADN chloroplastique de ces plantes portaient désormais le plan de la protéine humaine. Les plantes modifiées ont poussé normalement en serre, produisant des graines et ne présentant pas de pénalités visibles de taille, de forme ou de fertilité, ce qui suggère que la charge protéique supplémentaire n’a pas nui à la santé des plantes.
Prouver que la protéine d’origine végétale fonctionne
Ensuite, l’équipe a vérifié si l’α‑lactalbumine produite par la plante se comportait comme la protéine humaine authentique. Ils ont extrait les protéines solubles des feuilles, purifié l’α‑lactalbumine et étudié sa structure par une technique informant sur le repliement des protéines. L’« empreinte » spectrale de la protéine d’origine végétale s’est presque superposée à celle de l’α‑lactalbumine humaine commerciale, indiquant un repliement similaire. Sur le plan fonctionnel, la protéine végétale a activé l’enzyme synthétisant le lactose presque aussi bien que la version native, entraînant une formation de lactose à environ 93 % du taux de la protéine standard. Fait remarquable, l’α‑lactalbumine s’est accumulée jusqu’à représenter environ 23 % de toutes les protéines solubles des feuilles — parmi les niveaux les plus élevés rapportés pour des protéines humaines produites dans des chloroplastes de plantes — suggérant que ce système peut fournir des rendements d’intérêt industriel.
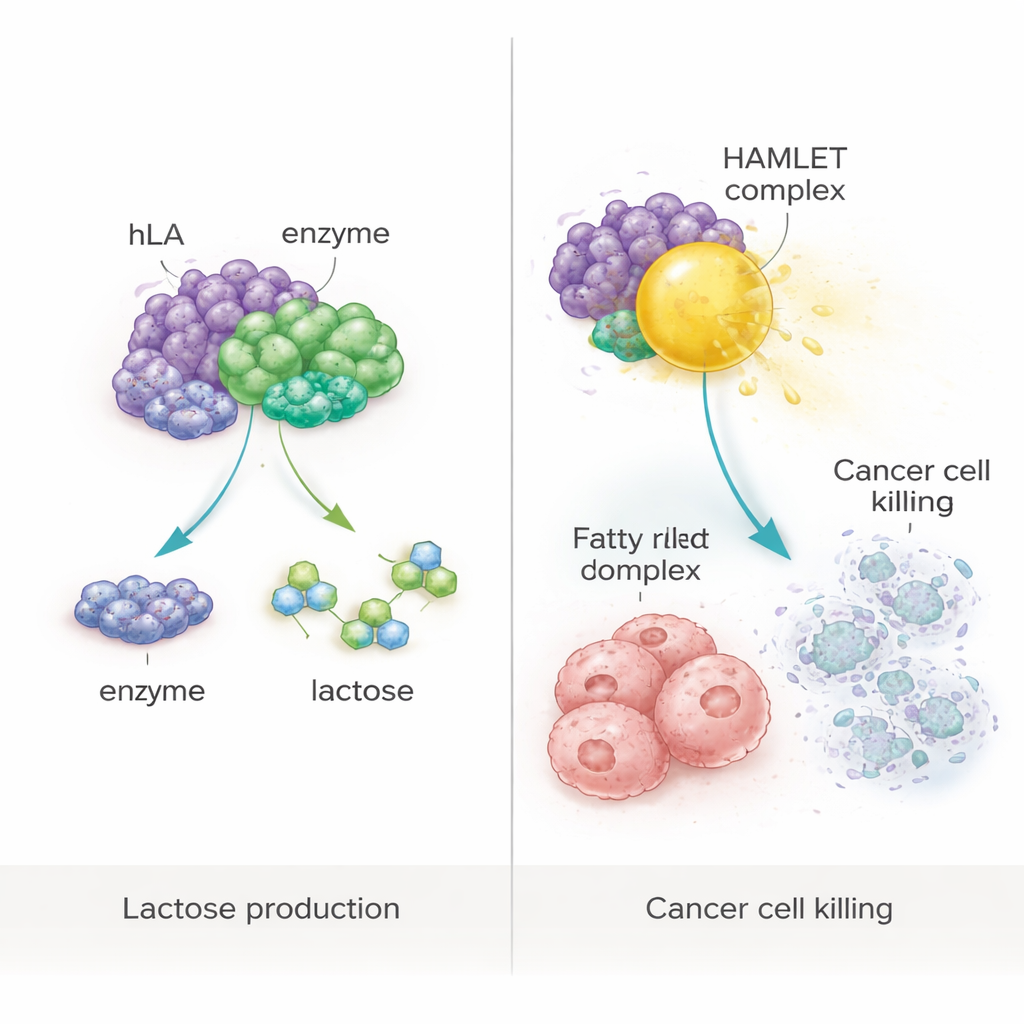
De la nutrition à des complexes anti‑cancer
L’étude a aussi testé une idée plus ambitieuse : utiliser la protéine végétale comme bloc de construction d’un complexe anticancéreux connu sous le nom de HAMLET, formé quand l’α‑lactalbumine se lie fortement à l’acide oléique, un acide gras courant. En chauffant doucement la protéine purifiée avec de l’acide oléique dans des conditions contrôlées, les chercheurs ont généré un complexe de type HAMLET. Lorsqu’appliqué à des cellules cancéreuses humaines colorectal (WiDr) et mammaire (MCF‑7) en culture, ce complexe a réduit de manière spectaculaire la survie cellulaire à moins de 10 %. Des analyses complémentaires ont montré que la plupart des cellules affectées présentaient des signes d’apoptose, une forme de mort cellulaire programmée plutôt qu’une rupture incontrôlée. De manière importante, ni la protéine seule, ni l’acide gras seul, ni des extraits de plantes non modifiées n’ont provoqué de mortalité cellulaire significative, confirmant que l’effet anticancéreux dépendait du complexe spécifique.
Ce que cela pourrait signifier pour les aliments et médicaments du futur
Dans l’ensemble, ces travaux montrent que les chloroplastes végétaux peuvent produire de manière fiable de grandes quantités d’une protéine du lait humain à la fois nutritionnellement pertinente et dotée d’une activité thérapeutique. Pour un public non spécialiste, cela signifie que des préparations pour nourrissons, des aliments fonctionnels ou des compléments pourraient un jour être fabriqués à partir de protéines cultivées dans des feuilles plutôt que prélevées sur des vaches, réduisant l’impact environnemental tout en s’alignant davantage sur la biologie humaine. Parallèlement, cette même protéine d’origine végétale peut être convertie en laboratoire en un complexe anticancéreux ciblé, laissant entrevoir des filières végétales pour des biothérapies abordables. Bien que des recherches supplémentaires soient nécessaires pour confirmer la sécurité et l’efficacité chez l’animal et chez l’humain — et pour transférer cette technologie vers des cultures comestibles — l’étude offre un aperçu convaincant des plantes agissant comme mini‑usines pour la nutrition et la médecine de nouvelle génération.
Citation: Ehsasatvatan, M., Kohnehrouz, B.B. Transplastomic biofactory for the production of functional human α-lactalbumin for nutritional and therapeutic applications. Sci Rep 16, 7359 (2026). https://doi.org/10.1038/s41598-026-38965-y
Mots-clés: protéines lactées produites par les plantes, bio-usine chloroplastique, alpha-lactalbumine humaine, alternatives laitières durables, thérapie anticancéreuse HAMLET