Clear Sky Science · fr
L’intégrine αv contribue à la régulation de la raideur des cellules musculaires lisses vasculaires
Pourquoi la « souplesse » des artères compte
En vieillissant ou en développant une hypertension, nos grosses artères perdent progressivement leur élasticité naturelle et deviennent plus rigides. Cette modification oblige le cœur à fournir un effort accru et augmente le risque d’infarctus, d’accidents vasculaires cérébraux et d’autres problèmes cardiovasculaires. Les scientifiques savent depuis longtemps que la composition des parois artérielles — des protéines comme l’élastine et le collagène — influence la raideur. Cette étude pose une question plus subtile : est‑ce que les cellules musculaires à l’intérieur des parois artérielles peuvent elles‑mêmes devenir plus rigides, et une petite famille de récepteurs de surface appelée intégrine αv aide‑t‑elle à maintenir ces cellules, et donc nos artères, plus flexibles ?
Les cellules musculaires qui façonnent le flux sanguin
Les grosses artères ne sont pas de simples tuyaux passifs. Leur couche moyenne est riche en cellules musculaires lisses vasculaires, capables de se contracter et de se relâcher pour ajuster finement le flux et la pression sanguins. Ces cellules sont ancrées à une armature environnante appelée matrice extracellulaire. Les auteurs se sont concentrés sur un groupe de molécules d’ancrage, l’intégrine αv, qui traverse la membrane cellulaire et relie physiquement le squelette interne de la cellule à cette armature externe. Des travaux antérieurs suggéraient que l’intégrine αv participait à la cicatrisation et au remodelage des vaisseaux, mais il restait incertain qu’elle contrôle aussi la raideur intrinsèque des cellules musculaires, notamment sous la contrainte d’hormones comme l’angiotensine II qui augmentent la pression artérielle et favorisent la fibrose.
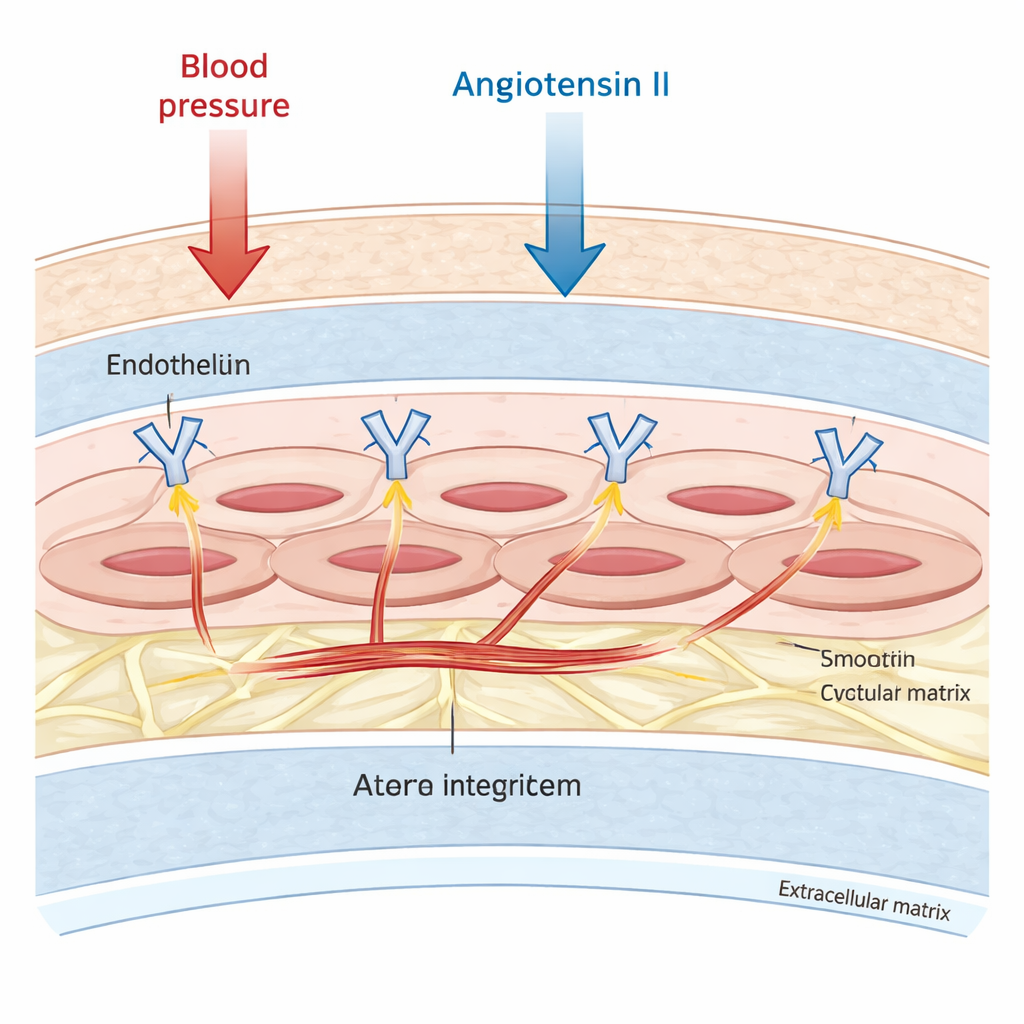
Mesurer la raideur cellule par cellule
Pour aborder la question, l’équipe a utilisé des cellules musculaires lisses de souris cultivées en laboratoire et des souris génétiquement modifiées pour être dépourvues d’intégrine αv spécifiquement dans leurs cellules musculaires vasculaires. Ils ont sondé la raideur des cellules avec la microscopie à force atomique, une technique où une pointe ultra‑fine enfonce doucement la surface cellulaire et enregistre la force nécessaire. Les cellules dépourvues d’intégrine αv étaient plus de deux fois plus rigides que les cellules témoin dans des conditions calmes. Exposées à l’angiotensine II pendant deux jours, ces cellules déficientes devenaient encore environ trois fois plus rigides, alors que les cellules normales changeaient à peine. Comme leurs mesures utilisaient des indentations très superficielles, les auteurs ont construit un modèle informatique détaillé d’une cellule musculaire lisse et ont simulé des enfoncements plus profonds. Les simulations ont montré que les tests peu profonds mettent l’accent sur la contribution de l’enveloppe externe et de la région corticale de la cellule, et restaient dans la plage observée chez les cellules mutantes rigides, ce qui soutient les résultats biologiques.
Un squelette interne remodelé
L’étape suivante a consisté à examiner l’intérieur des cellules. À l’aide de colorants fluorescents et de la microscopie, les chercheurs ont analysé l’actine, un filament clé qui forme l’armature interne de la cellule. Les cellules musculaires témoins présentaient un réseau d’actine relativement diffus, même après traitement à l’angiotensine II. En revanche, les cellules dépourvues d’intégrine αv formaient d’épaisses fibres de tension traversant la cellule et, après exposition à l’hormone, une bande intense d’actine juste sous la membrane cellulaire, appelée actine corticale. Une mesure quantitative de l’accumulation d’actine près du bord cellulaire confirma que cette couche corticale était fortement enrichie uniquement dans les cellules déficientes en intégrine. Ces cellules développaient aussi des structures d’adhésion anormalement longues là où elles s’accrochent à la matrice environnante, ce qui est compatible avec une transition vers des adhésions fibrillaires plus porteuses de tension qui peuvent verrouiller la cellule dans un état rigide.
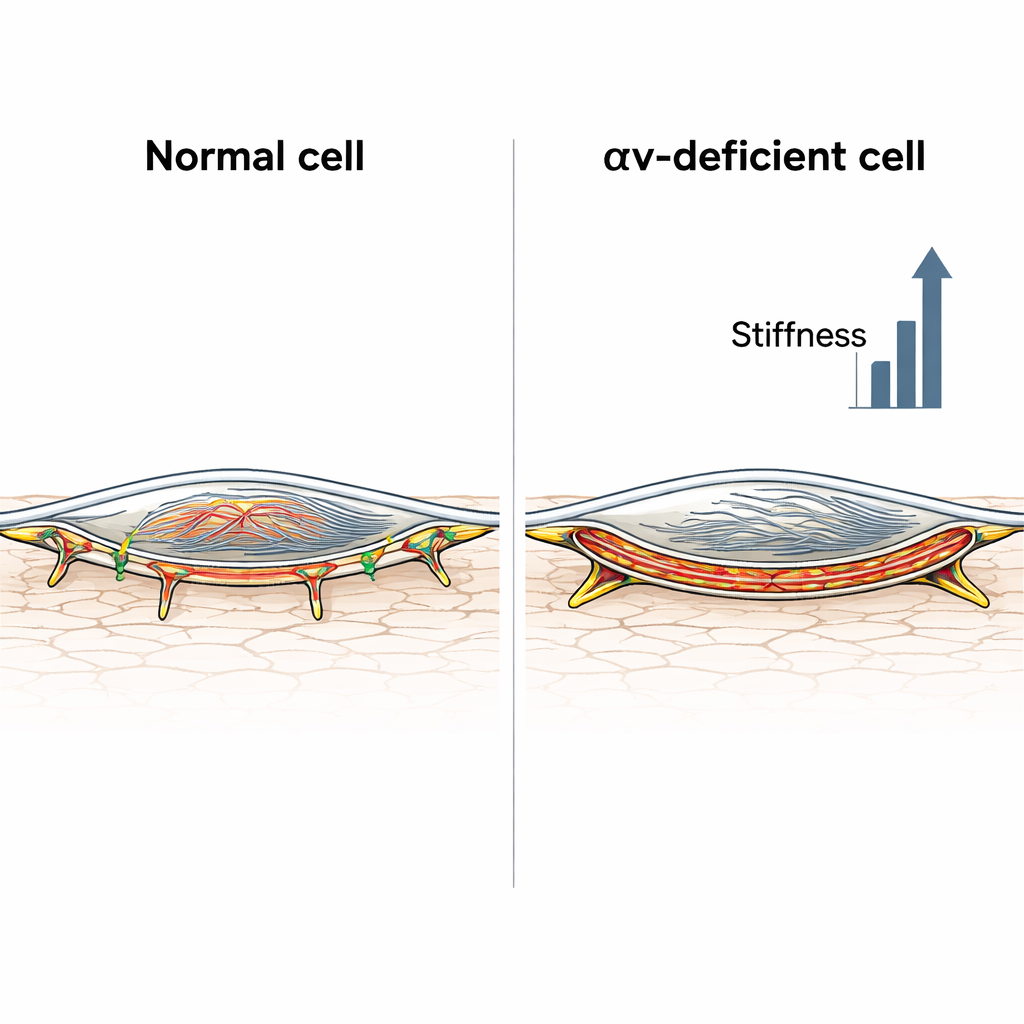
Quand la paroi a le même aspect mais se comporte différemment
Parce que les artères ne sont pas seulement constituées de leurs cellules musculaires, les scientifiques ont aussi mesuré les propriétés mécaniques des artères carotides chez des souris vivantes, avec ou sans intégrine αv dans leurs cellules musculaires vasculaires, et avec ou sans perfusion chronique d’angiotensine II. De façon surprenante, la pression artérielle globale et la raideur de la paroi — évaluées à partir de courbes pression‑diamètre obtenues par échographie — étaient similaires chez les deux souches de souris, au repos comme après traitement hormonal. Pourtant, la composition microscopique de la paroi différait. Sous angiotensine II, les souris témoins montraient moins d’élastine et plus de collagène, signes classiques d’une matrice plus rigide, tandis que les souris déficientes en intégrine présentaient relativement moins de modification du collagène mais des cellules musculaires beaucoup plus rigides. Autrement dit, chez les souris normales, c’est la matrice qui effectuait l’essentiel du raidissement ; chez les souris sans intégrine, ce sont les cellules musculaires elles‑mêmes qui devenaient si rigides qu’elles compensaient pratiquement les altérations matricielles plus modestes.
Ce que cela signifie pour les artères vieillissantes
Pour le grand public, le message clé est que la raideur artérielle ne se résume pas aux fibres élastiques usées ; elle dépend aussi de la façon dont les cellules musculaires de la paroi organisent leurs petits câbles internes. L’intégrine αv aide normalement à empêcher ces cellules de devenir trop rigides lorsqu’elles sont sollicitées par des hormones comme l’angiotensine II. Lorsque ce contrôle est perdu, les cellules réarrangent leur squelette d’actine — en particulier la zone corticale juste sous la membrane — et se verrouillent dans un état plus rigide qui peut entraîner le raidissement artériel même en l’absence de modifications spectaculaires de la matrice environnante. Cette découverte ouvre des pistes thérapeutiques : des médicaments qui détendent légèrement ou réorganisent le réseau d’actine cortical, ou qui moduleraient la signalisation liée aux intégrines, pourraient un jour compléter les traitements hypotenseurs pour restaurer plus directement le « ressort » des artères vieillissantes.
Citation: Bascetin, R., Belozertseva, E., Regnault, V. et al. Integrin αv contributes to the regulation of vascular smooth muscle cell stiffness. Sci Rep 16, 7682 (2026). https://doi.org/10.1038/s41598-026-38948-z
Mots-clés: raideur artérielle, cellules musculaires lisses vasculaires, intégrine alpha v, cytosquelette d’actine, angiotensine II