Clear Sky Science · fr
Conception, synthèse et évaluation antitumorale de nouveaux spiroindenopyridotriazinepyranes fonctionnalisés
Pourquoi de nouveaux médicaments contre le cancer sont importants
Les traitements du cancer ont sauvé de nombreuses vies, mais ils présentent souvent deux problèmes majeurs : les tumeurs peuvent cesser de répondre aux médicaments et les tissus sains peuvent être endommagés en même temps que les cellules cancéreuses. Cette étude explore une nouvelle famille de petites molécules à géométrie soignée conçues pour frapper fort les cellules cancéreuses tout en épargnant davantage les cellules normales. En construisant ces composés de manière intelligente et efficace et en les testant sur des cellules de cancers du sein et du pancréas agressifs, les chercheurs recherchent des signes précoces de médicaments futurs plus sûrs et plus sélectifs.
Façonner de meilleurs profils moléculaires
Le cœur de ce travail est une forme chimique tridimensionnelle particulière appelée échafaudage spiro. On peut l’imaginer comme deux systèmes cycliques reliés en un seul point de pivot, ce qui rend la molécule rigide, compacte et plus « objet » qu’une chaîne souple. De nombreux médicaments modernes utilisent ce type d’architecture car elle les aide à s’insérer précisément dans les poches complexes des protéines au sein de nos cellules. Dans ce projet, l’équipe a conçu de nouveaux spiros qui combinent plusieurs types d’anneaux déjà connus pour leur potentiel anticancéreux, le tout fusionné en une structure étroitement organisée.
Une recette simple pour des molécules complexes
Sur le plan chimique, ces composés spiro seraient normalement difficiles et longs à synthétiser. Les chercheurs ont opté pour une stratégie en une seule étape et à composants multiples : trois blocs de construction simples sont mélangés et, dans les bonnes conditions, ils s’assemblent d’eux‑mêmes pour former la structure cible complexe. Après avoir testé divers solvants et températures, les meilleures conditions se sont révélées être l’éthanol ordinaire chauffé modérément, sans catalyseur ajouté. Cette approche a permis d’obtenir une petite bibliothèque de molécules apparentées en rendements élevés, qu’ils ont ensuite analysées en détail par des techniques standard pour confirmer la formation des structures prévues.
Mettre les nouveaux composés à l’épreuve
Une fois la chimie établie, l’attention s’est tournée vers la biologie. L’équipe a exposé deux lignées cellulaires cancéreuses difficiles à traiter — pancréatique (Panc1) et triple négatif du sein (MDA‑MB‑231) — aux nouvelles molécules, en parallèle avec des cellules normales dérivées de la peau comme contrôle de sécurité. À l’aide d’un test colorimétrique mesurant le nombre de cellules vivantes après traitement, ils ont constaté que trois composés, étiquetés 9d, 9e et surtout 9f, se distinguaient par des effets inhibiteurs de croissance bien plus marqués que les autres. De manière remarquable, tous ces composés ont eu peu d’impact sur les cellules normales aux mêmes concentrations, suggérant un degré de sélectivité souvent absent des chimiothérapies actuelles.
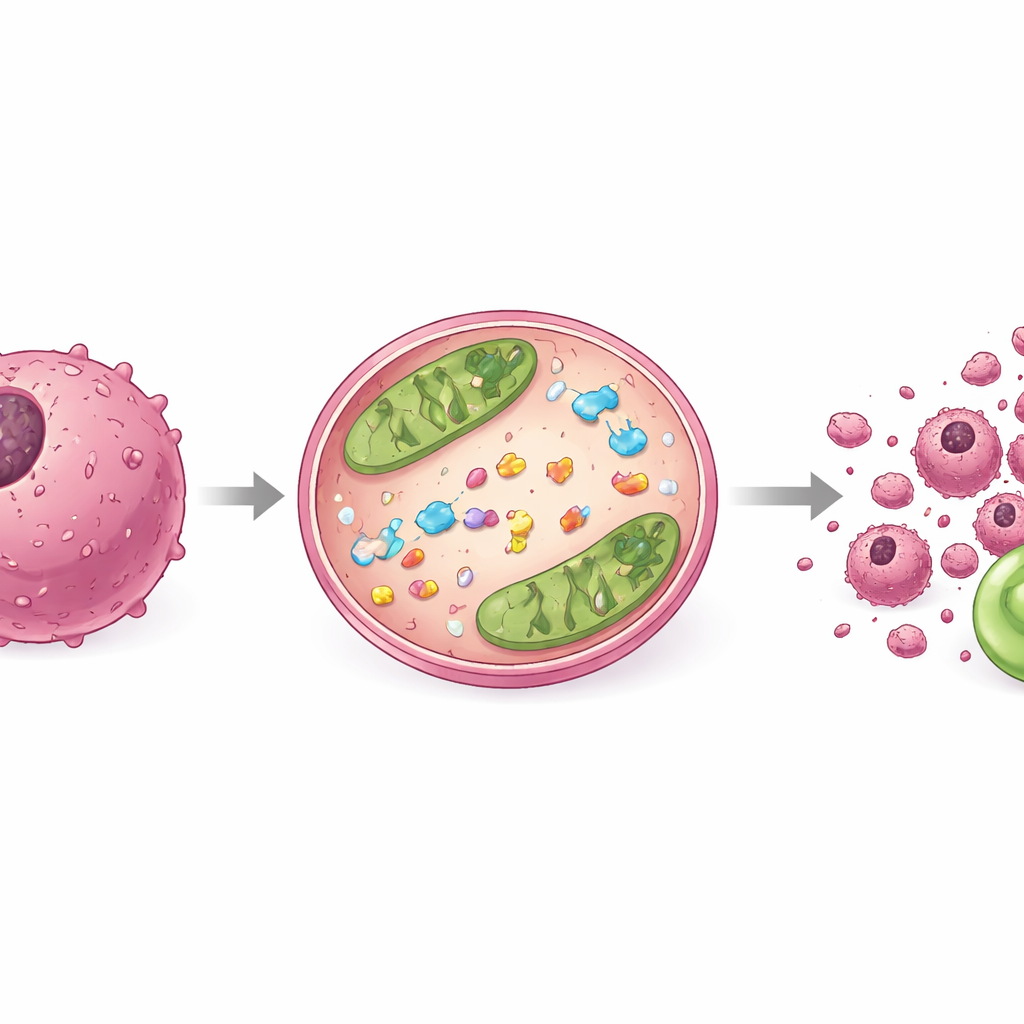
Comment les cellules réagissent et pourquoi la structure compte
Pour observer ce qui se passait à l’intérieur des cellules cancéreuses, les chercheurs ont coloré leur ADN et les ont examinées au microscope à fluorescence. Les cellules traitées par le composé le plus puissant, 9f, présentaient des noyaux rétrécis et fragmentés — des signes classiques de mort cellulaire programmée plutôt que d’un simple empoisonnement. Des expériences complémentaires ont analysé deux protéines gardiennes clés qui contrôlent cet interrupteur de mort cellulaire : l’une qui empêche la mort et l’autre qui la favorise. Le traitement par 9f a déplacé cet équilibre vers l’autodestruction dans les cellules cancéreuses, cohérent avec une induction ciblée de l’apoptose. En comparant les différents membres de la famille de composés, l’équipe a également constaté que de petites modifications autour du cœur spiro avaient de grands effets sur la puissance, soulignant comment à la fois la polarité électronique et le positionnement tridimensionnel des substituants peuvent moduler l’activité anticancéreuse.
Ce que cela pourrait signifier pour les traitements futurs
En termes simples, l’étude fournit une voie pratique pour fabriquer une nouvelle classe de molécules rigides et tridimensionnelles capables de ralentir fortement la croissance de certaines cellules cancéreuses tout en épargnant les cellules normales dans des tests en laboratoire. Un candidat, 9f, s’est montré aussi efficace qu’un médicament de chimiothérapie standard contre les lignées testées et semblait les tuer en activant leur programme d’autodestruction intrinsèque. Ces résultats sont préliminaires et limités aux cellules en culture : des études animales, le comportement pharmacocinétique et la sécurité à long terme restent inconnus. Néanmoins, ce travail montre comment une conception moléculaire intelligente et des méthodes de synthèse efficaces peuvent converger pour générer des pistes prometteuses en vue de futurs médicaments anticancéreux.
Citation: Safari, F., Bayat, M., Hosseini, H. et al. Design, synthesis, and antitumor evaluation of new functionalized spiroindenopyridotriazinepyrans. Sci Rep 16, 7917 (2026). https://doi.org/10.1038/s41598-026-38946-1
Mots-clés: thérapie du cancer, conception de médicaments, molécules spirocycliques, apoptose, synthèse multicomposants