Clear Sky Science · fr
Les A2-pancortines interagissent avec Bcl-xL et WAVE1 pour promouvoir les sites de contact mitochondrie-RER (MERCs) et exacerber l’élévation du calcium mitochondrial afin de médiatiser la mort cellulaire lors d’un AVC
Pourquoi de minuscules liaisons cérébrales comptent dans l’AVC néonatal
L’AVC est souvent perçu comme une maladie de l’adulte, mais lorsqu’il survient chez le nouveau‑né, il peut endommager en silence le cerveau en développement et provoquer des troubles à vie. Cette étude explore ce qui se passe au cœur des neurones lors d’une telle crise. Les auteurs ciblent une famille peu connue de protéines, les pancortines, et montrent comment deux isoformes propres au développement agissent comme des « amplificateurs » dangereux, resserrant les connexions entre des structures cellulaires clés et déclenchant un afflux de calcium qui peut pousser les jeunes neurones vers la mort.
Des coupables discrets dans le cerveau néonatal
Les pancortines sont des protéines de type échafaudage qui contribuent à façonner le cerveau en croissance. Deux formes, appelées A2‑pancortines, sont abondantes pendant le développement précoce puis s’atténuent largement à mesure que le cerveau mûrit. Parce que le cerveau du nouveau‑né est particulièrement vulnérable au manque d’oxygène, les chercheurs ont examiné si ces protéines propres à l’enfance pouvaient aggraver les lésions lorsque l’apport sanguin au cortex est brièvement interrompu, comme dans l’AVC néonatal. Dans des neurones corticaux de souris en culture, ils ont utilisé des outils génétiques pour diminuer l’ensemble des pancortines, puis ont exposé les cellules à une privation d’oxygène et de glucose mimant l’AVC. Les neurones avec niveaux réduits de pancortines survivaient beaucoup mieux, suggérant que ces protéines, au lieu de protéger les jeunes cellules, contribuent à leur blessure sous stress.
Des modèles murins d’AVC à un tissu cérébral préservé
Pour savoir si ce rôle nocif se manifestait aussi in vivo, l’équipe a conçu des souris déficientes spécifiquement pour les formes A2‑pancortines du développement. De jeunes souriceaux de deux semaines et leurs congénères normaux ont été soumis à l’occlusion d’une artère cérébrale majeure, modèle standard d’ischémie. Au bout d’un jour, les deux groupes présentaient des lésions dans des régions profondes du cerveau, mais le cortex des animaux dépourvus d’A2‑pancortines montrait environ deux fois moins de dommages que celui des animaux normaux. Fait marquant, cet effet protecteur disparaissait chez les souris de cinq semaines, âge où les variantes adultes de pancortines prédominent. Ces résultats dépendant de l’âge pointent les A2‑pancortines comme des facteurs pro‑mort clés dans le cortex néonatal, reliant un programme développemental à la vulnérabilité à l’AVC.
Zones de contact dangereuses à l’intérieur des neurones
À l’intérieur des cellules, les mitochondries productrices d’énergie se trouvent à proximité du réticulum endoplasmique (RE), un réseau membranaire replié qui stocke le calcium. Là où les deux membranes se rapprochent, les sites de contact mitochondrie–RE forment des tunnels microscopiques par lesquels le calcium peut transiter. Un transfert modéré soutient la production d’énergie, mais un excès peut saturer les mitochondries et déclencher la mort cellulaire. Les chercheurs ont découvert que les A2‑pancortines, avec deux partenaires — Bcl‑xL et WAVE1 — s’assemblent en un complexe tripartite localisé à ces sites de contact. Lorsqu’ils forçaient l’expression d’A2‑pancortines avec ces partenaires, mitochondries et RE se rapprochaient plus fréquemment et plus étroitement, comme l’indiquait un capteur fluorescent scindé spécialisé. Une protéine d’ancrage appelée GRP75 rejoignait ce complexe, contribuant à stabiliser les zones de contact.
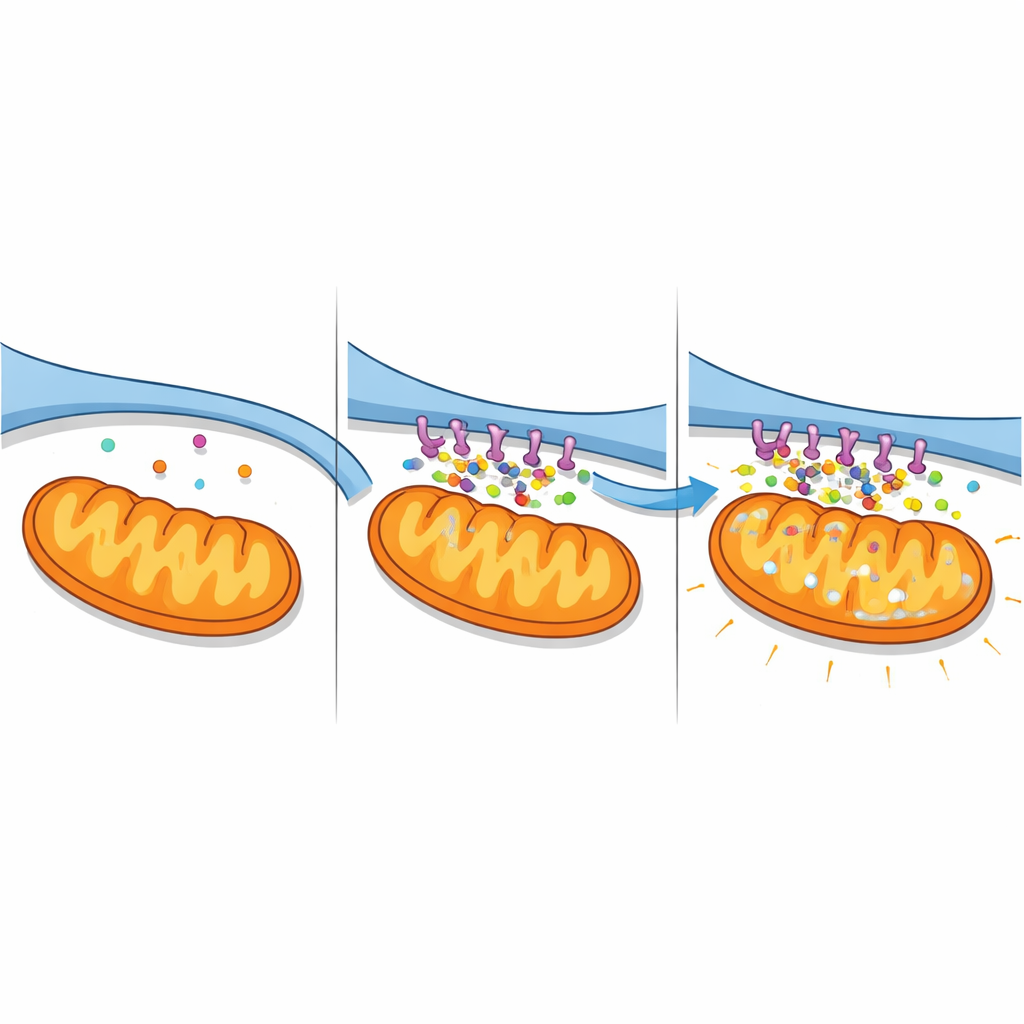
Déferlements calciques et centrales énergétiques en panne
Le renforcement des contacts avait de lourdes conséquences pour l’équilibre calcique. À l’aide d’indicateurs fluorescents rapportant séparément le calcium dans le cytosol, le RE et les mitochondries, les auteurs ont suivi l’évolution des niveaux au fil du temps. Les cellules exprimant le complexe A2‑pancortine présentaient une augmentation soutenue du calcium dans les mitochondries et dans le fluide environnant, accompagnée d’une chute des réserves du RE, signature d’un transfert massif du RE vers les mitochondries. Le blocage d’un canal clé de libération du calcium à la surface du RE (IP3R) a en grande partie prévenu ces changements, confirmant que le complexe amplifie une voie spécifique RE→mitochondrie. Dans des cellules de type nerveux exposées à une privation d’oxygène et de glucose simulant l’AVC, l’inhibition des pancortines produisait l’effet inverse : la surcharge calcique était atténuée et les réserves du RE mieux préservées. Ensemble, ces observations révèlent les A2‑pancortines comme des organisateurs d’une « autoroute » calcique qui devient mortelle sous stress ischémique.
Ce que cela implique pour la protection du cerveau néonatal
Pour un public non spécialiste, la leçon est que ce travail identifie un nouveau commutateur moléculaire qui contribue à décider si les jeunes neurones survivent ou non après un AVC. En resserrant les jonctions microscopiques entre les membranes stockant le calcium et les centrales énergétiques cellulaires, les A2‑pancortines provoquent une intoxication calcique des mitochondries et leur défaillance. Éliminer ces protéines chez de jeunes souris atténue l’impact de l’AVC expérimental, suggérant que des médicaments ou des thérapies géniques visant à perturber les complexes A2‑pancortine — ou à desserrer les sites de contact qu’ils renforcent — pourraient un jour réduire les lésions cérébrales chez les nouveau‑nés touchés. Bien que de tels traitements restent prospectifs, l’étude trace une voie claire et testable reliant des protéines du développement à la surcharge calcique et à la perte neuronale lors de l’AVC néonatal.
Citation: Yang, Q., Wang, CC., Matsuyama, T. et al. A2-pancortins interact with Bcl-xL and WAVE1 to promote mitochondria-ER contact sites (MERCs) and exacerbate mitochondrial calcium elevation to mediate cell death in stroke. Sci Rep 16, 8467 (2026). https://doi.org/10.1038/s41598-026-38928-3
Mots-clés: AVC néonatal, sites de contact mitochondrie-RER, surcharge calcique, protéines pancortines, mort neuronale