Clear Sky Science · fr
Un nouvel axe régulateur C/EBPα–miR-335-5p–PRKAA2 favorise l’accumulation lipidique hépatique dans la MASLD
Pourquoi la stéatose hépatique importe
Beaucoup de personnes qui ne consomment pas beaucoup d’alcool développent tout de même un « foie gras », une affection aujourd’hui appelée maladie hépatique stéatosique associée à un dysfonctionnement métabolique (MASLD). Elle est étroitement liée à l’obésité et au diabète de type 2 et peut évoluer silencieusement vers la fibrose hépatique, la cirrhose, voire le cancer du foie. Cette étude pose une question simple mais cruciale : que se passe-t-il à l’intérieur des cellules du foie qui les pousse à stocker autant de lipides, et peut‑on identifier un interrupteur moléculaire que l’on pourrait désactiver pour protéger le foie ?
Une réaction en chaîne cachée dans les hépatocytes
Les chercheurs se sont intéressés à une réaction en chaîne moléculaire qui relie l’alimentation et le métabolisme à l’accumulation de graisses dans le foie. Ils ont étudié des souris nourries avec un régime riche en graisses et des cellules hépatiques cultivées baignées d’acides gras pour reproduire la MASLD. Dans ces modèles, les animaux ont pris du poids, leurs lipides sanguins ont augmenté et leurs foies se sont remplis de gouttelettes huileuses, reproduisant des caractéristiques clés de la stéatose humaine. Dans ces foies gras, l’équipe a observé qu’un régulateur génétique particulier, un facteur de transcription nommé C/EBPα, et une petite molécule d’ARN, le miR‑335‑5p, étaient tous deux augmentés, tandis qu’une sous‑unité enzymatique protectrice appelée PRKAA2, composante du capteur d’énergie bien connu AMPK, était diminuée.
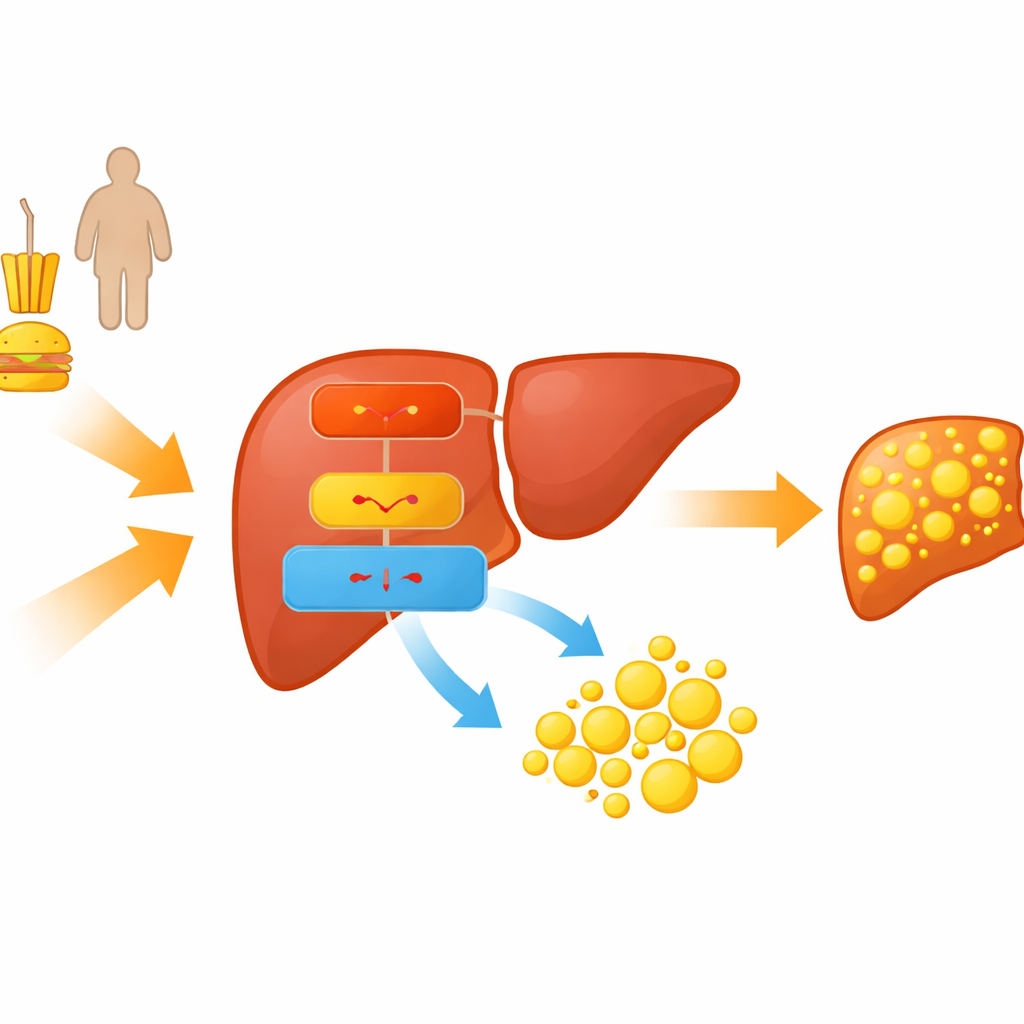
Comment un petit ARN inclina la balance vers les graisses
Les petites molécules d’ARN appelées microARN fonctionnent comme des variateurs moléculaires, en atténuant l’expression de gènes spécifiques. L’équipe a montré que le miR‑335‑5p se lie directement au message codant PRKAA2 et empêche la cellule de produire cette protéine. PRKAA2 participe à l’assemblage du complexe AMPK, qui détecte normalement une faible énergie et réagit en freinant la synthèse lipidique et en favorisant la combustion des graisses. Lorsque les taux de miR‑335‑5p ont été artificiellement augmentés dans des cellules hépatiques, les niveaux de PRKAA2 ont chuté, l’activité de l’AMPK a diminué et les protéines de synthèse lipidique ont augmenté, conduisant à des accumulations visibles de gouttelettes lipidiques. En bloquant le miR‑335‑5p, l’effet inverse a été observé : PRKAA2 et l’activité d’AMPK ont augmenté et l’accumulation de lipides a diminué.
L’interrupteur maître qui déclenche la cascade
Qu’est‑ce qui active le miR‑335‑5p au départ ? En analysant la séquence d’ADN qui contrôle ce microARN, les scientifiques ont prédit plusieurs déclencheurs possibles et se sont concentrés sur C/EBPα, déjà connu pour influencer la gestion des lipides et des glucides. Ils ont confirmé que C/EBPα se lie directement à la région régulatrice de miR‑335‑5p et en stimule l’activité. L’augmentation de C/EBPα dans des cellules hépatiques a élevé les taux de miR‑335‑5p, abaissé PRKAA2, affaibli la signalisation AMPK et favorisé l’accumulation lipidique. L’inhibition de C/EBPα a eu l’effet inverse, renforçant le frein énergétique de la cellule et réduisant les lipides. Des expériences de secours, dans lesquelles miR‑335‑5p était bloqué ou PRKAA2 rétabli, ont montré qu’une grande partie de l’effet pro‑lipidique de C/EBPα transite par cette unique chaîne.
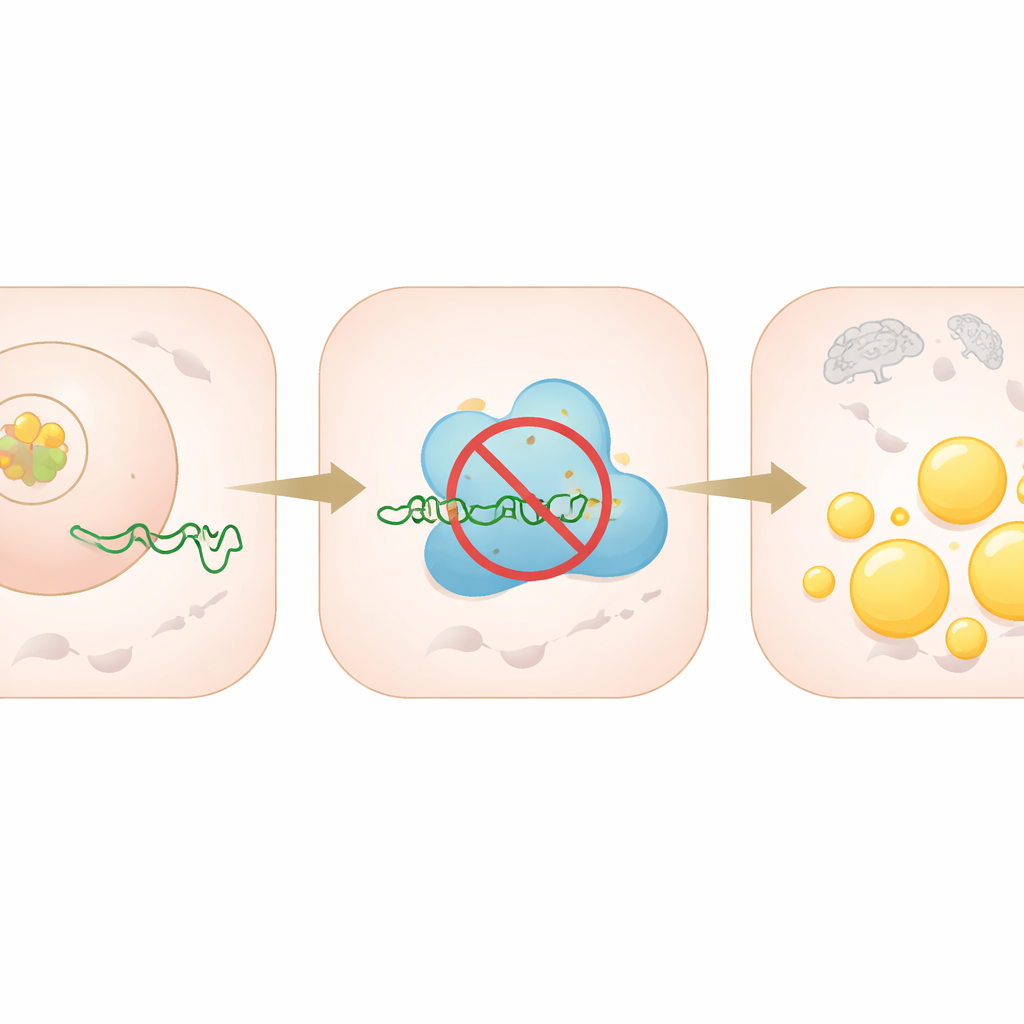
Des boîtes de culture aux souris vivantes
Pour tester si cette voie était pertinente chez l’animal vivant, les chercheurs ont utilisé des virus modifiés pour délivrer des outils génétiques directement dans le foie de souris nourries avec un régime riche en graisses. Un outil réduisait les niveaux de C/EBPα ; un autre captait l’excès de miR‑335‑5p. Dans les deux cas, les foies des animaux contenaient moins de graisses, leur apparence microscopique s’est améliorée, et PRKAA2 ainsi que l’activité d’AMPK ont rebondi, tandis que les protéines responsables de la synthèse lipidique ont diminué. Ces résultats in vivo concordent avec les observations en culture cellulaire et soulignent que la chaîne C/EBPα–miR‑335‑5p–PRKAA2 n’est pas une curiosité de laboratoire mais un moteur puissant de la stéatose hépatique chez un organisme vivant.
Ce que cela signifie pour les traitements futurs
En résumé, l’étude révèle un relais moléculaire en trois étapes qui pousse les cellules hépatiques à accumuler des lipides : C/EBPα active le miR‑335‑5p, qui à son tour éteint PRKAA2 et affaiblit l’AMPK, le frein énergétique de la cellule. Une fois ce frein désactivé, la machinerie de synthèse lipidique fonctionne sans contrôle et le foie se remplit de lipides. Interrompre n’importe quel maillon de ce relais — atténuer C/EBPα, bloquer le miR‑335‑5p ou renforcer PRKAA2/AMPK — a réduit la stéatose chez des souris. Si beaucoup de travail reste à faire avant que de telles stratégies puissent être utilisées en toute sécurité chez l’homme, cette voie offre une cible claire et testable pour de futurs médicaments visant à ralentir ou inverser la MASLD.
Citation: Zeng, X., Xu, Y., You, S. et al. A novel C/EBPα–miR-335-5p–PRKAA2 regulatory axis drives hepatic lipid accumulation in MASLD. Sci Rep 16, 9255 (2026). https://doi.org/10.1038/s41598-026-38918-5
Mots-clés: stéatose hépatique, microARN, AMPK, métabolisme des lipides, maladie métabolique