Clear Sky Science · fr
Profil du microbiote intestinal et des voies métaboliques chez des patients transplantés cardiaques infectés et non infectés avant et après la chirurgie
Pourquoi votre intestin compte après une nouvelle greffe cardiaque
La transplantation cardiaque peut offrir une seconde chance de vie aux personnes atteintes d’une insuffisance cardiaque sévère, mais les infections dans les semaines qui suivent l’opération restent une menace majeure. Cette étude pose une question apparemment simple mais aux grandes conséquences : comment la communauté microbienne de nos intestins — le microbiote intestinal — évolue-t-elle autour d’une transplantation cardiaque, et ces changements peuvent-ils aider à expliquer qui développera une infection et qui n’en développera pas ?
Le minuscule écosystème chez les patients transplantés
Nos intestins abritent des trillions de bactéries qui participent à la digestion, entraînent le système immunitaire et limitent l’implantation de germes envahissants. La chirurgie, les puissants immunosuppresseurs et les antibiotiques à large spectre peuvent tous perturber cet écosystème fragile. Pour suivre ce qui se passe chez les patients transplantés cardiaques, des chercheurs en Chine ont suivi 20 adultes recevant un cœur de donneur. Ils ont prélevé des échantillons de selles environ une semaine avant l’intervention puis 30 jours après, puis ont utilisé le séquençage de l’ADN pour recenser les bactéries présentes et des outils informatiques pour prédire les fonctions métaboliques potentielles de ces microbes.
Quatre groupes de patients, quatre profils microbiens
L’équipe a divisé les patients en quatre groupes : avec et sans infection avant la chirurgie, et avec et sans infection durant le premier mois après l’intervention. Avant la transplantation, la diversité globale et la structure du microbiote intestinal semblaient étonnamment similaires, que les patients aient déjà une infection ou non. Les personnes sans infection préopératoire étaient majoritairement colonisées par un genre bien connu, Bacteroides, souvent associé à un intestin relativement stable. En revanche, les patients infectés présentaient un mélange incluant l’éventuellement néfaste Enterococcus casseliflavus aux côtés de bactéries généralement considérées comme amies, telles que Limosilactobacillus et Weissella cibaria, suggérant une communauté intestinale en équilibre précaire et en évolution.
Après la chirurgie : bifurcation du trajet microbien
Trente jours après l’opération, le microbiote des patients qui n’ont pas développé d’infection a pris un profil identifiable, tandis que ceux qui ont présenté des infections étaient très différents. Les patients non infectés présentaient des communautés microbiennes plus riches et plus équilibrées, avec de nombreux membres du genre Blautia et des bactéries apparentées productrices de butyrate, un acide gras à chaîne courte connu pour nourrir les cellules intestinales et soutenir la stabilité immunitaire. Leurs écosystèmes intestinaux paraissaient diversifiés et équilibrés. Chez les patients infectés, en revanche, la diversité a chuté et la communauté a été dominée par Enterococcus faecium, une bactérie résistante souvent impliquée dans les infections nosocomiales. Les analyses statistiques ont montré que le microbiote de ce groupe infecté formait un groupe distinct de tous les autres, indiquant une dysbiose claire après la chirurgie.
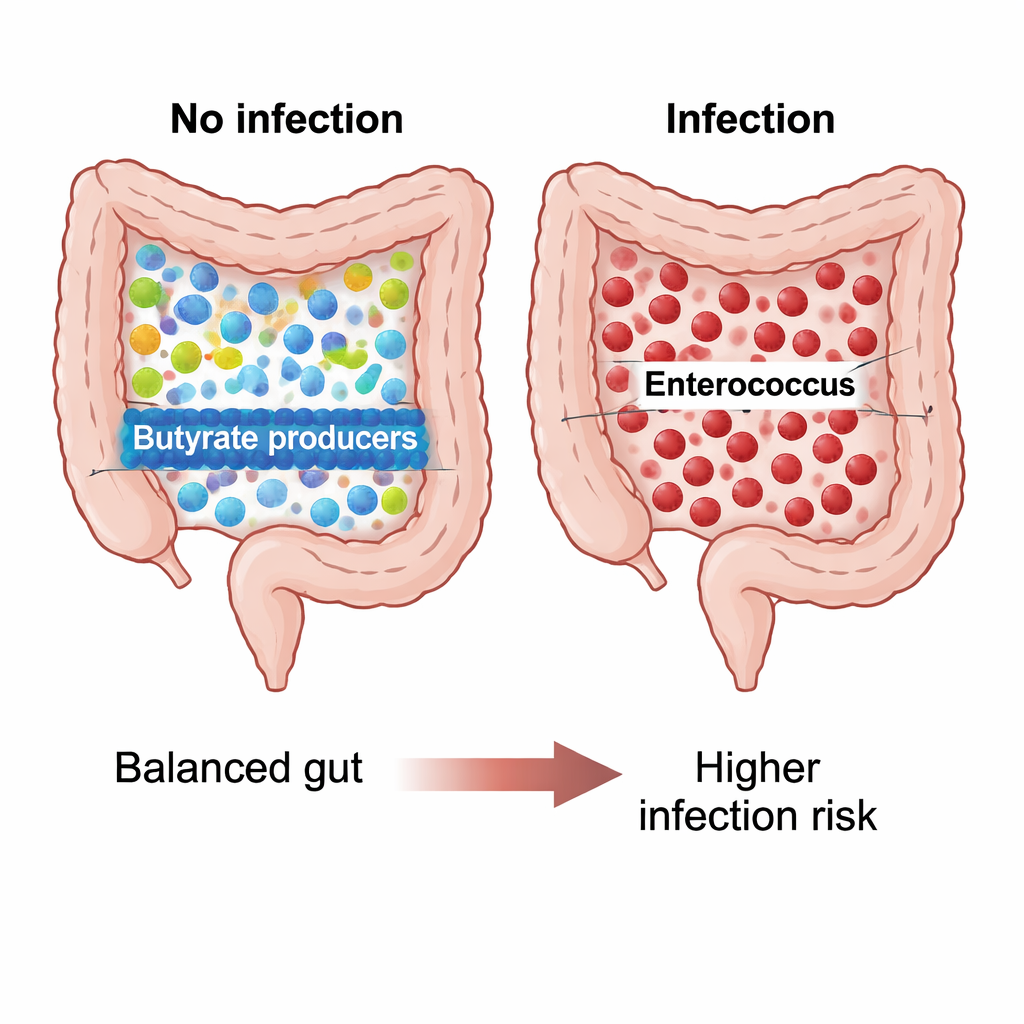
La chimie microbienne liée à protection ou risque
Les chercheurs ont aussi interrogé les fonctions chimiques potentielles de ces microbes. À l’aide de logiciels de prédiction, ils ont observé que, dans le groupe post-opératoire non infecté, Blautia était associé à des voies dégradant un composé appelé L-1,2-propanediol, un intermédiaire de la fermentation des fibres qui alimente la production d’acides gras bénéfiques comme le propionate. Chez les patients infectés, ce potentiel métabolique prédit était nettement réduit, cohérent avec une communauté intestinale moins capable de produire des molécules protectrices. Avant la chirurgie, Enterococcus casseliflavus chez les patients infectés était lié à des routes de fermentation inhabituelles pouvant refléter un environnement microbien stressé et en quête d’énergie, bien que cela nécessite une confirmation expérimentale directe.
Ce que cela signifie pour les patients et les équipes soignantes
Pour les personnes qui envisagent une transplantation cardiaque, ces résultats suggèrent que l’intestin n’est pas un simple spectateur ; il pourrait contribuer à façonner le risque d’infections graves. L’étude met en évidence un passage dynamique de la dominance de Bacteroides avant la chirurgie vers, selon l’évolution postopératoire, soit un enrichissement protecteur en Blautia soit une prolifération nuisible d’Enterococcus. Un fort stress lié à l’infection et l’usage d’antibiotiques semblent pousser la communauté intestinale vers un état pauvre en diversité dominé par Enterococcus, tel que retrouvé chez les patients infectés. Les auteurs proposent une stratégie « à double cible » : favoriser le retour des bactéries productrices de butyrate — par l’alimentation ou des probiotiques choisis avec soin — tout en surveillant de près les niveaux d’Enterococcus. Bien que des études plus nombreuses et sur des durées plus longues soient nécessaires, ce travail ouvre la voie à une prise en charge future des transplantations dans laquelle l’ajustement du microbiote intestinal deviendrait un volet courant de la protection des patients contre des infections potentiellement mortelles.
Citation: Han, J., Hua, L., Yang, B. et al. Gut microbiota and metabolic pathway profiles in infected and non-infected heart transplant patients before and after surgery. Sci Rep 16, 7697 (2026). https://doi.org/10.1038/s41598-026-38911-y
Mots-clés: transplantation cardiaque, microbiote intestinal, infection postopératoire, antibiotiques, bactéries productrices de butyrate