Clear Sky Science · fr
Évaluation de la relation évolutive de la protéine de liaison à la boîte TATA (TBP) avec diverses configurations de repliement des domaines protéiques à l’aide de machines à vecteurs de support (SVM)
Comment une protéine « interrupteur » de l’ADN se relie à beaucoup d’autres
La protéine de liaison à la boîte TATA, ou TBP, est un pilier de nos cellules : elle aide à activer les gènes en saisissant l’ADN à de nombreux promoteurs. Cette étude pose une question apparemment simple mais aux grandes implications : existe‑t‑il d’autres protéines, avec des fonctions très différentes, qui partagent discrètement la forme sous‑jacente de la TBP ? En combinant comparaison de structures 3D, analyse de séquences et outils modernes d’apprentissage automatique, les auteurs retracent des liens familiaux cachés entre la TBP et des protéines impliquées dans le métabolisme, la chimie des neurotransmetteurs et même des voies liées au cancer.
Une protéine clé au cœur du contrôle des gènes
La TBP se situe à la porte de l’expression génique chez des organismes allant de la levure à l’homme. Elle reconnaît une courte séquence d’ADN appelée boîte TATA et courbe l’ADN pour aider à assembler la grosse machinerie de transcription qui copie les gènes en ARN. Parce que cette étape est si centrale, le repliement — l’agencement tridimensionnel — du noyau de la TBP est fortement conservé au cours de l’évolution. Les auteurs se concentrent sur une structure de TBP bien étudiée, connue sous le nom de 1tba, et l’utilisent comme sonde pour rechercher d’autres protéines pouvant partager son plan architectural, même si leurs séquences d’acides aminés et leurs tâches courantes paraissent très différentes au premier abord.
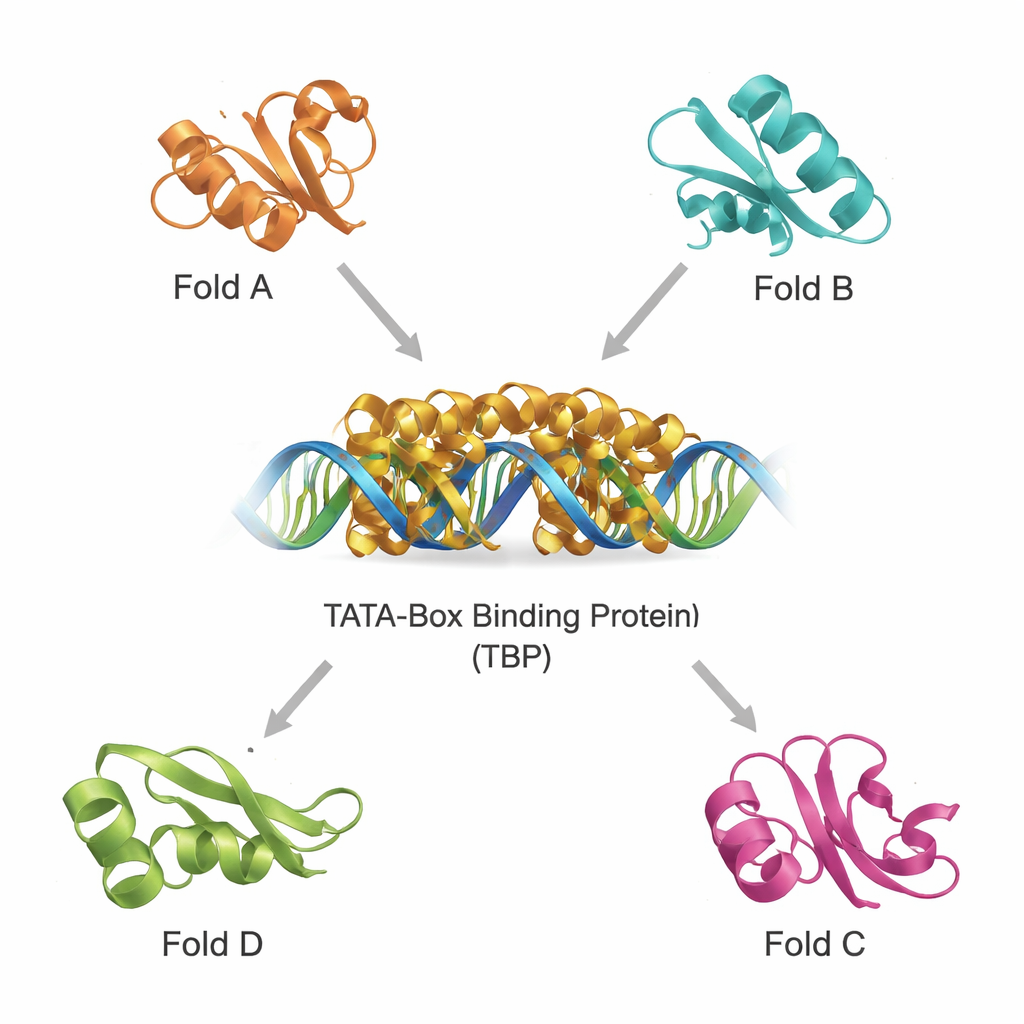
Trouver des cousins structuraux dans un univers protéique dense
Les bases de données modernes contiennent des centaines de milliers de structures protéiques, ce qui permet de rechercher des parents lointains par la forme 3D plutôt que par la séquence seule. À l’aide de deux outils puissants, DALI et TOP‑search, l’équipe a d’abord extrait des protéines dont le repliement ressemblait à celui de la TBP. Ils ont ensuite classé ces candidats à l’aide d’un catalogue évolutif de domaines et les ont réduits à un petit ensemble d’exemples structurellement similaires mais fonctionnellement divers. Parmi eux figurent une enzyme de synthèse de glutamine importante pour le métabolisme, un domaine présent dans plusieurs enzymes manipulant l’ARNt, une enzyme au repliement distinctif en « hot‑dog » impliquée dans la chimie des acides gras, et des protéines participant à la synthèse de la tétrahydrobioptérine, une molécule cruciale pour le fonctionnement cérébral. La superposition de leurs structures sur celle de la TBP a montré que, malgré des fonctions différentes, elles partagent des motifs centraux reconnaissables.
Apprendre aux machines à reconnaître des familles protéiques cachées
Pour dépasser l’inspection au cas par cas, les auteurs ont construit des modèles d’apprentissage automatique capables de signaler automatiquement les repliements de type TBP. Ils ont assemblé de grands ensembles de séquences protéiques connues comme appartenant à la TBP ou à chacun des repliements apparentés, ainsi qu’un large ensemble de « fond » d’enzymes non apparentées. Chaque protéine a été convertie en résumés numériques simples : la fréquence d’apparition de chaque acide aminé et la fréquence de chaque paire possible d’acides aminés dans la séquence. Ces profils ont alimenté des machines à vecteurs de support (SVM) et des forêts aléatoires, qui ont appris à séparer un type de repliement de tous les autres. Grâce à une validation croisée rigoureuse, les modèles ont atteint une très haute précision — souvent supérieure à 95 % — même lorsqu’ils étaient entraînés uniquement sur des parties des séquences correspondant à des régions conservées.
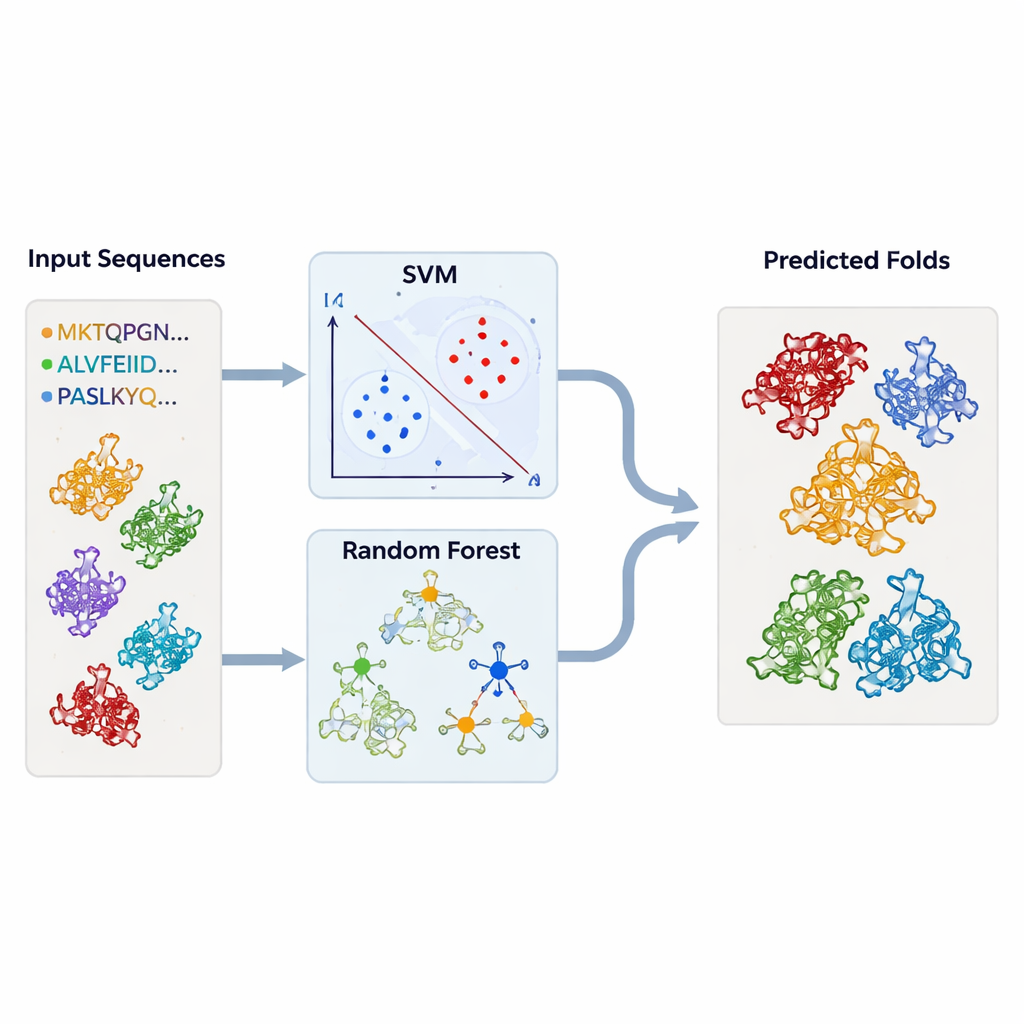
Tester les modèles sur des milliers de structures inconnues
Armés de ces classificateurs entraînés, l’équipe est retournée aux bases de données structurelles. Ils ont passé des milliers de chaînes protéiques — récupérées via DALI et TOP‑search — dans leurs modèles pour voir lesquelles présentaient les profils statistiques caractéristiques des repliements de type TBP ou apparentés. Les approches SVM et forêt aléatoire étaient largement concordantes et ont identifié de nombreux candidats que les outils structurels avaient également signalés comme similaires. Dans certains cas, des enzymes aux activités apparemment sans rapport se sont néanmoins regroupées fortement avec la TBP ou entre elles, renforçant l’idée que l’évolution peut réutiliser le même cadre de base pour de nombreux rôles biochimiques différents.
Pourquoi ces connexions cachées comptent
L’étude conclut que la TBP partage une profonde ascendance structurelle avec plusieurs familles d’enzymes, y compris des protéines de type glutamine synthétase et des domaines d’édition des enzymes de traitement de l’ARNt. Même lorsque les séquences se sont éloignées et que les fonctions ont divergé, ces protéines conservent des motifs architecturaux communs, suggérant une descendance à partir d’un ancêtre partagé. Pour le non‑spécialiste, le message principal est que la nature a tendance à recycler des conceptions performantes : un même repliement peut être adapté à plusieurs reprises pour résoudre des problèmes très différents, de l’activation des gènes à la régulation fine du métabolisme et de la chimie cérébrale. En combinant la comparaison de structures 3D avec l’apprentissage automatique, les auteurs fournissent une boîte à outils pratique pour découvrir de telles relations, aidant les biologistes à prédire la fonction de protéines non caractérisées et orientant les développeurs de médicaments vers de nouvelles cibles dictées par l’évolution dans des voies pertinentes pour la maladie.
Citation: Selvaraj, M.K., Kaur, J. Evaluating the evolutionary relationship of TATA binding protein (TBP) with various folding patterns of protein domains using support vector machine (SVM). Sci Rep 16, 7696 (2026). https://doi.org/10.1038/s41598-026-38883-z
Mots-clés: Protéine de liaison à la boîte TATA, évolution des protéines, apprentissage automatique, structure des protéines, machine à vecteurs de support