Clear Sky Science · fr
Mesures de masse volumique cellulaire en cellule unique par centrifugation dans un microcanal à gradient
Pourquoi peser des cellules minuscules importe
Chaque cellule vivante est plus qu’un simple sac de molécules ; son poids et sa compacité racontent quelque chose de sa santé. De subtils changements dans la densité d’emballage d’une cellule peuvent indiquer si elle croît, meurt, combat une infection ou devient cancéreuse. Pourtant, malgré ce potentiel, mesurer la masse volumique de milliers de cellules individuelles est resté lent, techniquement exigeant et coûteux. Cet article présente une nouvelle méthode, beaucoup plus simple, pour « peser » des cellules uniques en observant comment elles flottent ou coulent dans un liquide contrôlé à l’intérieur d’un canal de verre d’un cheveu de diamètre, tournant dans une centrifugeuse.
Une nouvelle variante d’une vieille astuce de labo
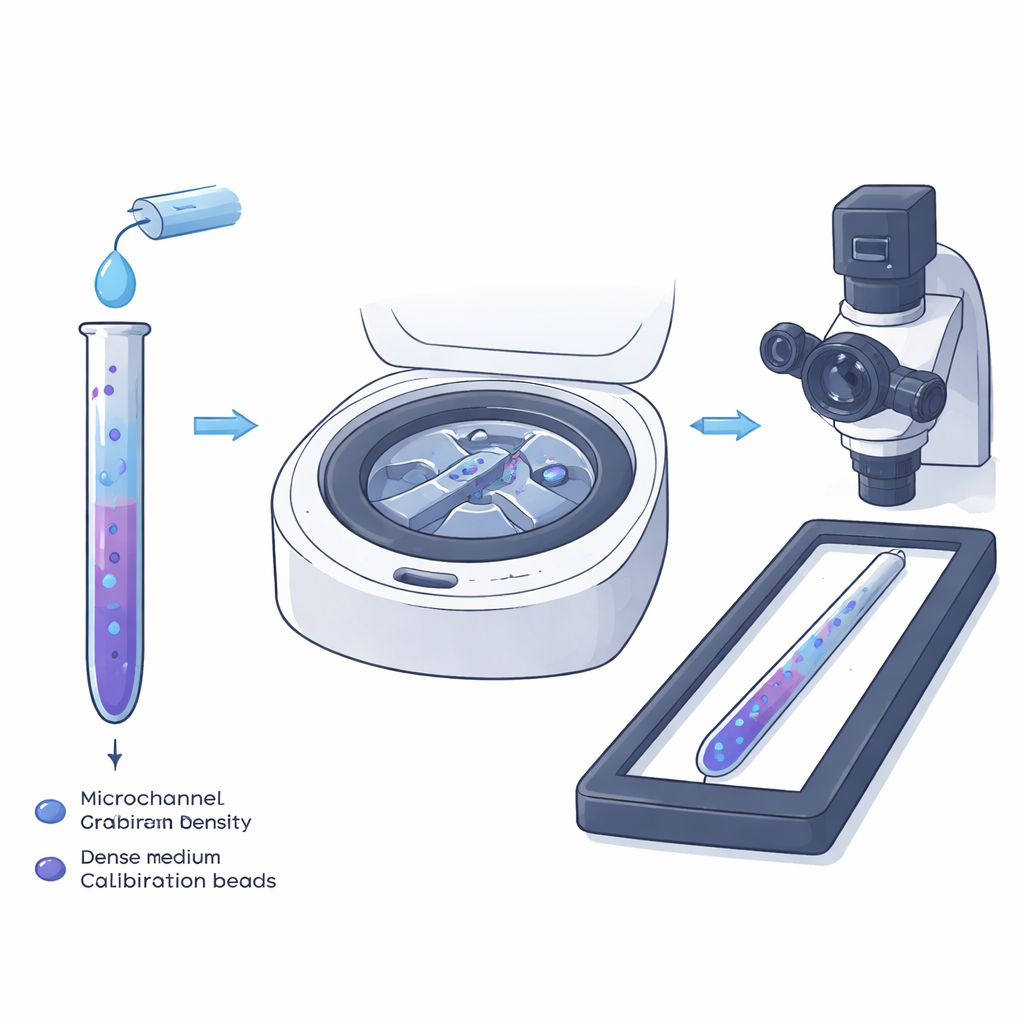
La centrifugation sur gradient de densité traditionnelle est depuis longtemps utilisée en tubes à essai pour séparer des mélanges cellulaires : lorsqu’on fait tourner, les cellules se positionnent au point d’un liquide stratifié où leur propre densité égale celle du fluide environnant. Les auteurs miniaturisent cette idée dans un microcanal étroit de sorte que des cellules individuelles, et pas seulement des couches, puissent être mesurées directement au microscope. Ils remplissent d’abord le canal avec un liquide léger contenant les cellules, puis avec un liquide plus lourd contenant de petites billes plastiques aux densités précisément connues. Quand ces deux liquides se rencontrent et s’écoulent dans le canal minuscule, ils forment naturellement un gradient de densité unidimensionnel et lisse le long de sa longueur.
Créer une pente de densité lisse
À l’intérieur de tels canaux fins, le fluide s’écoule lentement et de manière laminaire, sans turbulence. Dans ces conditions, le profil d’écoulement parabolique mélange juste assez les liquides léger et lourd pour créer une transition graduelle, plutôt qu’une frontière nette, entre eux. L’équipe a étudié ce processus expérimentalement à l’aide d’un colorant fluorescent et par simulations informatiques. Ils ont constaté qu’un gradient de densité presque linéaire s’étendant sur plusieurs millimètres peut se former en quelques secondes. La hauteur du canal s’est révélée cruciale : des canaux peu profonds maintiennent le gradient stable et empêchent le liquide plus lourd, poussé par la gravité, de se balancer, ce qui brouillerait la relation entre position et densité et introduirait des erreurs dans les mesures cellulaires finales.
Faire tourner les cellules jusqu’à leur point d’équilibre
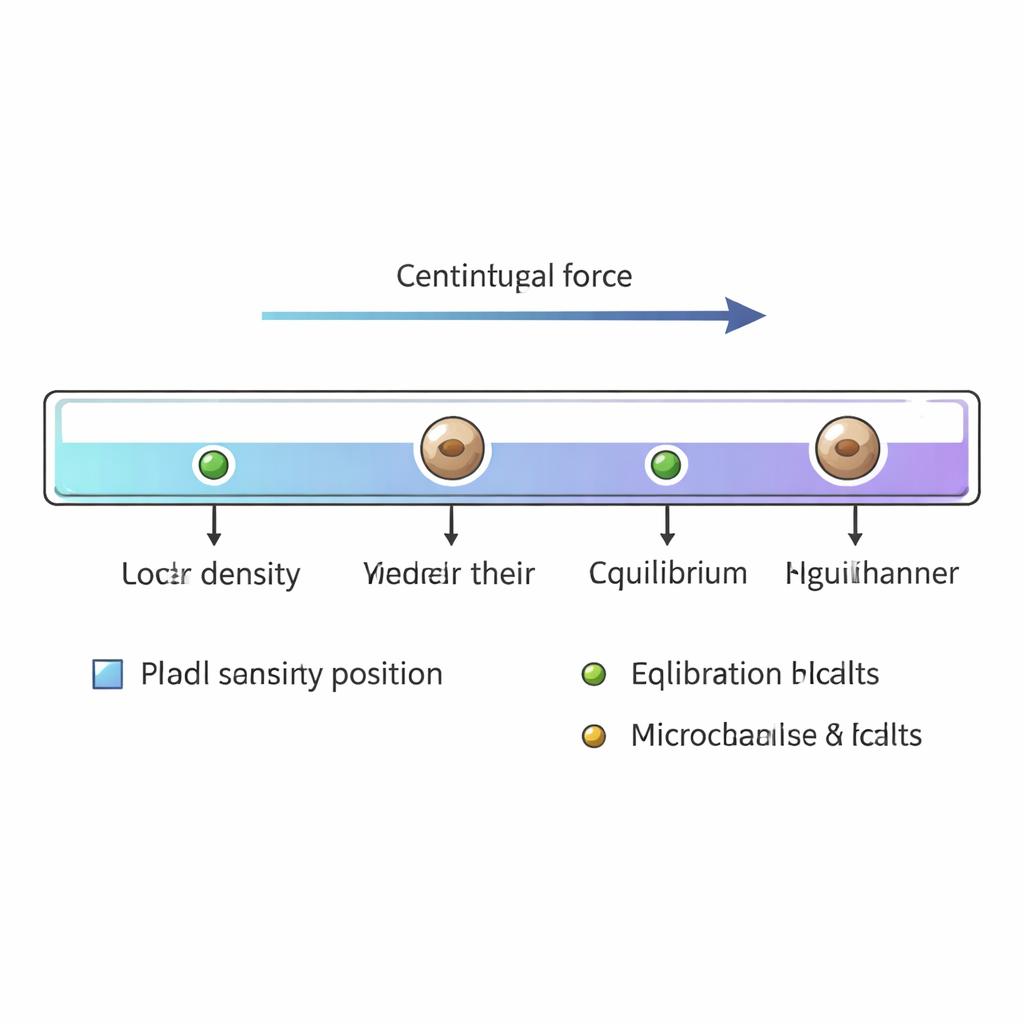
Une fois le canal rempli, ses extrémités sont scellées et il est placé dans une petite centrifugeuse. Tournant à environ 12 000 tours par minute, les cellules et les billes d’étalonnage se déplacent le long du canal jusqu’à ce que la force centrifuge vers l’extérieur soit exactement équilibrée par la poussée d’Archimède à leur densité propre. De taille supérieure à environ trois micromètres de diamètre, les cellules de levure atteignent cet équilibre en moins de 20 secondes. Après environ une minute et demie de rotation, le canal est retiré et observé au microscope standard. Les chercheurs enregistrent les positions de milliers de cellules de levure individuelles et des billes de référence, puis convertissent chaque position le long du gradient en une valeur de masse volumique en utilisant les densités connues des billes comme points d’ancrage.
Lire la santé cellulaire à partir de minuscules différences
Avec cette approche, les auteurs ont mesuré les densités de plus de 20 000 cellules de levure à travers plusieurs canaux. L’incertitude typique de mesure pour une cellule unique était d’environ 3,3 kilogrammes par mètre cube — suffisamment faible pour distinguer de réelles différences biologiques, qui étaient à peu près deux fois plus grandes dans leurs échantillons. Sur plusieurs heures, ils ont observé que la population principale de levures conservait une densité stable, tandis qu’une seconde population, plus dense et légèrement plus petite, apparaissait progressivement. Ce groupe plus dense était probablement constitué de cellules mortes ou endommagées ayant incorporé le fluide lourd, les rendant plus compactes. Les valeurs mesurées correspondaient bien aux résultats obtenus par des techniques beaucoup plus complexes et plus lentes, telles que les résonateurs microcanaux en suspension, des méthodes optiques et la lévitation magnétique.
Du prototype de laboratoire au biomarqueur pratique
L’étude montre qu’une combinaison simple de microcanaux en verre, de centrifugeuses grand public et de microscopes standard peut fournir des mesures de masse volumique en cellule unique à haut débit, à un rythme d’environ 16 000 cellules par heure. Bien que la méthode ne soit pas encore assez sensible pour détecter les plus infimes variations induites par des médicaments, elle est déjà suffisamment puissante pour distinguer différents types cellulaires ou différencier cellules vivantes et mortes en fonction de leur compacité. En rendant la « pesée » cellulaire précise plus accessible et abordable, cette méthode de gradient en microcanal pourrait aider à transformer la masse volumique cellulaire en un biomarqueur de routine pour surveiller les maladies, évaluer des thérapies et explorer la régulation interne des cellules.
Citation: Soller, R., Augustsson, P. & Barnkob, R. Single-cell mass-density measurements using microchannel gradient centrifugation. Sci Rep 16, 6501 (2026). https://doi.org/10.1038/s41598-026-38872-2
Mots-clés: masse volumique cellule unique, microfluidique, centrifugation, levures, biomarqueurs cellulaires